夏照帆院士领衔!开发新型环肽药物为脓毒症治疗提供突破性策略
| 导读 | 该研究进一步拓展了C5a靶向策略在感染性疾病中的应用价值,未来需进一步明确其临床治疗窗口,并探索与支持疗法的联合策略。 |
11月5日,海军军医大学第一附属医院夏照帆/罗子淼&复旦大学药学院陆伟跃团队发表于国际顶尖期刊《信号转导与靶向治疗》(Signal Transduction and Targeted Therapy,IF=52.7)的一项重磅研究揭示了一种新型长效C5a阻断环肽药物Cp1,可通过精准抑制补体系统关键介质C5a,有效阻断脓毒症引发的炎症级联反应,从而预防多器官功能障碍并显著延长生存期。该研究为脓毒症这一高死亡率疾病的防治提供了创新解决方案。
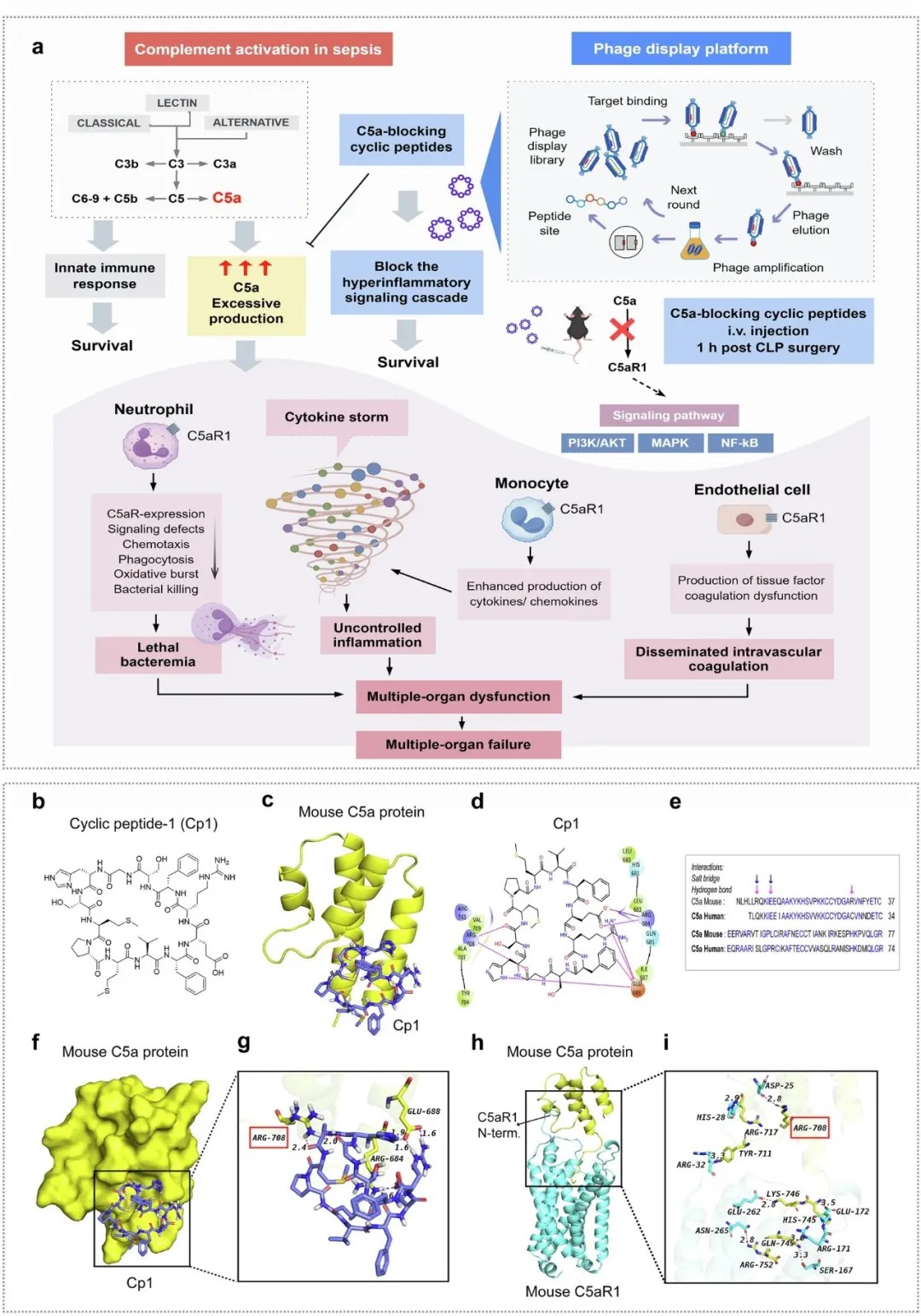
一种用于脓毒症预防性治疗的新型C5a阻断环肽药物Cp1
研究背景:脓毒症治疗困境与补体系统
脓毒症是宿主对感染反应失调导致的危及生命的综合征,其死亡率高达28%-56%。目前临床针对细胞因子风暴的治疗策略(如单抗、激素等)存在覆盖范围有限、副作用大或易引发继发感染等问题。
补体系统作为先天免疫的核心环节,其过度激活是脓毒症炎症放大的关键驱动因素。研究指出,C5a是补体系统中最强的过敏毒素,其趋化作用比C3a强20倍,能招募中性粒细胞、单核细胞等免疫抑制性细胞至炎症部位,加剧组织损伤。然而,传统C5a抑制剂存在半衰期短、稳定性差或成本高昂等局限。该研究中Cp1的研发旨在通过靶向上游瓶颈分子C5a,实现炎症瀑布反应的高效遏制,同时保留补体系统的有益功能。
研究亮点:Cp1的优势与作用机制
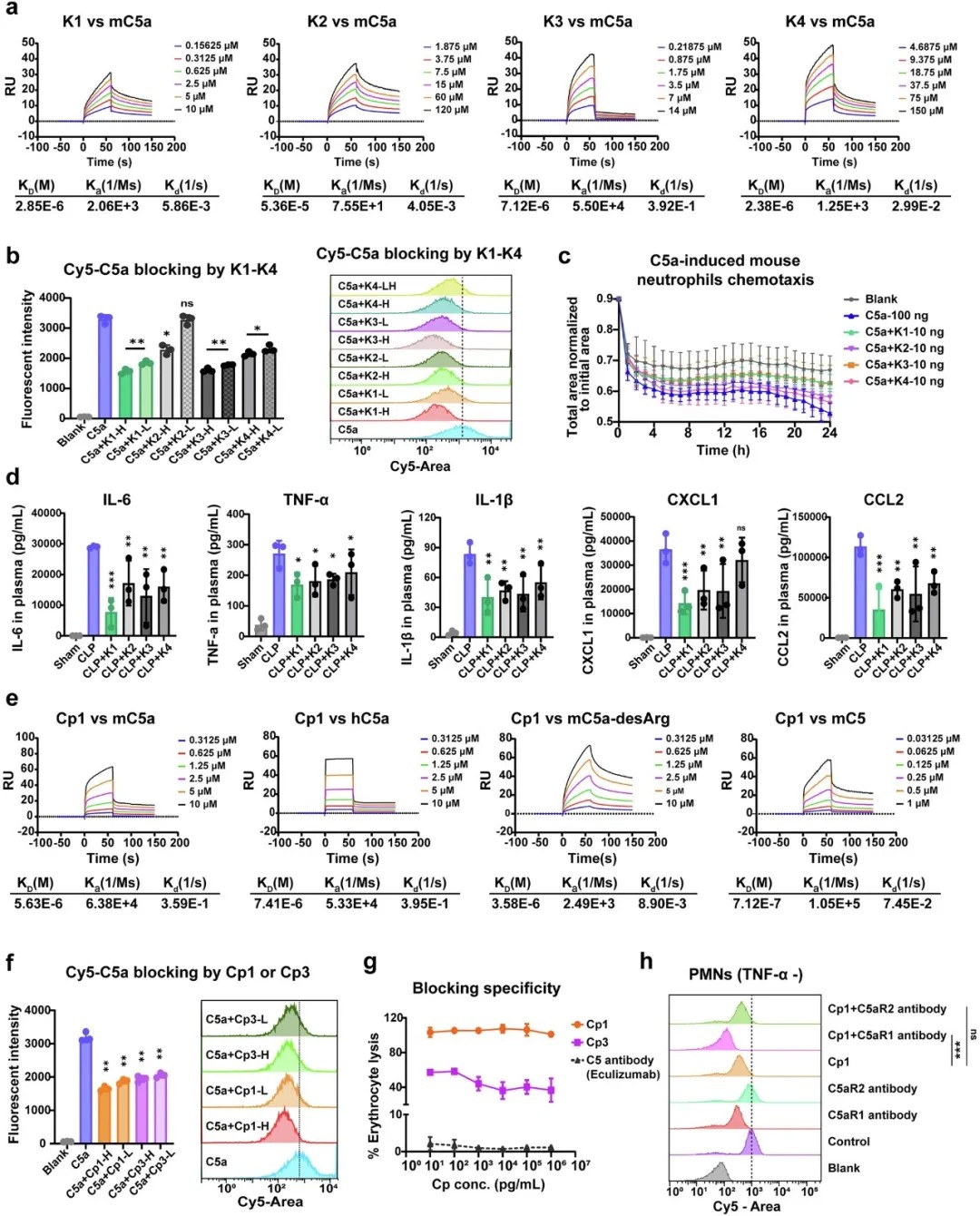
C5a阻断剂Cp1的结合亲和力与阻断特异性验证
Cp1通过噬菌体展示技术从12肽库中筛选得到,并经头尾环化修饰优化其稳定性。分子对接分析显示,Cp1与小鼠C5a形成6个氢键和2个盐桥,其结合位点与线性肽K1显著不同,能更有效破坏C5a与受体C5aR1的相互作用。
关键特性验证:
-
高亲和力与特异性:Cp1对小鼠和人类C5a的表现出高亲和力,且不干扰C5裂解或膜攻击复合物形成,避免增加感染风险。
-
长效循环能力:单次给药后,Cp1在血浆中保留90%初始浓度达14天,远超C5a的5分钟半衰期。
-
炎症抑制效果:在CLP诱导的脓毒症模型中,Cp1显著降低血浆和腹腔灌洗液中的IL-6、TNF-α等炎性因子水平(最高抑制99%),并恢复中性粒细胞吞噬功能。
作用机制:器官保护与生存获益

Cp1治疗的小鼠对继发感染的反应,以及Cp1治疗诱导的外周血单核细胞mRNA水平的变化
Cp1治疗通过多重机制缓解脓毒症病理损伤:
-
改善器官功能:血清ALT、AST、尿素和肌酐水平显著下降,提示肝肾功能保护。
-
减轻肺损伤:肺组织湿干重比降低85%,血管通透性标志物(VCAM-1、E-选择素)减少71%-100%。
-
调控凝血异常:凝血参数(PT、APTT)趋于正常,抑制补体-凝血交叉对话。
-
提升生存率:单剂Cp1将脓毒症小鼠中位生存时间从30小时延长至120小时,7天生存率达60%,而对照组为零。
RNA测序分析显示,Cp1预处理可逆转C5a诱导的2552个上调基因中的87.5%,其中G蛋白偶联趋化因子受体活性相关通路下调最显著。此外,体外细胞毒性实验及血液生化指标均未发现Cp1引发的免疫毒性或肝肾功能损伤。
未来展望与临床意义
Cp1的环化设计兼具抗体类长效循环特性与小分子药物的成本优势,其独特的作用机制为脓毒症预防和治疗提供了新范式。该研究进一步拓展了C5a靶向策略在感染性疾病中的应用价值,未来需进一步明确其临床治疗窗口,并探索与支持疗法的联合策略。(转化医学网360zhyx.com)
原文链接:
https://www.nature.com/articles/s41392-025-02457-8
【关于投稿】
转化医学网(360zhyx.com)是转化医学核心门户,旨在推动基础研究、临床诊疗和产业的发展,核心内容涵盖组学、检验、免疫、肿瘤、心血管、糖尿病等。如您有最新的研究内容发表,欢迎联系我们进行免费报道(公众号菜单栏-在线客服联系),我们的理念:内容创造价值,转化铸就未来!
转化医学网(360zhyx.com)发布的文章旨在介绍前沿医学研究进展,不能作为治疗方案使用;如需获得健康指导,请至正规医院就诊。
责任声明:本稿件如有错误之处,敬请联系转化医学网客服进行修改事宜!
微信号:zhuanhuayixue
 腾讯登录
腾讯登录






还没有人评论,赶快抢个沙发