辅助化疗引起乳癌转移?救了乳腺却害了肺!|Nature子刊
| 导读 | 在乳腺癌的治疗中,先对患者进行化疗,抑制肿瘤生长,再进行手术切除病灶。也就是所谓的新辅助化疗,但在2017年,《科学》杂志报道发现新辅助化疗可能通过肿瘤转移微环境(TMEM)机制诱发乳腺癌转移,从此引发了人们新的思考 |
在乳腺癌的治疗中,先对患者进行化疗,抑制肿瘤生长,再进行手术切除病灶。也就是所谓的新辅助化疗,但在2017年,《科学》杂志报道发现新辅助化疗可能通过肿瘤转移微环境(TMEM)机制诱发乳腺癌转移,从此引发了人们新的思考,而现在《Nature》新的研究又为此增添了新的证据。新辅助化疗,真是让人欢喜让人忧。
通过化学药物来抑制肿瘤细胞分裂,患者的病情往往能得到立竿见影的控制。新辅助化疗是指在实施手术前所做的全身化疗,目的是使肿块缩小、及早杀灭看不见的转移细胞,以利于后续的手术、放疗等治疗。
在乳腺癌的治疗中,医生们往往会先对患者进行化疗,抑制患者肿瘤的生长,然后再进行手术,切除病灶。在这些情况下,患者在手术后很可能终身“无癌”。
但2017年,美国《科学》杂志却发文称:乳腺癌细胞通过TIE2/MENACalc/MENAINV通路进行扩散即为肿瘤转移微环境(TMEM),根据临床验证为乳腺癌患者转移的预后标志。该研究发现,术前新辅助化疗可使肿瘤缩小,同时也可能为肿瘤细胞进入血液循环提供途径,使其容易发生远处转移。
在接受多柔比星+环磷酰胺+紫杉醇新辅助化疗的小鼠中,反映乳腺癌细胞转移“门窗”的TMEM评分、MENAINV表达密度和活性显著增加。同时还发现,在接受乳腺癌化疗的小鼠中,全身和肺部的乳腺癌细胞数量显著增加。所以,新辅助化疗引起了人们新的思考,“to be or not to be,that's a question”。
近期,《Nature》子刊发表文章称,又发现了一项新的证据来支持化疗可引起乳癌转移。

外泌体中的annexin-A6
来自瑞士洛桑联邦理工学院(EPFL)的科学家们在小鼠模型中做了深度研究,研究人员使用肿瘤模型小鼠,发现经常用于患者的两种化疗药物:紫杉醇和阿霉素,可诱导乳腺肿瘤细胞释放出“外泌体”。外泌体是由细胞分泌出的小囊泡,内部含有核酸和蛋白等物质。
(红色为外泌体)
在接受化疗的实验动物中,肿瘤外泌体里的annexin-A6(膜联蛋白-A6)水平有明显上升。外泌体从肿瘤细胞中释放后,可以在血液中循环。到达肺部后,外泌体释放其内容物,包括膜联蛋白-A6。
它刺激肺部细胞释放另一种蛋白质——CCL2,而CCL2可以吸引单核细胞,引起免疫反应。这种免疫反应可能很危险,因为之前的研究表明,单核细胞可以促进肺癌细胞的存活和生长,这是转移的最初步骤之一。
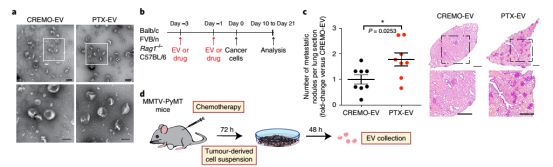
紫杉醇增加了转移性肺结节的数量
“简而言之,我们的研究已经确定了化疗与乳腺癌转移之间的新联系,”De Palma说。
从动物到人体
研究人员证实了他们的实验室数据,发现在接受新辅助化疗的乳腺癌患者的外泌体中膜联蛋白-A6水平也有所增加。然而,De Palma警告不要妄下结论:“虽然这一观察结果支持了我们研究结果,但目前我们还不知道膜联蛋白-A6是否在人类乳腺癌中具有任何促转移活性”。
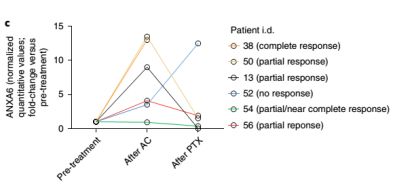
(与治疗前水平相比,六个病例中有五个患者的ANXA6含量增加)
研究阻断方法
研究人员发现在化疗期间,采取措施中和膜联蛋白-A6或阻断单核细胞,可防止乳腺肿瘤转移至肺部。这些结果可能有助于提高新辅助化疗的疗效和安全性。“各种单核细胞抑制剂已被开发用于临床,因此可以与新辅助化疗联合,以潜在地限制外泌体介导的不良副作用,”研究者说。
敲重点:不可片面看问题
临床研究小组补充说:“我们的研究结果并不是去阻止患者接受新辅助化疗。” “对于许多侵袭性乳腺癌,新辅助化疗仍然是一种必不可少的治疗方法,正如多项临床试验所示,目前来看仍利大于弊。”我们目前是发现了新辅助化疗的一个缺点,就是它有可能促进肿瘤转移,我们会进一步研究它的具体机制,从发生机制上找到阻断方法。
参考资料:
[1] Neoadjuvant chemotherapy induces breast cancer metastasis through a TMEM-mediated mechanism
[2]Ioanna Keklikoglou et al., (2018), Chemotherapy elicits pro-metastatic extracellular vesicles in breast cancer models, Nature Cell Biology
[3] Tumors backfire on chemotherapy, Retrieved January 1, 2019, from https://www.eurekalert.org/pub_releases/2018-12/epfd-tbo122618.php
(转化医学网360zhyx.com)
 腾讯登录
腾讯登录







还没有人评论,赶快抢个沙发