Nature重磅发布!90万人群分析揭示DNA重复序列在人类生命周期中的动态变化规律
| 导读 | 研究首次系统性地量化了短串联重复序列(STRs)在体细胞与生殖细胞中的不稳定性,并发现其与多种疾病风险密切相关,为神经退行性疾病的机制研究与治疗策略提供了新视角。 |
近日,一项发表于国际知名期刊《Nature》的大型研究通过对90万生物样本库参与者数据的分析,揭示了DNA重复序列在人类生命周期中的动态变化规律。研究首次系统性地量化了短串联重复序列(STRs)在体细胞与生殖细胞中的不稳定性,并发现其与多种疾病风险密切相关,为神经退行性疾病的机制研究与治疗策略提供了新视角。
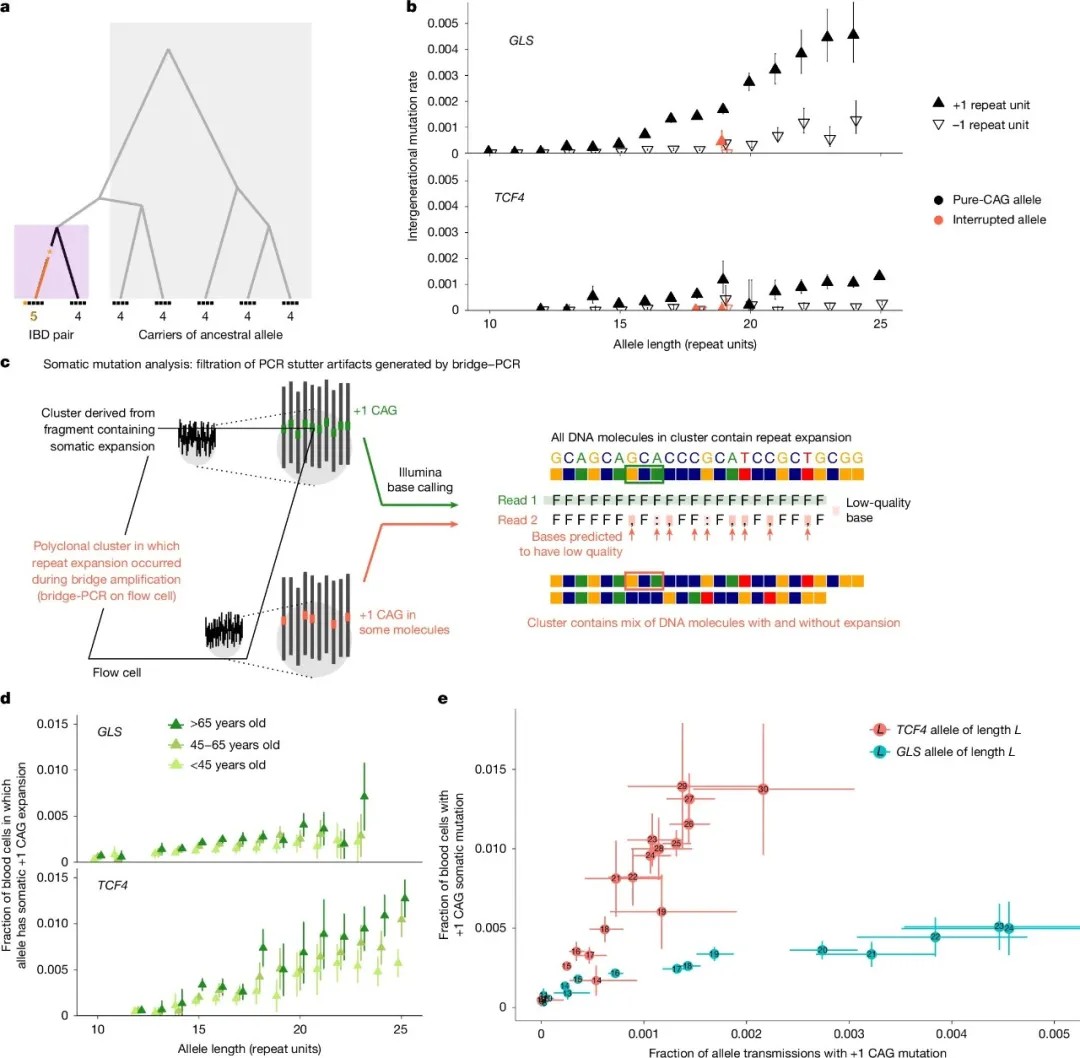
常见CAG重复等位基因的生殖系与体细胞不稳定性
DNA重复序列的“自我修复”与不稳定性
人类基因组中超过50%的区域由重复序列组成,其中三核苷酸重复序列的异常扩增与亨廷顿病、肌强直性营养不良等50多种神经退行性疾病相关。早期研究发现,DNA分子可通过“短途旅行”至细胞核边缘进行自我修复,其中核孔复合物蛋白通过调控修复蛋白Rad52促进DNA稳定性。然而,当重复序列长度超过临界值,修复机制可能失效,导致疾病发生。
体细胞扩增:驱动疾病进展的“隐形时钟”
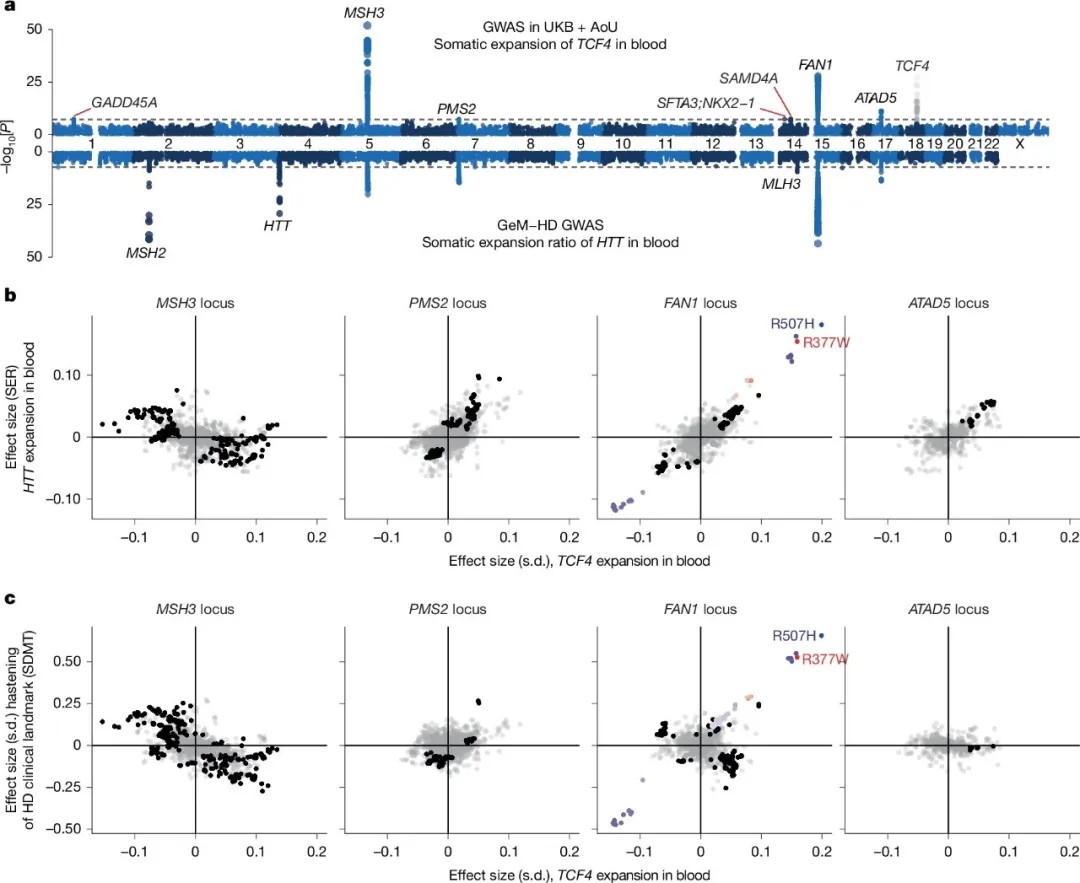
血液中TCF4重复等位基因体细胞扩展的遗传影响
最新研究通过对亨廷顿病患者脑组织的单细胞分析发现,携带40次以上CAG重复序列的神经元中,重复长度会随年龄增长缓慢增加;一旦重复次数超过80次,扩增速度急剧加快,并在达到150次时触发神经元死亡。这一过程被比喻为“滴答作响的DNA时钟”,解释了为何患者多在中年才出现症状——此时大量神经元的重复扩增已突破致命阈值。此外,不同神经元积累重复序列的速率差异极大,导致疾病进展的个体差异显著。
DNA修复蛋白的双重角色

17种不稳定短串联重复序列(STRs)遗传影响的变异
DNA修复蛋白在重复序列稳定性调控中呈现复杂作用。经典复制蛋白A(RPA)可通过解链异常DNA结构、增强FAN1核酸内切酶活性促进修复,而其替代形式Alt-RPA则抑制修复过程,加速CAG重复扩增。研究还发现,MSH3、FAN1等修复基因的常见单倍型可显著影响不同组织中的重复不稳定性。
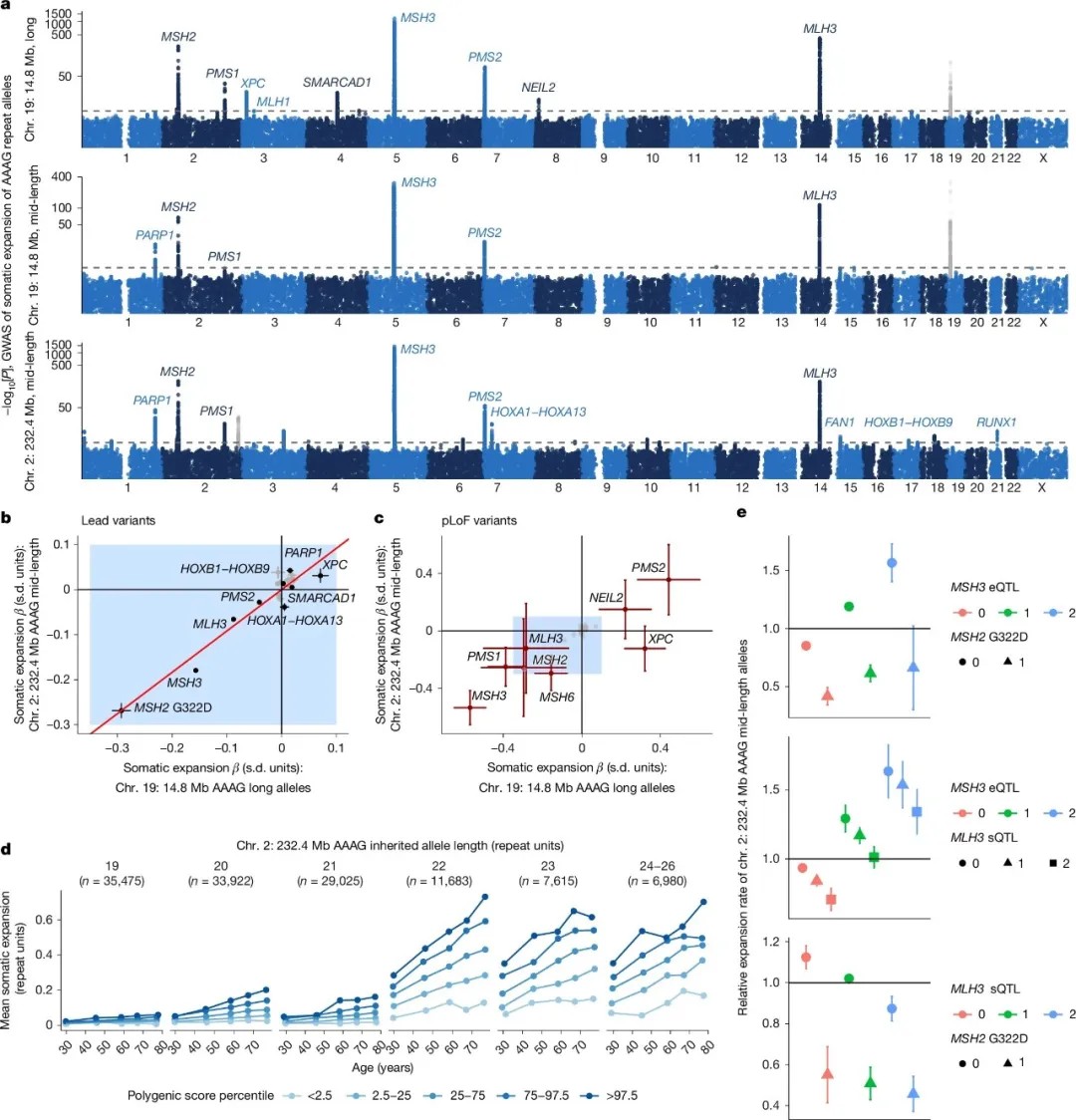
血液中常见AAAG重复体细胞扩展的遗传决定因素
新型致病重复与临床关联
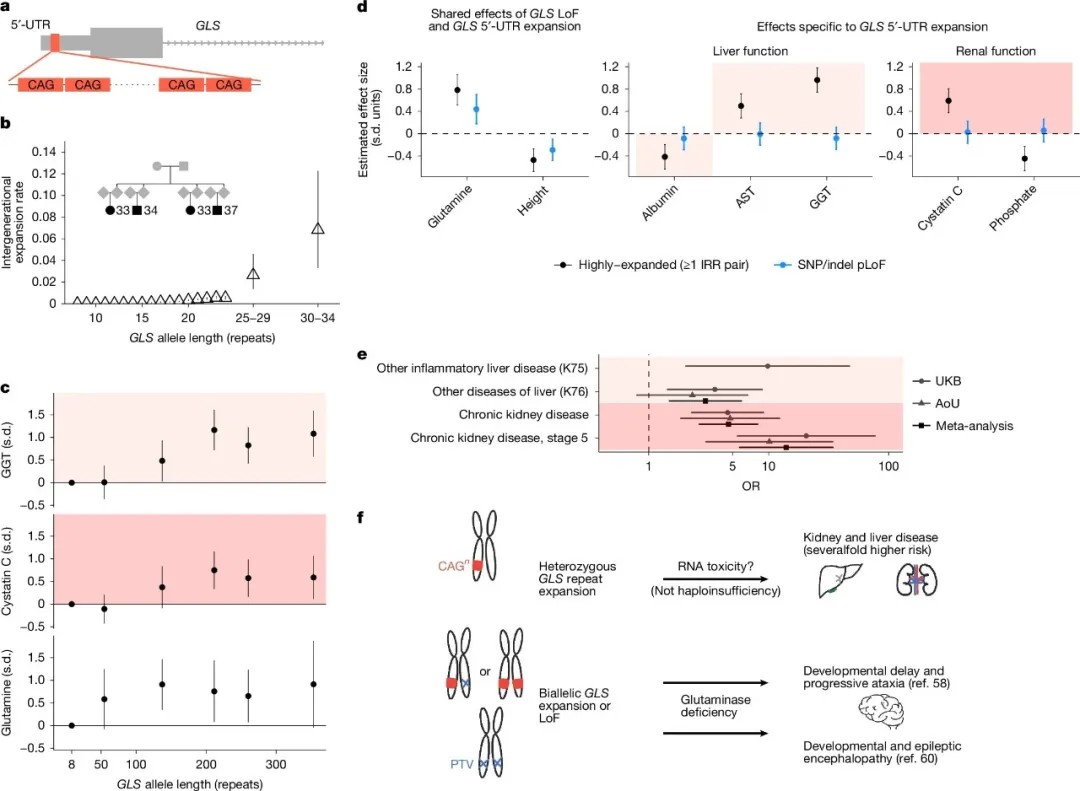
5′ UTR内CAG重复扩展的不稳定性与致病性
研究首次报道了5′-UTR的GLS基因CAG重复扩展与肝肾疾病的关联。携带高度扩展GLS重复(≥100次)的个体,患晚期慢性肾病风险提高14倍,肝病风险提高3倍。值得注意的是,这种致病性仅出现在重复高度扩展的等位基因中,而GLS功能丧失突变并未导致类似表型,提示其机制可能涉及RNA毒性而非蛋白质功能缺失。
研究意义与未来展望
DNA重复序列的动态变化已成为理解遗传性疾病机制的关键。随着测序技术与生物信息学方法的革新,科学家正逐步揭示重复不稳定性在衰老与疾病中的核心作用,为精准诊疗开辟新路径。(转化医学网360zhyx.com)
原文链接:
https://www.nature.com/articles/s41586-025-09886-z
【关于投稿】
转化医学网(360zhyx.com)是转化医学核心门户,旨在推动基础研究、临床诊疗和产业的发展,核心内容涵盖组学、检验、免疫、肿瘤、心血管、糖尿病等。如您有最新的研究内容发表,欢迎联系我们进行免费报道(公众号菜单栏-在线客服联系),我们的理念:内容创造价值,转化铸就未来!
转化医学网(360zhyx.com)发布的文章旨在介绍前沿医学研究进展,不能作为治疗方案使用;如需获得健康指导,请至正规医院就诊。
责任声明:本稿件如有错误之处,敬请联系转化医学网客服进行修改事宜!
微信号:zhuanhuayixue
 腾讯登录
腾讯登录









还没有人评论,赶快抢个沙发