新免疫调节功能!苏州大学附属第四医院等单位发文:有前景的抗肿瘤治疗靶点
| 导读 | 总的来说,CSC 乙酰辅酶 A 在抗肿瘤治疗中是一个很有前景的治疗靶点。 |
近日,苏州大学附属第四医院/上海交通大学医学院附属仁济医院/上海交通大学附属第六人民医院研究团队合作共同在期刊《Advanced Science》上发表了研究论文,题为“Cancer Stem Cells Shift Metabolite Acetyl-Coenzyme A to Abrogate the Differentiation of CD103+ T Cells”,在此,研究人员证明了癌症干细胞(CSCs)在非小细胞肺癌(NSCLC)患者中对 CD103+ T 细胞分化起着关键的抑制作用。具体而言,CSCs 通过依赖外泌体的途径促进代谢物乙酰辅酶 A(acetyl-CoA)向相互作用的 T 细胞转移。Blimp-1 的乙酰化增强了其与 E3 泛素连接酶 LIS1 的相互作用,从而促进 Blimp-1 的降解,最终阻碍 CD103+ T 细胞的分化。相应地,使用 CD133 抗体偶联纳米颗粒靶向 CSCs 和 acetyl-CoA 生物合成可增加肿瘤浸润的 CD8+CD103+ T 细胞并抑制肿瘤生长。尤其是,使用 NSCLC 患者来源的类器官(PDOs)和人源化 PDO-NSG 嵌合体的研究证实,阻断 acetyl-CoA 的生成、CSCs 的外泌体分泌以及参与 Blimp-1 乙酰化和泛素化的关键酶能够有效恢复 CD103+ T 细胞的分化。总的来说,CSC 乙酰辅酶 A 在抗肿瘤治疗中是一个很有前景的治疗靶点。

https://advanced.onlinelibrary.wiley.com/doi/10.1002/advs.202513535
非小细胞肺癌治疗之挑战:聚焦T细胞机制优化策略
01
肺癌仍是癌症相关死亡的首要原因,其中非小细胞肺癌(NSCLC)占临床患者的主导地位,约占 85%。对于无法手术切除的患者,免疫治疗与放化疗相结合正成为新的标准治疗方案。癌症的发展和进展与肿瘤微环境(TME)中癌细胞和抗肿瘤 T 细胞之间的相互作用密切相关。TME 是一个复杂的生态系统,包含成纤维细胞、内皮细胞以及先天性和适应性免疫细胞。肿瘤细胞能够扰乱 T 细胞上免疫检查点蛋白的表达,这是关键的免疫逃逸机制。这一原理支持在 TME 中应用免疫检查点阻断(ICB)疗法。然而,在临床实践中,大多数患者对包括 ICB 在内的治疗方案无反应,甚至可能导致一系列器官特异性炎症,甚至多器官衰竭。因此,探究抗肿瘤 T 细胞的缺陷和功能障碍的机制对于优化临床治疗具有重要意义。
靶向CSC-T 细胞相互作用以挽救 CD103+ T 细胞分化并限制非小细胞肺癌的生长
02
尽管小鼠肿瘤模型极大地促进了研究人员对肿瘤生物学的理解,并在抗肿瘤疗法的开发中发挥了关键作用,但在小鼠研究中表现出疗效的药物却常常在人类肿瘤中失效。相比之下,患者来源的类器官(PDOs)对于常规药物和试验性药物的反应特征与相应患者的情况极为相似。因此,研究人员从非小细胞肺癌(NSCLC)患者身上获取了外周血单个核细胞(PBMCs),并培养了与其匹配的 PDOs,以模拟体内条件,并评估靶向CSC 介导的 Blimp-1 乙酰化的靶向治疗在转化应用中的效果。尽管 NSCLC PDOs 能够降低相互作用的 T 细胞中 Blimp-1 的蛋白水平,但用 BMS303141 和 ACSS2 抑制剂预先处理 PDOs 能够有效恢复 Blimp-1 的表达以及 CD103+ T 细胞的分化。这一效果通过预先用 ACLY 和 ACSS2 靶向 shRNA 转染 PDOs 并与 PBMC 共培养得到证实,同样促进了 CD103+ T 细胞的分化。此外,在 T 细胞中敲低 GCN5 也恢复了 PDO 条件下 CD103+ T 细胞中 Blimp-1 的蛋白水平。尤其是,在肺类器官(PDOs)中靶向乙酰辅酶 A 合成以及在 T 细胞中靶向 GCN5 显著抑制了非小细胞肺癌(NSCLC)肺类器官的生长。这些发现表明,破坏肿瘤干细胞介导的 Blimp-1 乙酰化是治疗非小细胞肺癌的一种有前景的策略。
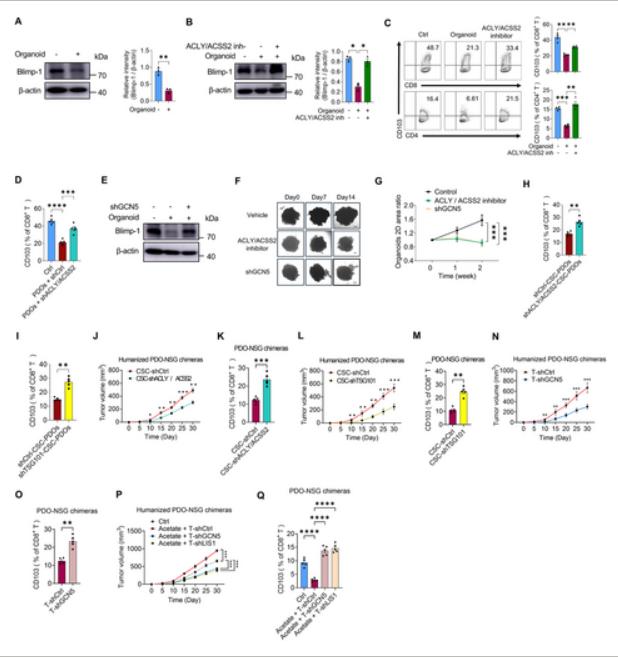
阻断 CSC 介导的 CD103⁺ T 细胞抑制以抑制非小细胞肺癌的扩张(转化医学网360zhyx.com)
参考资料:
https://advanced.onlinelibrary.wiley.com/doi/10.1002/advs.202513535
【关于投稿】
转化医学网(360zhyx.com)是转化医学核心门户,旨在推动基础研究、临床诊疗和产业的发展,核心内容涵盖组学、检验、免疫、肿瘤、心血管、糖尿病等。如您有最新的研究内容发表,欢迎联系我们进行免费报道(公众号菜单栏-在线客服联系),我们的理念:内容创造价值,转化铸就未来!
转化医学网(360zhyx.com)发布的文章旨在介绍前沿医学研究进展,不能作为治疗方案使用;如需获得健康指导,请至正规医院就诊。
责任声明:本稿件如有错误之处,敬请联系转化医学网客服进行修改事宜!
微信号:zhuanhuayixue
 腾讯登录
腾讯登录









还没有人评论,赶快抢个沙发