双抑制剂组合!显著增强抗肿瘤效果!复旦大学郭伟剑团队发现胃癌治疗潜在靶点
| 导读 | 转移是癌症治疗的瓶颈,研究表明长链非编码RNAs(lncRNAs)在调节癌症转移中发挥着关键作用,但对lncRNAs在胃癌中的研究仍有限。 |
3月29日,复旦大学郭伟剑研究团队在期刊《Cell Death&Disease》上发表了题为“LncRNA SNHG26 promotes gastric cancer progression and metastasis by inducing c-Myc protein translation and an energy metabolism positive feedback loop”的研究论文。本研究中,功能实验表明,SNHG26在体内外均可促进细胞上皮-间充质转化和增殖。机制上,SNHG26与核仁素(NCL)相互作用,通过增加c-Myc的转化来调节其表达,进而通过己糖激酶2(HK2)促进能量代谢,从而促进胃癌恶性发展。能量代谢的增加为促进c-Myc的转化和表达提供了足够的能量,形成了正反馈循环。此外,代谢和转化抑制剂可以阻断这一循环,从而抑制细胞增殖和迁移,且两种抑制剂联合应用可增强抗肿瘤效果,提示其在GC 治疗中具有潜在的治疗前景。

https://www.nature.com/articles/s41419-024-06607-8#Sec36
研究背景
01
胃癌(GC)是人类第五种常见的肿瘤,每年估计有超过100万新病例。由于其高转移频率,GC 是导致癌症相关死亡的第四大原因,超过60% 的患者在诊断时呈现局部或远处转移。尽管在分子靶向药物和免疫治疗方面取得了实质性进展,但由于转移的存在,GC 患者的5年生存率仍然不理想。因此,迫切需要对 GC 转移机制进行调查,以开发新的治疗方法。
长链非编码RNA(lncRNA)超过200个核苷酸,具有有限的蛋白质编码能力。lncRNA被广泛表达,并在基因调控中发挥关键作用。lncRNA通过与RNA、DNA和蛋白质相互作用发挥多种功能。大量研究表明,lncRNA的异常表达与癌细胞行为相关。lncRNA BDNF-AS/WDR5/FBXW7轴通过调节VDAC3泛素化介导胃癌腹膜转移中的铁死亡。lncRNA TNFRSF10A-AS1通过与MPZL1结合促进胃癌进展。然而,由于lncRNA数量众多,其机制复杂,我们对胃癌中lncRNA的认识仍然有限。
研究进展
02
为了证实SNHG26在体内的致癌作用,研究人员首先通过将过表达SNHG26的MKN-28细胞注射到裸鼠皮下生成皮下肿瘤模型。4周后,将小鼠处死,并称量肿瘤。SNHG26过表达组的肿瘤比对照组大,表明SNHG26可以促进肿瘤生长。接下来,研究人员将过表达SNHG26的MKN-28细胞注射到裸鼠尾静脉中,以评估转移能力。8周后,将小鼠处死,并量化肺中的转移位点。此外,HE染色显示SNHG26过表达组的肺部转移位点数量显著高于对照组。而且,皮下肿瘤的免疫组化显示SNHG26过表达后E-cad表达降低。总的来说,体内外结果表明SNHG26促进胃癌的增殖和转移。
研究还表明,SNHG26通过c-Myc/HK2途径介导糖酵解和能量代谢,促进胃癌细胞的增殖和迁移,糖酵解代谢增加提供能量促进mRNA转化,形成正反馈循环,代谢和转化抑制剂阻断该正反馈循环作用,抑制癌细胞增殖和迁移。两者联合抑制可增加抗肿瘤效果,提示其在胃癌治疗中具有潜在的治疗前景。
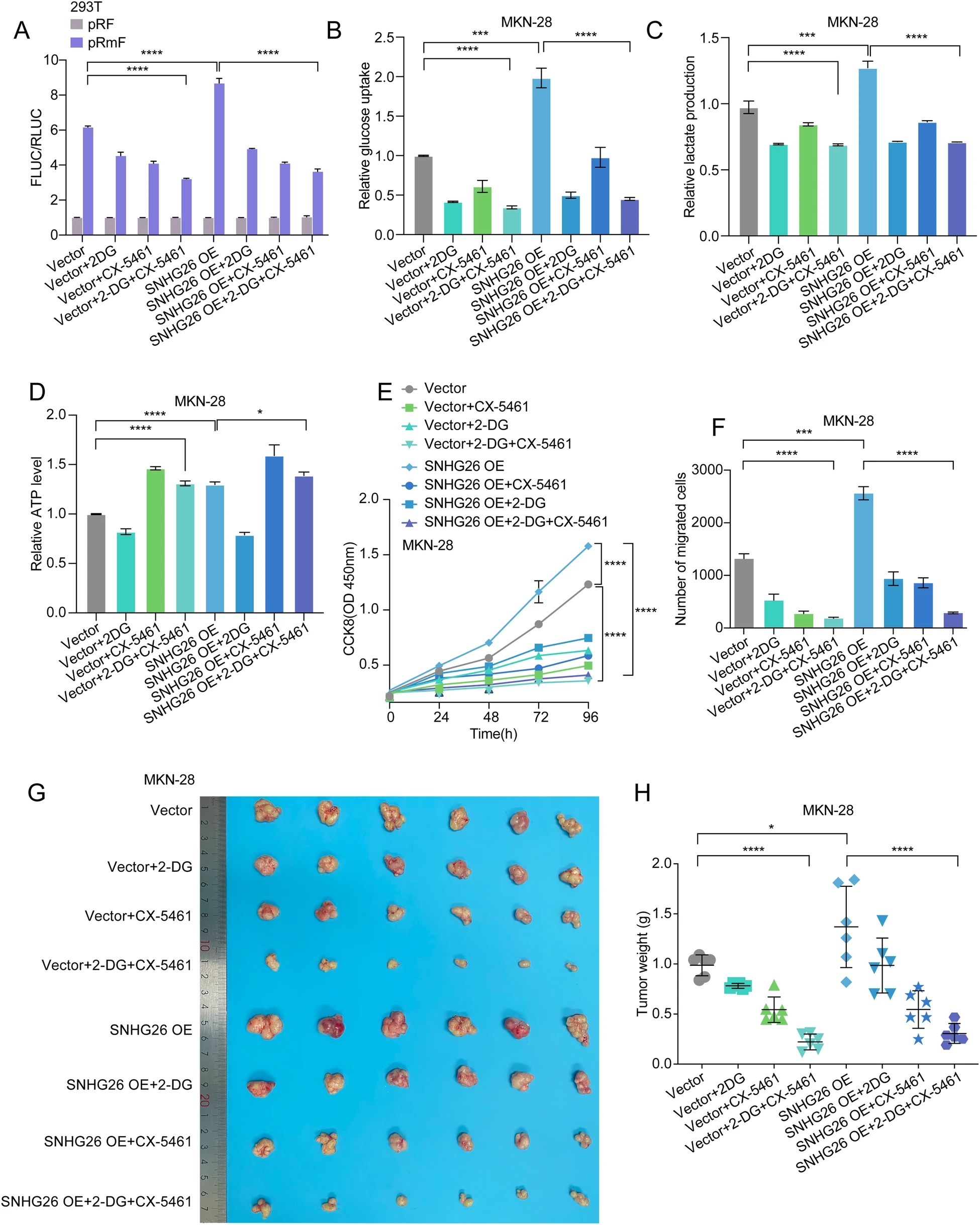
转化抑制剂(CX-5461)和代谢抑制剂(2-DG)的联合使用在体内和体外均有显著的治疗效果
研究结论
03
总之,研究人员发现了一种新的lncRNA SNHG26,它在胃癌中表达上调。SNHG26与NCL相互作用,通过增加c-Myc的转化促进胃癌的增殖和转移。本研究揭示了lncRNA在转化和转移之间的新机制,表明SNHG26/NCL/c-Myc轴是胃癌的潜在治疗靶点。(转化医学网360zhyx.com)
参考资料:
https://www.nature.com/articles/s41419-024-06607-8#Sec36
注:本文旨在介绍医学研究进展,不能作为治疗方案参考。如需获得健康指导,请至正规医院就诊。
 腾讯登录
腾讯登录








还没有人评论,赶快抢个沙发