免疫逃避“元凶”!复旦大学徐洁杰、郭剑明发文:助力“克服”癌症免疫治疗耐药性
| 导读 | 免疫疗法正在获得发展势头,但目前的治疗方法在受益者方面存在局限性。透明细胞肾细胞癌 (ccRCC) 在所有实体瘤中含有最高表达的人白细胞抗原 E (HLA-E),即 NKG2A 的配体。在这项研究中,我们旨在研究NKG2ACD8 T细胞在肿瘤微环境中的作用及其作为ccRCC新靶点的潜力。 |
近日,复旦大学基础医学院徐洁杰教授联合复旦大学附属中山医院郭剑明教授共同通讯在期刊《Journal for Immuno Therapy of Cancer》上发表文章“NKG2ACD8 T cells infiltration determines immunosuppressive contexture and inferior response to immunotherapy in clear cell renal cell carcinoma”,研究发现ccRCC 中 NKG2ACD8 T 细胞浸润较高的患者表现出较短的总生存期和对免疫治疗的耐药性。NKG2ACD8 T 细胞表达上调的检查点分子,并显示出受损的效应功能,以及组织驻留特征。程序性细胞死亡蛋白-1 (PD-1) 阻断和 NKG2A 阻断的组合证明了重新激活 CD8 T 细胞效应器功能的增强能力。

https://jitc.bmj.com/content/12/1/e008368
研究背景
01
肾细胞癌(RCC)是泌尿系统三大恶性肿瘤之一。2020年,全球新发肾细胞癌病例超过40万例,其中透明细胞肾细胞癌(ccRCC)约占75%,是最常见的病理类型。与非转移性局限性 ccRCC 患者的 5 年生存概率较高(超过 80%)相比,其他 20%-50% 的转移性肾细胞癌 (mRCC) 患者的生存率会大大降低,大多数仅在手术后 3 年内发生。
在过去十年中,免疫疗法彻底改变了mRCC的治疗。与单独使用酪氨酸激酶抑制剂(TKI)相比,III期试验的最新结果表明,基于免疫检查点阻断(ICB)加TKI的联合治疗显着改善了mRCC患者的预后。因此,亟需探索mRCC患者新的治疗方法。
有趣的是,与其他肿瘤不同,CD8 T 细胞的强烈浸润与 ccRCC 的较差预后相关,这可能是由于不同 CD8 T 细胞亚型的功能细分。我们小组之前还发现,在ccRCC中,TNFRSF9CD8 T细胞同时具有耗竭和效应表型,CXCL13CD8 T细胞具有抗肿瘤功能受损的耗竭表型。
NKG2A 是 C 型凝集素家族成员,可在细胞表面与 CD94 形成二聚体。与程序性细胞死亡蛋白-1/程序性细胞死亡配体 1 (PD-1/PD-L1) 通路不同,NKG2A 独立于 T 细胞受体 (TCR) 起作用。非经典的主要组织相容性复合物-I 分子人白细胞抗原-E (HLA-E) 是 NKG2A-CD94 的主要配体。在实体瘤中,ccRCC代表了HLA-E表达的最高水平。据报道,NKG2A 主要在 CD8αβ T 细胞、CD56hi 自然杀伤 (NK) 细胞和自然杀伤 T (NKT) 细胞中表达。NKG2A-CD94与HLA-E结合可抑制T细胞和NK细胞的活化。先前的研究表明,NKG2A拮抗作用主要通过NKG2ACD8 T细胞而不是NKG2A NK细胞在肿瘤疫苗治疗耐药个体中发挥作用。然而,NKG2ACD8 T细胞在肿瘤微环境(TME)中的作用以及靶向NKG2A在ccRCC中的治疗效果仍然未知。
研究进展
02
由于 NKG2A CD8 T 细胞的较高浸润与对免疫治疗的反应较差有关,因此我们通过使用新鲜 ccRCC 组织的体外干预模型进一步探索了这些患者的潜在治疗方法。干预分为4组,即对照组、PD-1单克隆抗体(nivolumab)治疗组、NKG2A单克隆抗体(mAb)治疗组和联合治疗组(图 5A)。在纳武利尤单抗体外干预后,CD8 T细胞上NKG2A表达较低的患者在CD8 T细胞中表现出IFN-γ和GZMB的显著上调(图5B-D),证实了NKG2A CD8 T细胞浸润较高的患者对免疫治疗的反应较差。此外,在纳武利尤单抗干预后,CD8 T细胞显示NKG2A的表达增加(图5E;p=0.047),这表明基于抗NKG2A和抗PD-1的联合治疗可能增加PD-1阻断单药治疗的潜在价值。
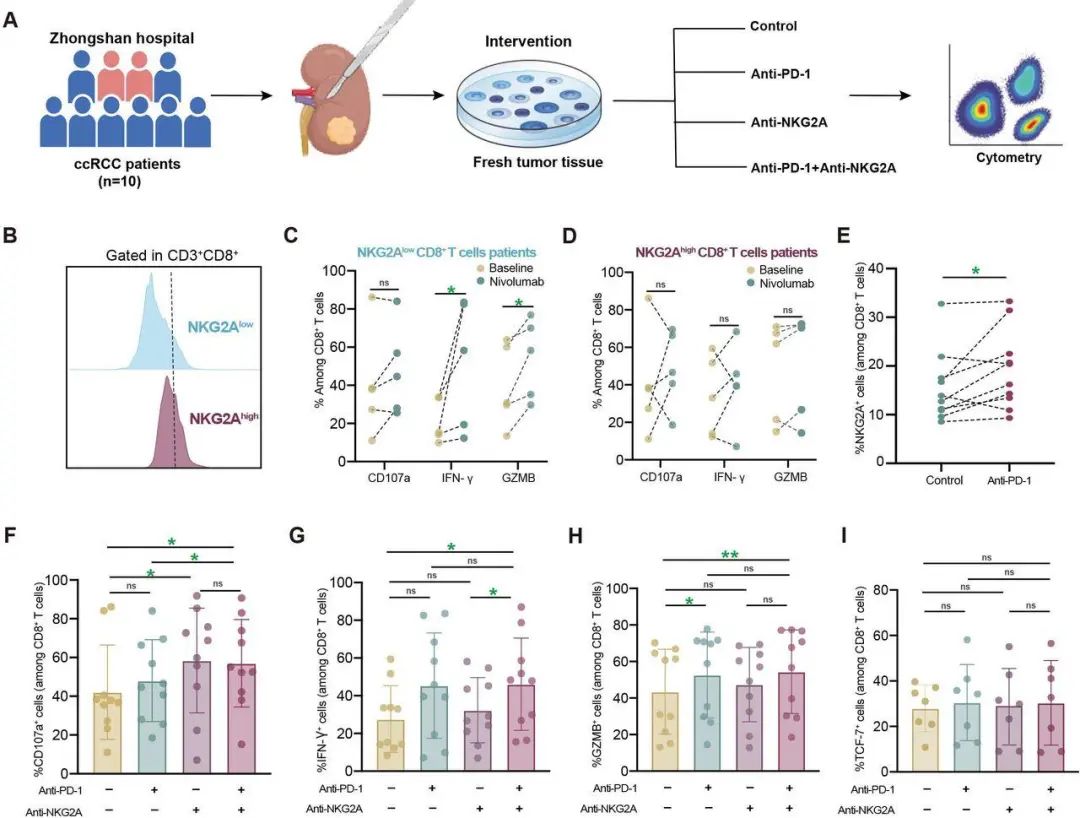
NKG2A 阻断与抗 PD-1 疗法协同作用,重振 CD8 T 细胞的细胞毒性
随后,我们对不同干预方案下CD8 T细胞内的动态功能改变进行了全面评估。值得注意的是,接受抗NKG2A治疗以及NKG2A和PD-1联合抑制组均表现出CD8 T细胞脱颗粒功能(CD107a)的显著增强(图5F;p=0.047和p=0.013),而接受纳武利尤单抗治疗的组未能表现出这种改善(图5F;p=0.241)。抗NKG2A和抗PD-1治疗的组合增强了CD8 T细胞的细胞毒性,仅在组合治疗组中观察到IFN-γ分泌显著增加(图5G;p=0.017),并且优于抗NKG2A单药治疗组(图5G;p=0.011)。此外,值得注意的是,组合疗法可以显著提高CD8 T细胞内GZMB的表达(图5H;p = 0.007)。但TCF-7的表达没有差异(图 5I)。总体而言,这些发现表明,抗 PD-1 和抗 NKG2A 的联合治疗可增强 CD8 T 细胞效应功能,这可能使抗 PD-1/PD-L1 免疫治疗耐药的患者受益。
研究结论
03
本研究表明,在ccRCC中,NKG2ACD8 T细胞与不良预后和对免疫治疗的反应有关。NKG2ACD8 T 细胞表现出耗竭的表型,并且与炎症但免疫抑制的微环境有关,并伴有富集的调节性 CD4 T 细胞 (Tregs) 浸润。NKG2A 阻断和当前免疫疗法的协同相互作用表现出重新激活 ccRCC 中 CD8 T 细胞效应功能的强大能力。总之,抗程序性细胞死亡蛋白-1(PD-1)和抗NKG2A的联合治疗可增强CD8 T细胞效应功能,这可能成为克服ccRCC当前免疫治疗耐药性的有效方法。(转化医学网360zhyx.com)
参考资料:
https://jitc.bmj.com/content/12/1/e008368
注:本文旨在介绍医学研究进展,不能作为治疗方案参考。如需获得健康指导,请至正规医院就诊。
 腾讯登录
腾讯登录









还没有人评论,赶快抢个沙发