【Nature子刊】华西医院杨胜勇团队开发深度学习分子生成模型,发现选择性RIPK1小分子抑制剂
| 导读 | 近日,四川大学华西医院生物治疗国家重点实验室杨胜勇教授团队发表最新研究成果。该研究报告了基于深度学习的分子生成模型发现RIPK1小分子抑制剂的研究过程;显示了生成式深度学习(GDL)模型生成全新分子结构的能力,表明深度学习在药物发现领域具有巨大潜力。 |
发现全新骨架结构活性化合物面临的挑战
01
开发新药是一个昂贵且耗时的过程,可能需要超过10亿美元和10年的时间。在药物研发初期,尤其是对于创新药物研发而言,高效地发现具有新型骨架结构的苗头化合物或先导化合物是至关重要的一步。传统的策略是利用高通量筛选方法从现有化合物库中进行筛选;然而,因为现有化合物库的结构多样性有限,以及各大制药公司和药物研发机构已对化合物库进行了反复筛选,可能无法找到具有不同支架的其他活性化合物,发现具有自主知识产权的全新骨架结构活性化合物已变得越来越具有挑战性。
目前,人们已提出通过从头分子设计(De novo molecular design)——通过计算生成具有所需性质的新分子——来解决上述问题。然而,传统的从头分子设计方法(包括基于结构的分子设计方法、基于配体和基于药效团模型的方法)涉及一个相对手动的过程,这需要经验丰富的设计师和明确的设计规则。此外,由于头分子设计方法主要是基于片段,因此其生成的分子的质量和多样性在很大程度上取决于片段库和用于片段组装的算法。
近年来,基于深度学习的生成模型或生成式深度学习(generative deep learning, GDL)模型的研究获得了快速发展。其中,基于循环神经网络(recurrent neural network, RNN)的GDL模型研究报道最为广泛;而条件循环神经网络(conditional RNN, cRNN)通过给定RNN初始状态向量作为条件,可显式指导后续分子生成过程。
然而,现有cRNN以及其他GDL模型仍然存在诸多缺陷——例如过度依赖目标函数,生成分子新颖性、多样性有限等。此外,尽管大多数GDL模型已在理论层面得到验证,但应用于实际创新药物发现并获得成功的例子依然较少。
新型cRNN分子生成模型
发现选择性RIPK1小分子抑制剂
02
为了解决上述问题,华西医院生物治疗研究中心杨胜勇教授团队提出了一种新型cRNN分子生成模型——该模型整合了迁移学习(transfer learning)、正则化增强(regularization enhancement)和采样增强(sampling enhancement)等策略。研究团队应用该策略成功发现了RIPK1激酶抑制剂。

https://www.nature.com/articles/s41467-022-34692-w
RIPK1是一种丝氨酸/苏氨酸蛋白激酶,参与了细胞存活的各种信号通路。值得注意的是,RIPK1还是程序性细胞坏死(坏死性凋亡)的关键调节因子,因此与各种炎症和免疫疾病的发生和发展密切相关。
当坏死性凋亡被诸如肿瘤坏死因子家族等刺激触发时,RIPK1将首先被激活。激活的RIPK1与其下游蛋白RIPK3结合并磷酸化,后者随后募集并磷酸化假激酶混合谱系激酶结构域(MLKL)磷酸化的MLKL形成低聚物并转移到细胞膜上以执行坏死性凋亡。基于上述RIPK1在坏死性凋亡中的核心作用,它被认为是治疗坏死性凋亡相关疾病的有希望的靶点。
通过建立定制化的RIPK1抑制剂虚拟化合物库、虚拟筛选、化学合成和生物活性验证,研究人员在未经任何改构的情况下,获得了一个高活性和选择性的RIPK1抑制剂(RI-962)。随后,研究人员解析了RIPK1–RI-962的晶体结构,从结构上阐明了RI-962具有高活性和选择性的分子机制。此外,团队还在TNFα诱导的全身炎症反应综合征(systemic inflammatory response syndrome, SIRS)和DSS诱导的炎症性肠病(inflammatory bowel disease, IBD)的小鼠模型上评价了RI-962的体内效果;其结果显示:RI-962通过抑制RIPK1激酶活性进而改善了TNFα诱导SIRS和DSS诱导的IBD损伤。
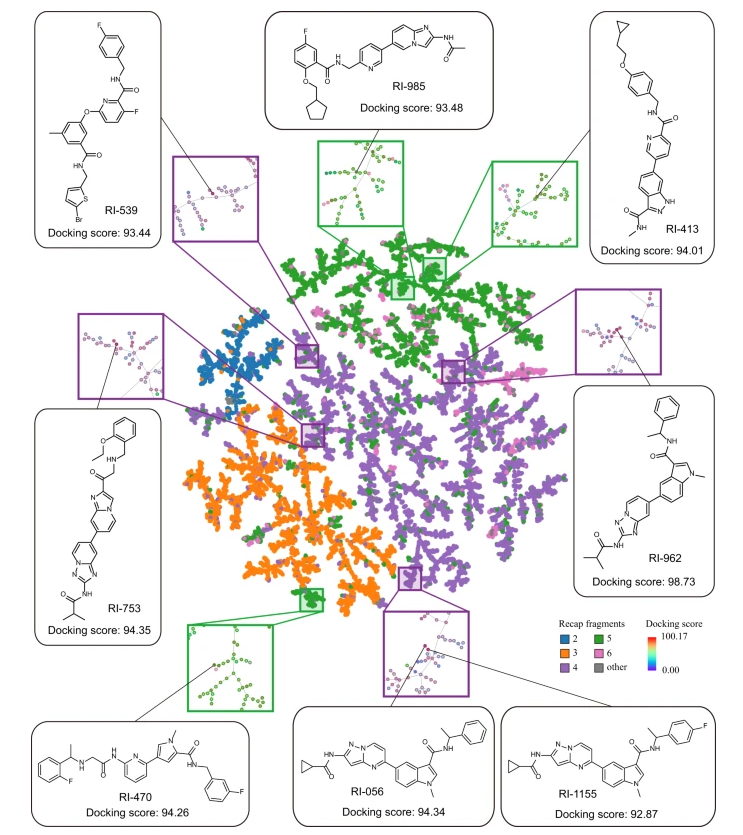
所选分子的位置,以便在过滤分子的TMAP中进行进一步的实验验证:
中心:由RECAP片段数量着色的TMAP概述。
周围框:其相应字段的放大版本,其中分子由对接分数(红-黄-绿)着色。
具有对接分数的分子:选定的分子指向它们在TMAP中的位置。
研究意义
03
杨胜勇教授团队开发的新型条件循环神经网络(cRNN)分子生成模型已成功应用于建立针对RIPK1的虚拟化合物库。与已知的RIPK1抑制剂相比,生成的文库富含更多的新支架分子。通过针对已建立的化合物库的标准药物筛选过程,研究团队检索到了一种有效的选择性RIPK1抑制剂,该抑制剂具有以前未报道的支架。
一方面,该应用实例验证了该生成式深度学习(GDL)模型的有效性。尽管RIPK1是一种激酶,但此GDL模型可以应用于不同类型的生物靶标——唯一的要求是生物靶标必须具有足够数量的已知活性化合物(靶标数据)。已知活性化合物的数量越多,GDL模型的性能就越好。
另一方面,该应用示例导致鉴定出具有先前未报道的支架的有效RIPK1抑制剂(RI-962)。值得注意的是,RI-962对其他407激酶表现出高选择性。它还在体外和体内显示出有效的活性。即便如此,该化合物仍然具有一些不利的性质,需要在未来进一步优化。(转化医学网360zhyx.com)
参考资料:
https://www.nature.com/articles/s41467-022-34692-w
http://www.wchscu.cn/academic/70225.html
注:本文旨在介绍医学研究进展,不能作为治疗方案参考。如需获得健康指导,请至正规医院就诊。
 腾讯登录
腾讯登录









还没有人评论,赶快抢个沙发