颠覆认知!《Cell》最新研究揭示肠道致病菌的全新生存策略:主动改造肠道环境,为自己创造巨大的生长优势
| 导读 | 这项发现为理解肠道病原体定植机制和开发针对炎症性肠病乃至结直肠癌的新疗法开辟了全新路径。 |
长期以来,脆弱拟杆菌(Bacteroides fragilis)被教科书归类为典型的“专性厌氧菌”,即只能在无氧环境中生存。然而,一项发表于国际顶级期刊《Cell》的最新研究彻底颠覆了这一传统认知。研究揭示,一种与结肠炎和结直肠癌密切相关的致病亚型——产肠毒素脆弱拟杆菌(ETBF),不仅能耐受氧气,更会主动改造肠道环境,将其变成一个富含氧气和乳酸的“氧化型生态位”,从而为自己创造巨大的生长优势。这项发现为理解肠道病原体定植机制和开发针对炎症性肠病乃至结直肠癌的新疗法开辟了全新路径。
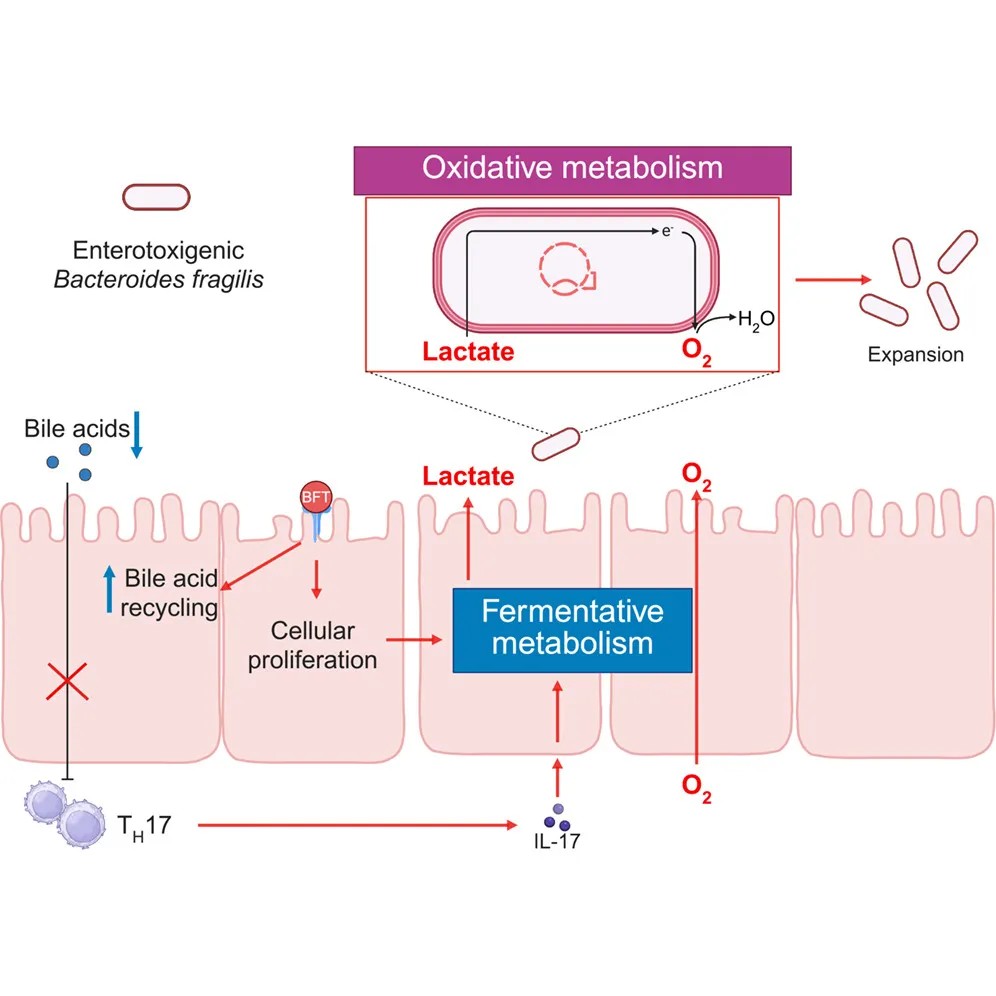
图形摘要
角色转变:一个生存策略的逆转
在健康的肠道中,结肠上皮细胞(结肠细胞)通过氧化磷酸化高效产能,这个过程会消耗掉组织中的氧气,从而在肠腔维持一个严密的厌氧环境,以供以发酵为生的厌氧共生菌生长。产肠毒素脆弱拟杆菌(ETBF)产生的脆弱拟杆菌毒素( BFT)是其主要武器。
研究团队发现,BFT如同一把“代谢扳手”,直接作用于宿主。它通过切割上皮细胞间的连接蛋白E-钙粘蛋白,并异常激活Wnt/β-连环蛋白信号通路,导致上皮细胞过度增生。新生的、未分化的上皮细胞更倾向于进行效率较低的“糖酵解”而非氧化磷酸化。
双重驱动:打造病原体的理想家园
这一代谢模式的转变产生了两个关键后果:第一,糖酵解产生大量乳酸并分泌到肠腔;第二,上皮细胞耗氧减少,使得氧气从肠道组织扩散到肠腔。于是,一个富含乳酸和氧气 的局部微环境便形成了。
令人惊讶的是,研究团队通过先进的靶向转录组测序技术发现,在这种发炎的肠道中,ETBF自身开启了氧化代谢程序。它高表达三羧酸循环(TCA)关键酶、乳酸脱氢酶和细胞色素氧化酶,表明其能够利用乳酸和氧气进行高效的呼吸代谢,产生更多能量。这完全颠覆了其作为“专性厌氧菌”的经典定义。
更巧妙的是,ETBF的改造远不止于上皮细胞。研究首次揭示,BFT还能“劫持”宿主的胆汁酸循环通路。它上调肠道胆汁酸转运蛋白的表达,加速了胆汁酸从肠腔被回收入血。
临床转化:多环节干预展现出治疗潜力
基于这一全新机制,研究团队在动物模型中测试了多种干预策略,均取得了显著效果:
-
恢复宿主正常代谢:补充短链脂肪酸丁酸的前体“丁酸甘油酯”,可以促进上皮细胞恢复氧化磷酸化,减少肠腔氧气和乳酸,从而显著降低ETBF的定植负荷和肠道炎症。
-
补充保护性胆汁酸:直接补充被ETBF消耗的次级胆汁酸,可以有效抑制IL-17的产生,减轻炎症并抑制ETBF。
-
抑制胆汁酸过度回收:使用胆汁酸转运蛋白抑制剂,可以阻断BFT对胆汁酸循环的干扰,恢复肠道胆汁酸水平,从而缓解疾病。
-
靶向炎症信号:直接中和IL-17或抑制Wnt/β-连环蛋白信号通路,也能打断上述恶性循环,抑制ETBF。
研究还发现ETBF依赖的这种有氧呼吸代谢,是其驱动结直肠肿瘤发生的关键。在易感小鼠模型中,敲除ETBF的呼吸链关键基因,或通过丁酸甘油酯恢复上皮缺氧,都能显著减少结肠肿瘤的发生。
研究意义与未来展望
这项研究不仅揭示了一种经典厌氧病原体惊人的环境适应与改造能力,更建立了“肠道病原体-胆汁酸代谢-宿主免疫(IL-17)-上皮细胞代谢”之间的完整作用轴。它阐明了ETBF促进结肠炎症乃至癌变的精密机制,并为治疗ETBF相关疾病提供了多个极具潜力的精准干预靶点。(转化医学网360zhyx.com)
原文链接:
https://www.cell.com/cell/fulltext/S0092-8674(26)00401-0
|
免费论坛
|
创新多组学队列研究学术论坛 |
|
干细胞前沿创新与临床转化研讨会 |
|
|
第八届上海国际癌症大会 |
|
|
第二届西部单细胞与空间组学论坛 |
【关于投稿】
转化医学网(360zhyx.com)是转化医学核心门户,旨在推动基础研究、临床诊疗和产业的发展,核心内容涵盖组学、检验、免疫、肿瘤、心血管、糖尿病等。如您有最新的研究内容发表,欢迎联系我们进行免费报道(公众号菜单栏-在线客服联系),我们的理念:内容创造价值,转化铸就未来!
转化医学网(360zhyx.com)发布的文章旨在介绍前沿医学研究进展,不能作为治疗方案使用;如需获得健康指导,请至正规医院就诊。
责任声明:本稿件如有错误之处,敬请联系转化医学网客服进行修改事宜!
微信号:zhuanhuayixue
 腾讯登录
腾讯登录









还没有人评论,赶快抢个沙发