克服免疫治疗局限!香港中文大学发文:有前景的癌症治疗策略
| 导读 | 这种增强活性氧的纳米平台为克服当前癌症免疫疗法的局限性提供了一种有前景的策略,它能够同时诱导有效的化学动力学治疗(CDT)并重新编程肿瘤免疫微环境。 |
4月27日,香港中文大学研究团队在期刊《Advanced Science》上发表了研究论文,题为“ROS Self-Supply Nanoplatform Based on Fenton Catalyst for Chemodynamic and Immunotherapy: Reprogramming Cold Tumor Into Hot Tumor in Cancer Treatment”,本研究中,研究人员开发了一种活性氧(ROS)自供纳米平台(HA-PGMC),通过在金属有机框架(MOF)材料 MIL-100 内原位生长过氧化铜(CuO₂)纳米点并负载葡萄糖氧化酶(GOx)实现。HA-PGMC 利用释放的 Fe²⁺ 和 Cu⁺ 离子之间的催化级联反应,在酸性和葡萄糖丰富的肿瘤条件下生成大量羟基自由基(•OH),从而放大氧化应激。同时,Cu²⁺ 离子消耗谷胱甘肽(GSH),进一步促进 ROS 积累。体外研究表明,HA-PGMC 能够显著诱导 ROS 生成、GSH 消耗、脂质过氧化、线粒体功能障碍,并产生强大的抗肿瘤效果,同时对正常细胞的毒性极小。重要的是,HA-PGMC 通过促进钙网蛋白(CRT)暴露和高迁移率族蛋白 B1(HMGB1)释放,触发免疫原性细胞死亡(ICD),有效地将“冷”肿瘤转化为“热”肿瘤。这种增强的免疫激活为与免疫检查点阻断疗法的协同作用铺平了道路。总体而言,这种增强活性氧的纳米平台为克服当前癌症免疫疗法的局限性提供了一种有前景的策略,它能够同时诱导有效的化学动力学治疗(CDT)并重新编程肿瘤免疫微环境。
免疫疗法治癌:进展、局限与“冷热”挑战
01
免疫疗法为癌症治疗带来了革命性的治疗益处,为癌症患者创造了机会。通过使用诸如αPD-L1 这样的免疫检查点药物,肿瘤细胞的免疫检查点 PD-1 被阻断,恢复了肿瘤浸润淋巴细胞(TILs)的抗肿瘤功能,同时由于αPD-L1 受体在肿瘤中特异性高表达,副作用得以最小化。然而,临床研究中的应答率仍不尽人意,不同癌症类型的平均客观缓解率(ORR)仅为 19.56%。因此,提高免疫疗法的疗效已成为治疗癌症的一个有前景但具有挑战性的任务。导致临床反应不佳的主要因素是肿瘤缺乏 T 细胞浸润,表现为“冷肿瘤”——也称为免疫排斥肿瘤和免疫荒漠肿瘤——其中 CD8+T 淋巴细胞仅定位于侵袭边缘或完全不在肿瘤及其周围区域。因此,在应用免疫检查点抑制剂(ICIs)之前增加 T 细胞浸润对于将“冷肿瘤”转变为“热肿瘤”至关重要。
HA-PGMC的体外抗肿瘤功效
02
鉴于对(HA-PGMC)的良好表征,研究人员接下来评估了其体外抗肿瘤活性。首先,通过共聚焦激光扫描显微镜(CLSM)评估 4T1 细胞对 HA-PGMC 的细胞摄取情况,以验证透明质酸对 PGMC 的靶向作用。随后,研究人员通过活/死细胞染色、MTT 检测和细胞凋亡分析评估了 4T1 细胞的抗肿瘤活性。研究人员还检测了对正常 L929 成纤维细胞的细胞毒性。HA-PGMC 对正常细胞的毒性低于对肿瘤细胞的毒性,在 L929 细胞中保持约 60%的活力,表明其具有肿瘤选择性。此外,研究人员还对细胞凋亡进行了定量分析,以进一步验证治疗效果。
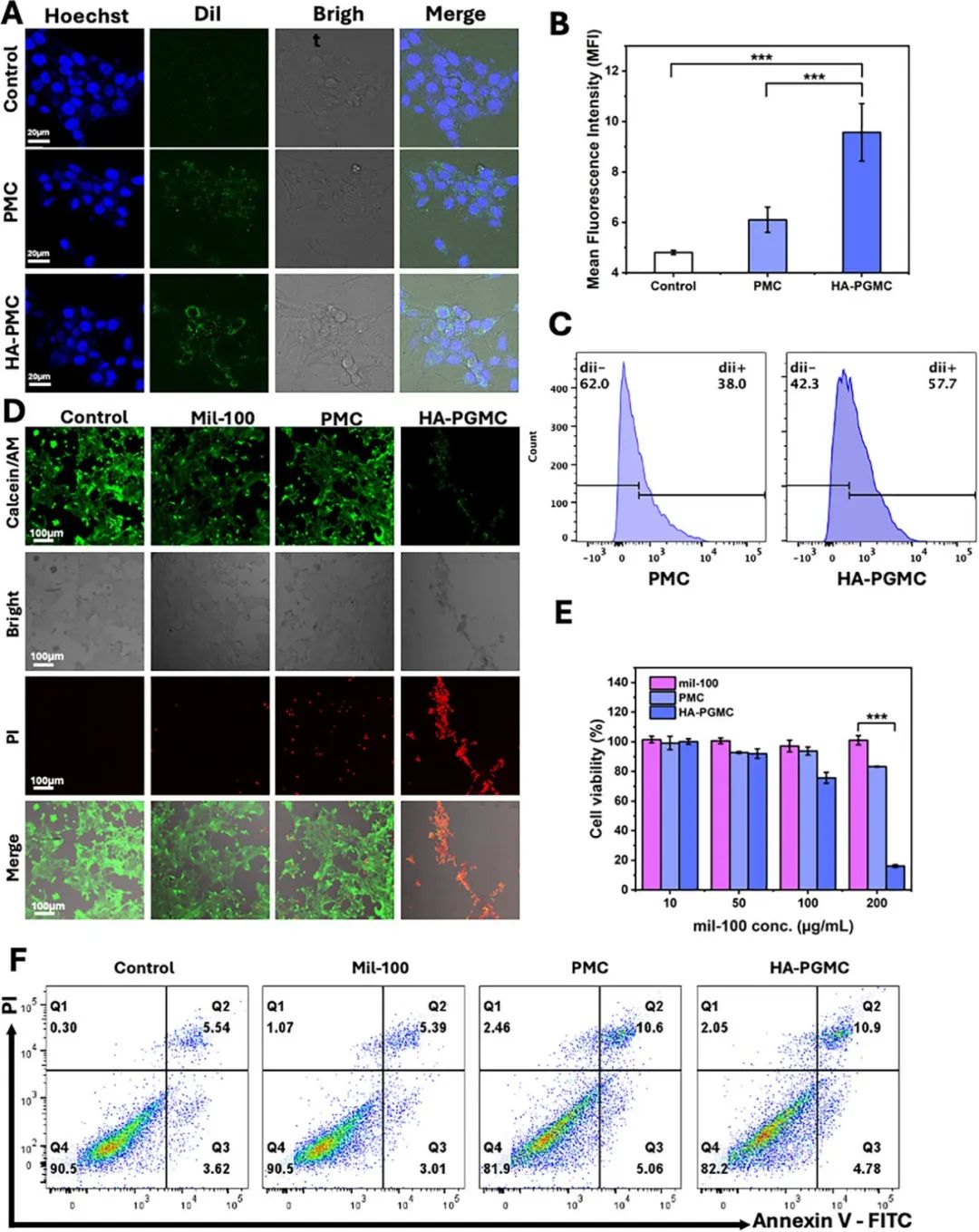
HA-PGMC在体外的抗肿瘤功效
总之,HA-PGMC 展示出卓越的肿瘤靶向能力和强大的抗肿瘤效果,对肿瘤细胞具有高度特异性,对正常细胞的毒性极小,凸显了其在选择性癌症治疗中的巨大潜力。(转化医学网360zhyx.com)
参考资料:
https://advanced.onlinelibrary.wiley.com/doi/10.1002/advs.202523039
|
免费论坛
|
|
【关于投稿】
转化医学网(360zhyx.com)是转化医学核心门户,旨在推动基础研究、临床诊疗和产业的发展,核心内容涵盖组学、检验、免疫、肿瘤、心血管、糖尿病等。如您有最新的研究内容发表,欢迎联系我们进行免费报道(公众号菜单栏-在线客服联系),我们的理念:内容创造价值,转化铸就未来!
转化医学网(360zhyx.com)发布的文章旨在介绍前沿医学研究进展,不能作为治疗方案使用;如需获得健康指导,请至正规医院就诊。
责任声明:本稿件如有错误之处,敬请联系转化医学网客服进行修改事宜!
微信号:zhuanhuayixue
 腾讯登录
腾讯登录









还没有人评论,赶快抢个沙发