Cell重磅发布!一种新型CAR-T疗法在多种实体瘤中展现出强大的抗肿瘤活性
| 导读 | 该研究为克服CAR-T细胞治疗实体瘤的长期瓶颈提供了全新策略。 |
近日,国际顶尖期刊《Cell》发表一项重磅研究:一种名为尿激酶型纤溶酶原激活物受体(uPAR)的蛋白,是攻击多种实体瘤及其赖以生存的“保护罩”的关键靶点。基于此研发的uPAR CAR-T细胞疗法,在临床前研究中展现出强大的抗肿瘤活性,并能有效清除转移病灶,且未引发持久的骨髓抑制等严重毒性,该研究为克服CAR-T细胞治疗实体瘤的长期瓶颈提供了全新策略。
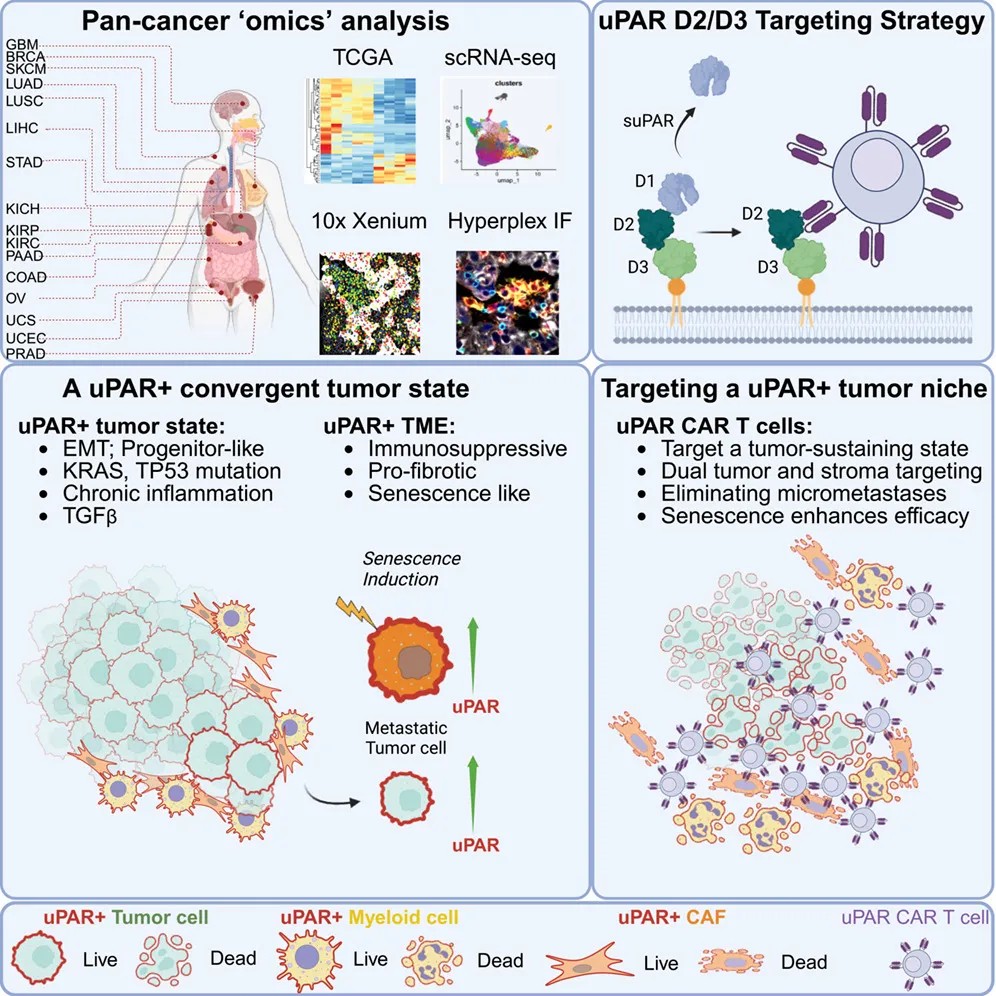
图形摘要
发现共性靶点:uPAR标记恶性“生态系统”
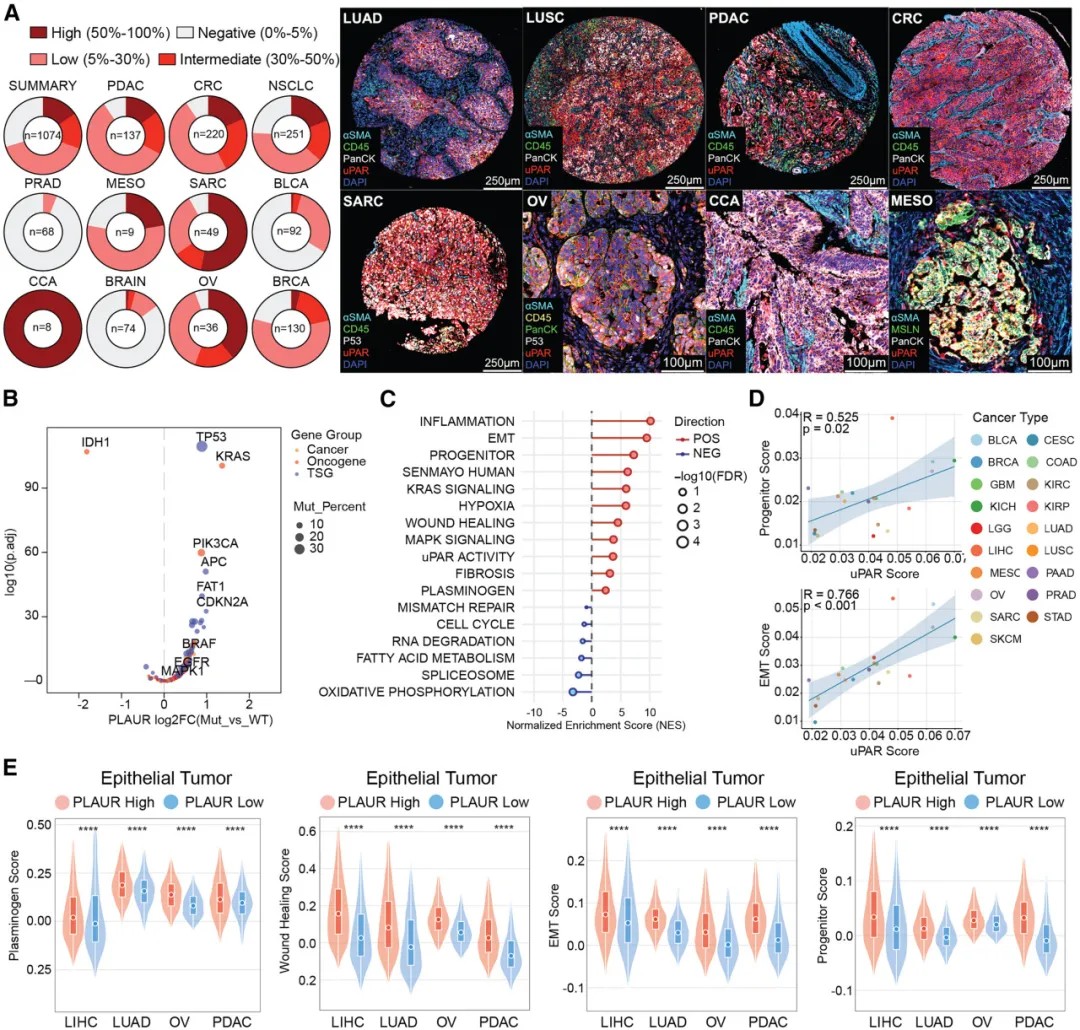
uPAR标记一种富含TP53突变和EMT程序的独特细胞状态
研究团队通过整合分析超过1万个肿瘤样本的数据发现,uPAR在多种携带TP53和RAS通路突变的实体瘤中广泛高表达,尤其是在卵巢癌、胰腺癌、结直肠癌、肺癌和脑癌的特定亚型中。
更关键的是,uPAR不仅高表达于肿瘤细胞本身,还高表达于肿瘤内部具有衰老特征的癌相关成纤维细胞和髓系免疫抑制细胞。空间转录组学和多重免疫荧光分析揭示,这些uPAR阳性的肿瘤细胞、基质细胞和免疫细胞在空间上紧密聚集,形成了一个结构保守的促纤维化、免疫抑制性“生态位”。这个生态位如同肿瘤的“保护罩”,将效应T细胞排斥在外,是导致治疗抵抗的重要原因。
uPAR定义的不是某个特定的细胞谱系,而是一种具有攻击性的、由肿瘤细胞及其支持性微环境共同构成的恶性细胞状态,这使其与CD19等传统靶点有着本质不同。
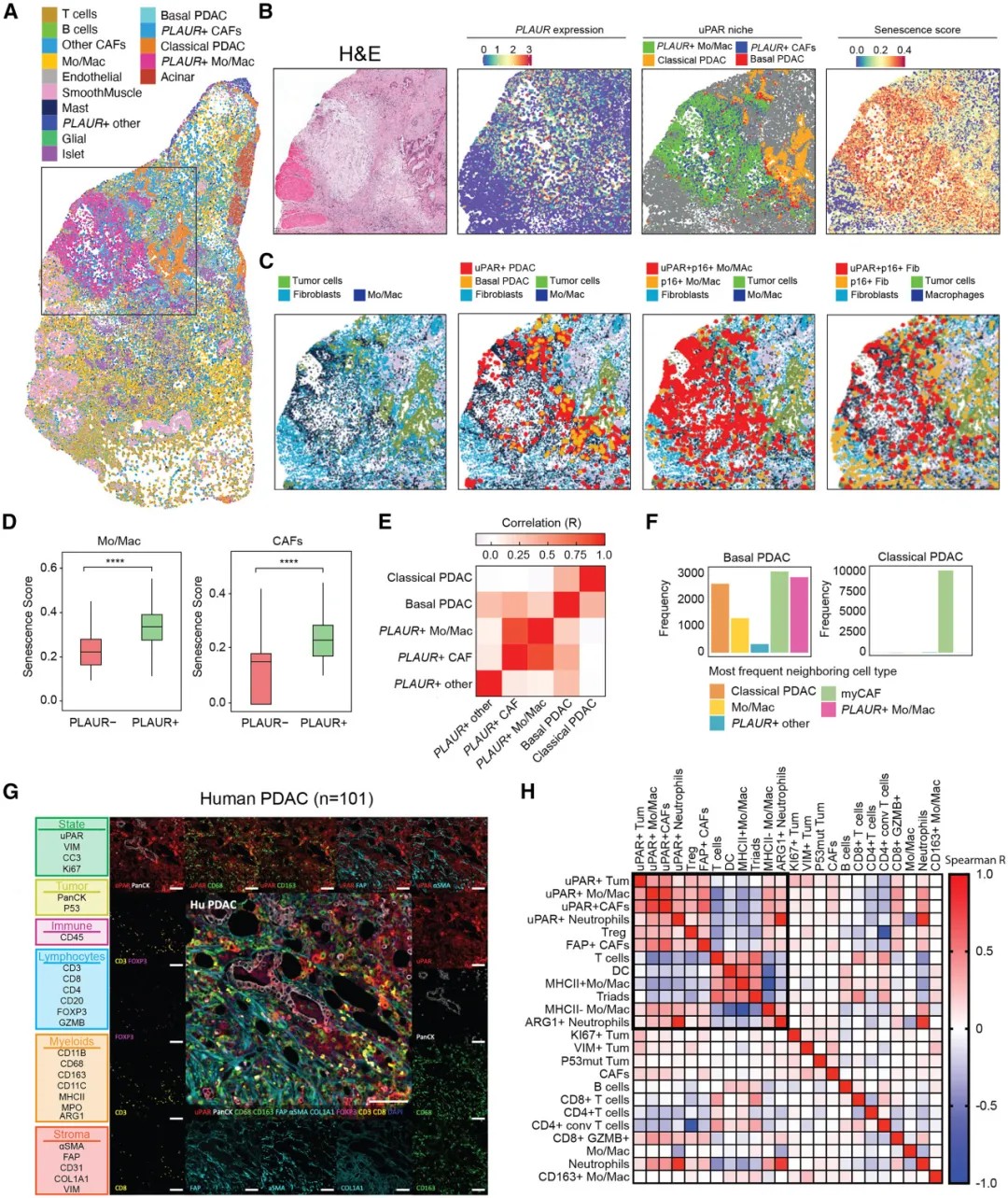
uPAR阳性肿瘤细胞、CAF与髓系细胞构成一个纤维化、免疫抑制性生态位
一箭双雕:uPAR CAR-T细胞同时清除肿瘤与基质
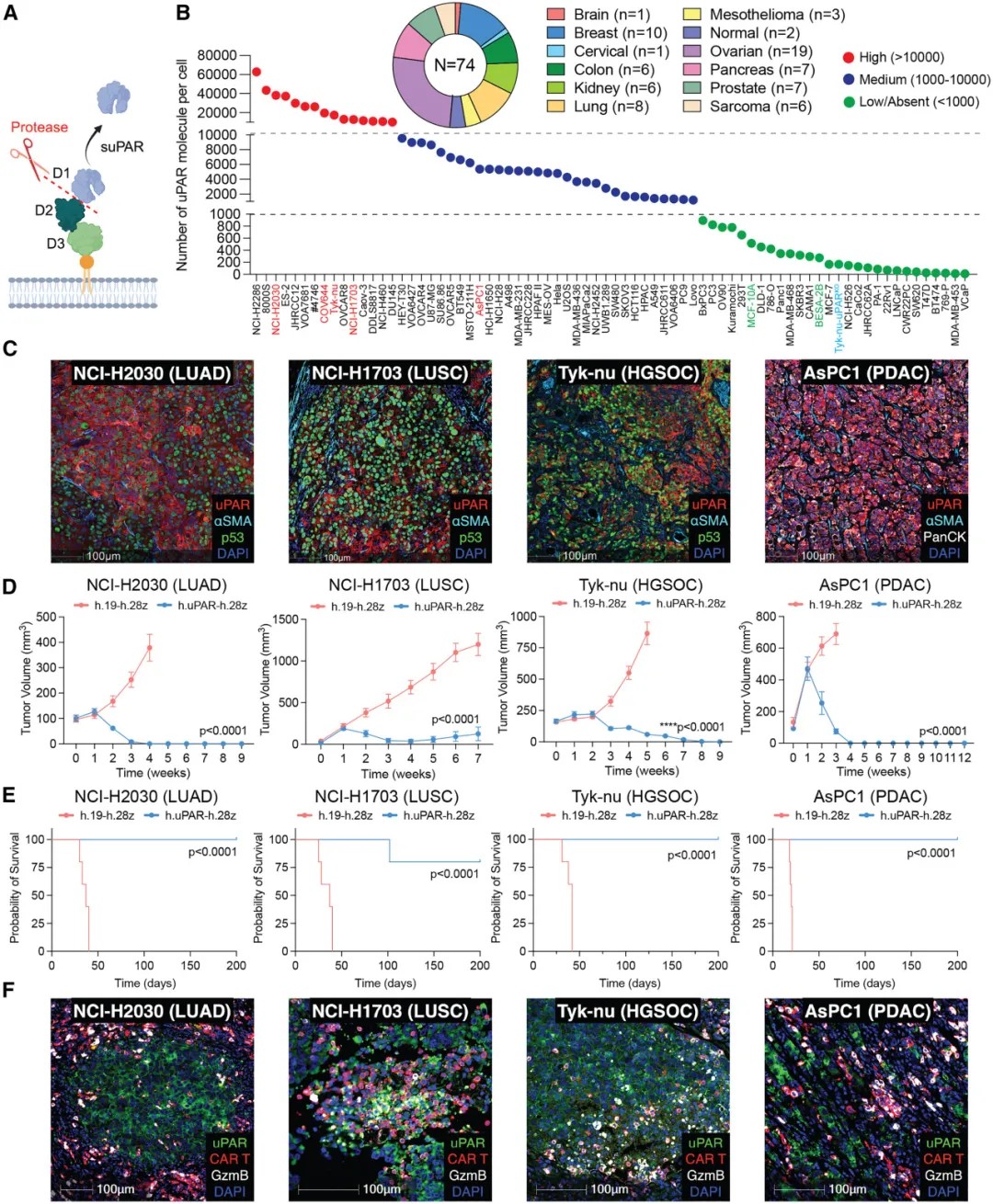
uPAR CAR-T细胞在多种癌症模型中展现出强大的抗肿瘤活性
基于这一发现,研究团队开发了靶向uPAR蛋白D2-D3结构域的人源化CAR-T细胞。体外实验证实,这些CAR-T细胞能有效识别并杀伤表面uPAR分子数超过1500个的肿瘤细胞。
在多种小鼠模型中,uPAR CAR-T疗法显示出卓越疗效。在肺癌、胰腺癌、卵巢癌的细胞系及患者来源的异种移植瘤模型中,单次输注uPAR CAR-T细胞可诱导肿瘤快速、持久消退,并显著延长小鼠生存期。尤为重要的是,在高致死性的高级别浆液性卵巢癌模型中,该疗法不仅能根除原位肿瘤,还能有效清除已广泛播散的腹腔转移灶,并在模拟临床辅助治疗场景中清除残余病灶,防止复发。
研究通过使用物种特异性的scFv抗体片段进一步证明,uPAR CAR-T细胞能够同时靶向并清除肿瘤细胞(人源uPAR)和肿瘤内的促纤维化基质细胞(鼠源uPAR)。这种“双重打击”策略比单独靶向肿瘤细胞产生了更优且更持久的肿瘤控制效果,并显著减少了多个器官转移灶中的纤维化程度。体外与人源肿瘤组织的共培养实验也证实,uPAR CAR-T细胞能直接杀伤患者肿瘤中的uPAR阳性癌细胞、癌相关成纤维细胞和髓系抑制性细胞。
安全性良好:并可与现有疗法协同增效
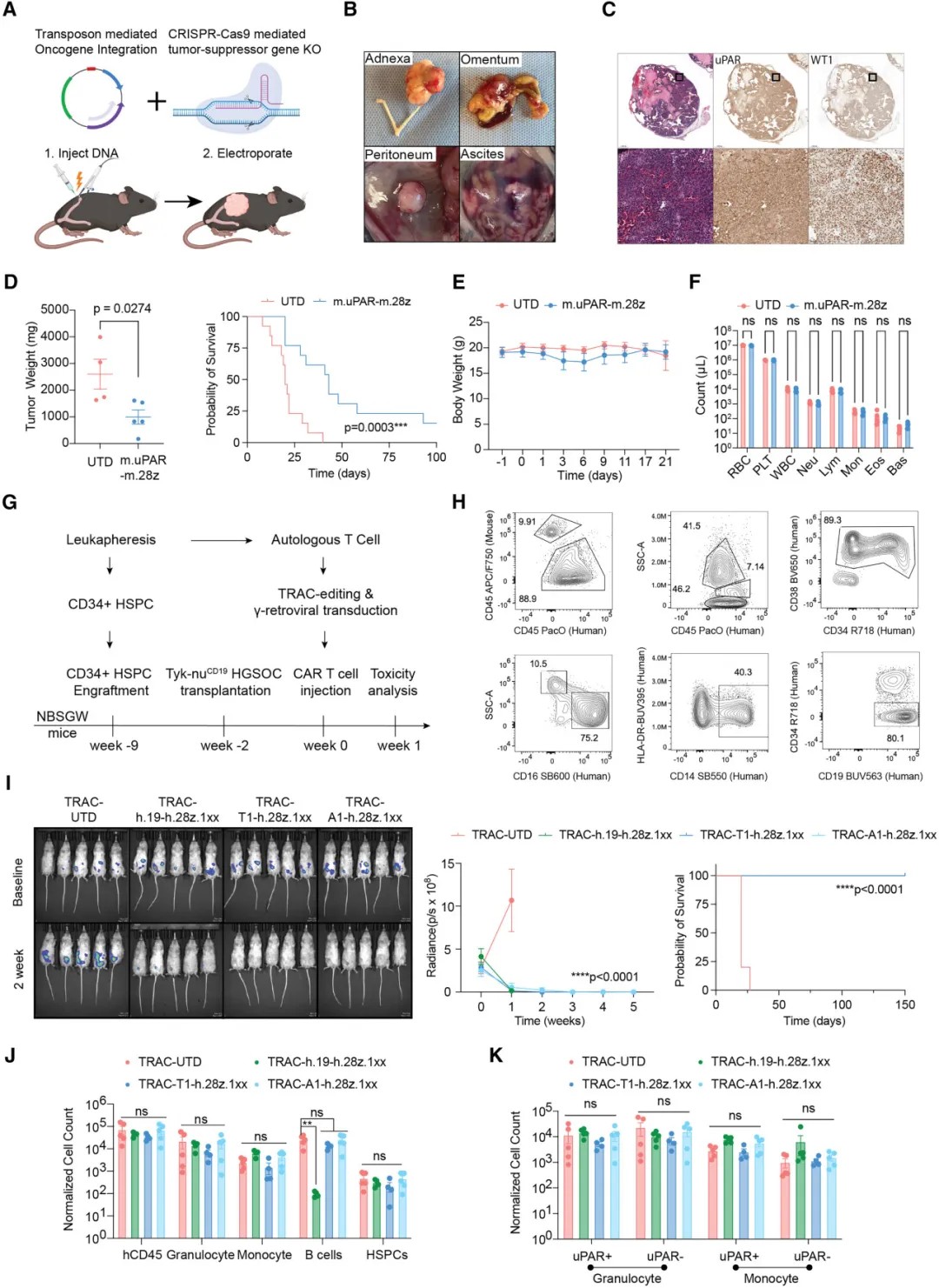
uPAR CAR-T细胞展现出良好的安全性特征
安全性是CAR-T疗法临床转化的关键。分析显示,uPAR在正常成人重要器官中的表达水平显著低于PSMA、TROP2等已获批药物靶点,其表达主要局限于部分髓系细胞。在具有人源化免疫系统的小鼠模型中,uPAR CAR-T细胞在有效清除肿瘤的同时,并未对单核细胞、粒细胞等髓系细胞区室产生持续耗竭,显示出良好的治疗窗口。
此外,研究还发现了一个潜在的联合治疗策略。许多化疗、放疗或靶向药物在杀伤肿瘤的同时,会诱导存活的肿瘤细胞进入一种“衰老样”状态,而这种状态会上调uPAR的表达。在卵巢癌和肺癌的小鼠模型中,先使用顺铂等诱导衰老的化疗药物预处理,可显著增加肿瘤细胞的uPAR抗原密度,从而大幅增强后续uPAR CAR-T细胞的疗效,实现“1+1>2”的协同抗肿瘤效果,且不增加额外毒性。
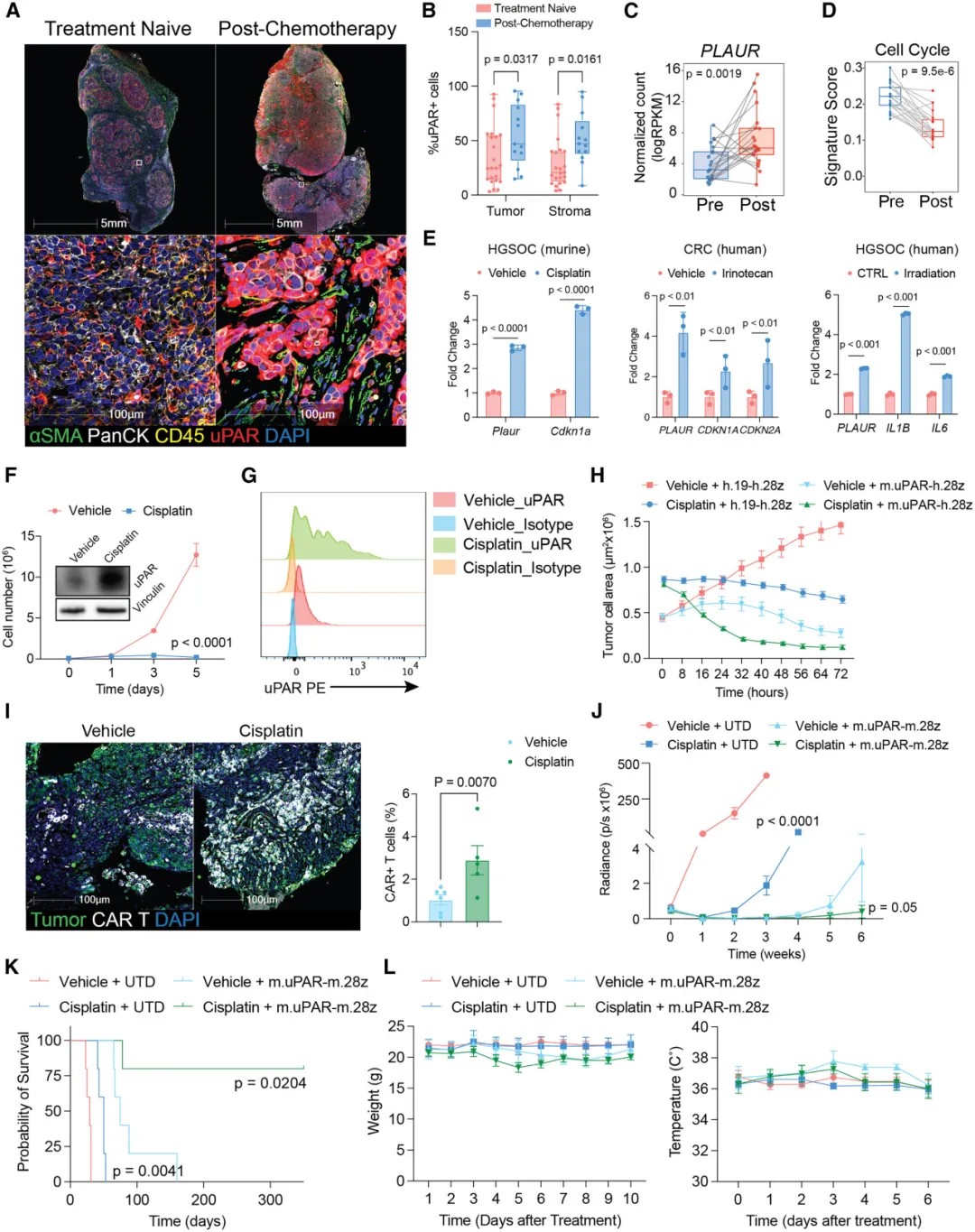
治疗诱导的衰老增强CAR-T细胞疗效
研究意义与未来展望
该研究确立了uPAR作为一个具有广阔应用前景的CAR-T靶点,它能够克服实体瘤治疗中的主要障碍,研究的目标不仅是杀死肿瘤细胞,更是要瓦解维持肿瘤生长的整个病理生态系统。这为实现下一代超越肿瘤类型的CAR-T疗法提供了框架。
原文链接:
https://www.cell.com/cell/fulltext/S0092-8674(26)00269-2(转化医学网360zhyx.com)
【关于投稿】
转化医学网(360zhyx.com)是转化医学核心门户,旨在推动基础研究、临床诊疗和产业的发展,核心内容涵盖组学、检验、免疫、肿瘤、心血管、糖尿病等。如您有最新的研究内容发表,欢迎联系我们进行免费报道(公众号菜单栏-在线客服联系),我们的理念:内容创造价值,转化铸就未来!
转化医学网(360zhyx.com)发布的文章旨在介绍前沿医学研究进展,不能作为治疗方案使用;如需获得健康指导,请至正规医院就诊。
责任声明:本稿件如有错误之处,敬请联系转化医学网客服进行修改事宜!
微信号:zhuanhuayixue
 腾讯登录
腾讯登录







还没有人评论,赶快抢个沙发