破解药物递送难题!中国科学技术大学王育才/朱书/蒋为团队Science发文揭示菌群驱动血清素信号调控肝脏清除的新机制
| 导读 | 它们通过一条此前未知的“肠道-肝脏”免疫轴,持续激活肝脏中的巨噬细胞,使其保持高度活跃的“清道夫”状态,从而大幅清除血液中的合成或病毒递送载体。 |
在生命科学与肿瘤治疗的前沿,如何将药物精准、高效地送达病灶,一直是药物递送的核心挑战。尽管脂质体、纳米颗粒等递送系统飞速发展,但人体肝脏强大的免疫清除功能,如同一个“黑洞”,吞噬了大部分治疗载体,导致疗效大打折扣。近日,中国科学技术大学王育才/朱书/蒋为团队一项发表于国际顶尖期刊《Science》的重磅研究,为破解这一难题提供了全新视角。研究发现:肠道内数以万亿计的共生微生物,竟是影响药物递送效率的“关键第三方”。它们通过一条此前未知的“肠道-肝脏”免疫轴,持续激活肝脏中的巨噬细胞,使其保持高度活跃的“清道夫”状态,从而大幅清除血液中的合成或病毒递送载体。
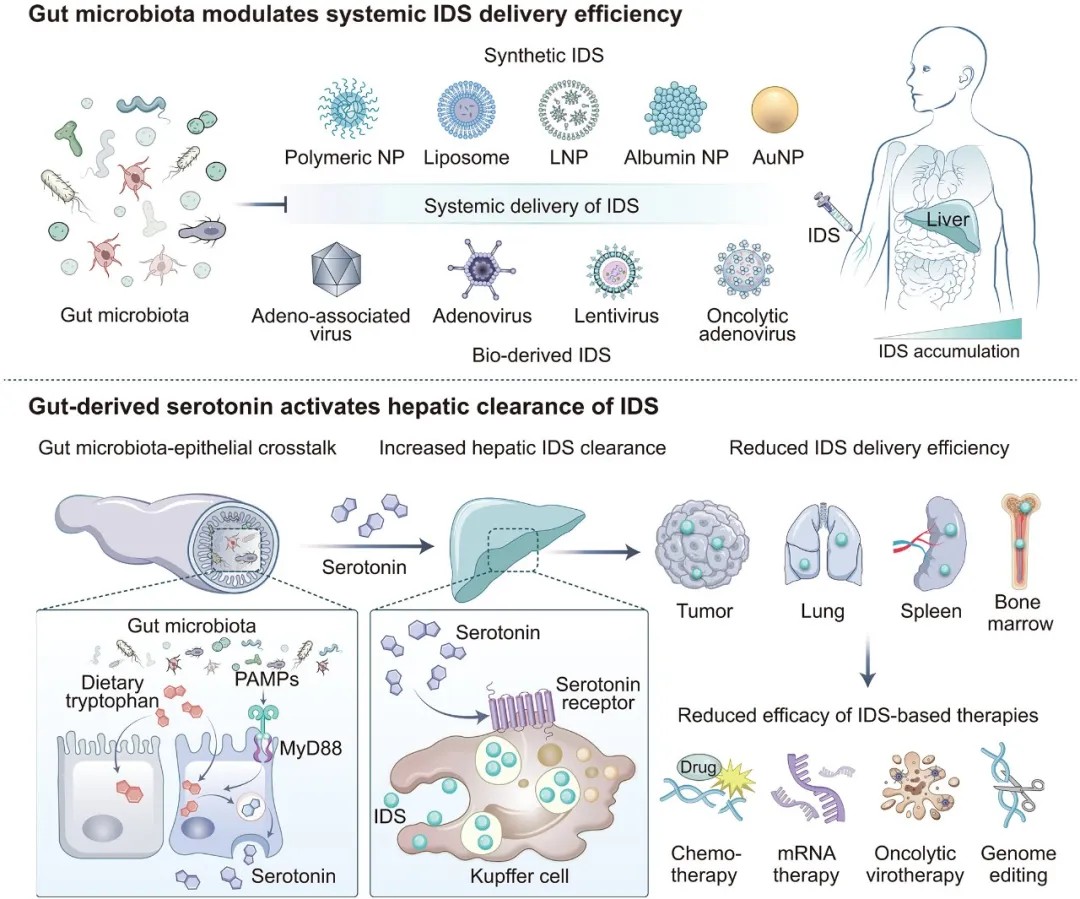
一条肠道-肝脏免疫轴限制了基于体内递送系统的疗法的效力
机制揭秘:细菌遥控,血清素传令
研究揭示了这一过程精细的分子机制。肠道中的革兰氏阴性菌并不直接作用于肝脏,而是刺激肠道上皮细胞。这些上皮细胞随后改变了色氨酸代谢途径,大量产生神经递质——血清素。血清素随血液循环到达肝脏,作为核心信使,与库普弗细胞表面的特定受体结合。
这一结合触发了库普弗细胞内部的骨架重组,并上调了与吞噬作用相关基因的表达,从而使其捕获和清除各种外来递送系统的能力普遍增强。这意味着,无论是用于化疗的纳米颗粒、用于基因编辑的病毒载体,还是用于mRNA疗法的脂质纳米粒,都会在抵达目标组织前,被这条由肠道菌群驱动的通路大量拦截。
干预策略:短暂阻断,效果显著
更具临床转化价值的是,研究团队发现,无需永久改变肠道菌群,仅需短暂干预血清素信号,即可显著提升递送效率。通过饮食控制(限制血清素合成前体的摄入)或使用药物短暂阻断相关的血清素受体,可以有效地让库普弗细胞“暂时休息”,为治疗载体打开通往靶组织的时间窗。
这种策略效果惊人。在动物模型中,它使基于化疗和溶瘤病毒疗法的抗肿瘤效果提升了三倍以上;更令人瞩目的是,对于体细胞基因编辑和mRNA疗法,其递送效率提升了5至15倍,极大增强了这些前沿疗法的潜力。
研究意义与未来展望
该研究首次将肠道微生物组与系统性的药物递送效率直接联系起来,指出了一条超越传统材料工程改良的新途径。通过调节内源性生物通路(色氨酸代谢-血清素信号轴)来改善递送系统性能,这一策略具有广谱适用性。
对于精准肿瘤诊疗、基因治疗、mRNA疫苗等众多领域,这一发现意味着可以通过简单的短期联合用药或饮食辅助方案,安全地降低肝脏清除率或肝毒性,从而大幅提升现有疗法的成功率与安全性,为攻克诸多疑难疾病带来了新的希望。
原文链接:
https://www.science.org/doi/10.1126/science.adu7686(转化医学网360zhyx.com)
【关于投稿】
转化医学网(360zhyx.com)是转化医学核心门户,旨在推动基础研究、临床诊疗和产业的发展,核心内容涵盖组学、检验、免疫、肿瘤、心血管、糖尿病等。如您有最新的研究内容发表,欢迎联系我们进行免费报道(公众号菜单栏-在线客服联系),我们的理念:内容创造价值,转化铸就未来!
转化医学网(360zhyx.com)发布的文章旨在介绍前沿医学研究进展,不能作为治疗方案使用;如需获得健康指导,请至正规医院就诊。
责任声明:本稿件如有错误之处,敬请联系转化医学网客服进行修改事宜!
微信号:zhuanhuayixue
 腾讯登录
腾讯登录







还没有人评论,赶快抢个沙发