Cell重磅发布!科学家发现癌症良恶性转变的关键窗口与拦截新策略
| 导读 | 更关键的是,研究揭示了短暂干预即可显著延迟癌症发生的治疗窗口,为癌症的早期拦截提供了全新策略。 |
癌症并非一蹴而就,在肿瘤最终形成并开始致命性扩散之前,会经历一个漫长而隐秘的演化过程。其中,从良性病变向恶性癌症的转变,是决定疾病走向的临界点,但这一关键步骤的具体机制一直成谜。近日,国际顶尖学术期刊《Cell》发表一项突破性研究首次在胰腺癌模型中以高时空分辨率“直播”了这一转变过程,并找到了一个驱动恶性进展的核心细胞状态及其所构建的、类似癌症的“生态位”。更关键的是,研究揭示了短暂干预即可显著延迟癌症发生的治疗窗口,为癌症的早期拦截提供了全新策略。
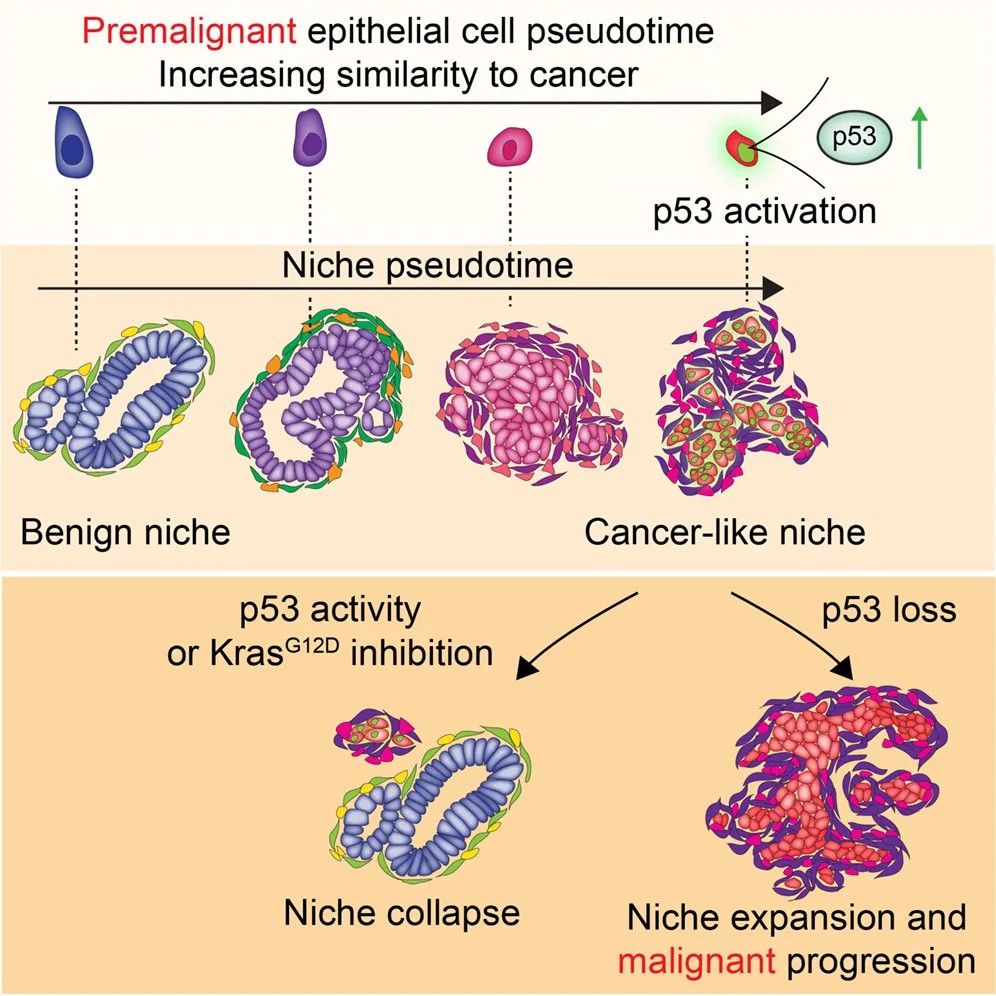
图形摘要
癌基因与抑癌基因的战场:聚焦于“祖细胞样”状态
胰腺导管腺癌是恶性程度最高的癌症之一,其发生通常始于KRAS基因突变,但仅有突变并不足以致癌,往往还需要TP53、CDKN2A等关键抑癌基因的后续失活。然而,这些遗传事件如何协同驱动细胞“越界”,一直不甚清楚。
研究团队利用能标记自发性p53丢失的小鼠模型,并结合单细胞与空间转录组学技术,精细描绘了胰腺癌从癌前到恶性的演化路径。
研究发现,在携带KRAS突变的癌前胰腺上皮细胞中,存在一个特殊的、数量稀少的细胞亚群。这些细胞呈现出“祖细胞样”状态,表达如Nes、Msn、Hmga2等标志物。令人惊讶的是,在这个亚群内部,促癌的KRAS信号通路与p53、CDKN2A、SMAD4三大关键抑癌通路被同时激活,并引发了类似细胞衰老的反应。
自我强化的“癌前生态位”:癌症微环境的提前预演
更深入的发现是,这些“祖细胞样”细胞并非孤立存在。研究人员通过创新的空间转录组学分析框架,发现这些细胞具有强大的细胞间通讯潜力,并能主动重塑其周围的微环境。随着“祖细胞样”特征增强,上皮细胞逐渐丧失原有的腺泡结构,获得间质特性,同时其周围会逐步聚集起特定的免疫细胞和活化的成纤维细胞,最终形成一个独特的、多细胞构成的“祖细胞生态位”。
这个在癌前阶段就出现的“生态位”,惊人地再现了晚期侵袭性胰腺癌典型的促纤维化、免疫抑制性肿瘤微环境的诸多特征。癌症并非在真空中发展,研究表明,在肿瘤实体形成之前,一个支持其生长和演化的“癌症样”生态系统就已经被这些先驱细胞搭建好了。这解释了为何许多胰腺癌在早期就表现出强烈的免疫逃逸和耐药性。
关键的干预窗口:靶向“祖细胞”状态可瓦解生态位、延迟癌变
研究最具有转化潜力的发现在于,这个“祖细胞样”状态及其生态位是“可靶向、可逆转”的脆弱环节。
一方面,研究显示,通过使用KRASG12D特异性抑制剂MRTX1133进行短暂处理,可以迅速清除这些依赖持续KRAS信号存活的“祖细胞样”细胞。令人瞩目的是,仅仅是早期、短期(48-72小时)的KRAS抑制,就足以导致整个“祖细胞生态位”的瓦解——支持性的免疫细胞和成纤维细胞也随之消失。更重要的是,在癌前小鼠模型中,这样一次短暂的干预,就能显著延迟胰腺癌的发生。
另一方面,研究揭示了经典抑癌基因p53的核心作用。在正常组织损伤修复中,p53的功能是确保“祖细胞样”这种高可塑性状态被及时清除,使组织回归稳态。而p53的缺失,则会导致“祖细胞样”细胞及其生态位不受控制地扩增,并形成一个富含PD-L1高表达巨噬细胞的免疫豁免微环境,为癌变铺平道路。
研究意义与未来展望
研究团队在人类慢性胰腺炎组织中也发现了类似的现象:存在KRT17+的基底样上皮细胞,它们周围同样聚集了富含TNC+成纤维细胞和ARG1+巨噬细胞的免疫抑制性微环境,与小鼠模型中的“祖细胞生态位”高度相似。这证明了该机制在人类疾病中的相关性。
该研究描绘了一个全新的癌症发生框架,同时,传统的抗癌策略往往在癌症已经形成后才介入,此时肿瘤生态系统已根深蒂固,该研究表明,在癌前阶段存在一个关键的干预窗口,这为开发全新的癌症预防和早期干预策略指明了方向。
原文链接:
https://www.cell.com/cell/fulltext/S0092-8674(26)00333-8(转化医学网360zhyx.com)
【关于投稿】
转化医学网(360zhyx.com)是转化医学核心门户,旨在推动基础研究、临床诊疗和产业的发展,核心内容涵盖组学、检验、免疫、肿瘤、心血管、糖尿病等。如您有最新的研究内容发表,欢迎联系我们进行免费报道(公众号菜单栏-在线客服联系),我们的理念:内容创造价值,转化铸就未来!
转化医学网(360zhyx.com)发布的文章旨在介绍前沿医学研究进展,不能作为治疗方案使用;如需获得健康指导,请至正规医院就诊。
责任声明:本稿件如有错误之处,敬请联系转化医学网客服进行修改事宜!
微信号:zhuanhuayixue
 腾讯登录
腾讯登录









还没有人评论,赶快抢个沙发