可改善免疫治疗效果!中山大学等单位合作发文:有前景的食管鳞癌治疗靶点
| 导读 | 本研究揭示了一个此前未被认识的 NIPAL1-HCK-H3K18la 信号回路,该回路将肿瘤代谢与免疫调节相结合,为提高 ESCC 免疫治疗效果提供了有前景的靶点。 |
近日,中山大学/南方医科大学珠江医院/广东省人民医院(广东省医学科学院)研究团队合作共同在期刊《Advanced Science》上发表了题为“NIPAL1 Drives a Metabolic-Epigenetic Feedback Loop to Promote Lactate-Mediated Immune Evasion in Esophageal Cancer”的研究论文,本研究中,研究人员发现食管鳞状细胞癌(ESCC)中存在一个由 NIPAL1 驱动的代谢 - 表观遗传回路,该回路促进肿瘤生长并抑制抗肿瘤免疫。该轴独立于 NIPAL1 的经典镁离子转运活性,并通过损害 CD8+ T 细胞功能促进免疫逃逸。药理学抑制 HCK 或 p300 可破坏此循环并恢复抗肿瘤免疫,使肿瘤对抗 PD-1 治疗敏感。本研究揭示了一个此前未被认识的 NIPAL1-HCK-H3K18la 信号回路,该回路将肿瘤代谢与免疫调节相结合,为提高 ESCC 免疫治疗效果提供了有前景的靶点。
食管鳞状细胞癌免疫治疗疗效受限,探寻肿瘤进展与免疫抵抗分子机制迫在眉睫
01
食管鳞状细胞癌(ESCC)是食管癌(EC)最常见的组织学亚型,仍是一种高度侵袭性的恶性肿瘤,预后不良。尽管免疫治疗,尤其是免疫检查点阻断(ICB)方面近期取得了进展,但临床反应仅限于部分患者。这种有限的疗效在很大程度上归因于免疫逃逸和免疫抑制性肿瘤微环境(TME)。因此,阐明驱动肿瘤进展和免疫抵抗的分子机制对于识别新的治疗靶点和改善 ESCC 患者的预后至关重要。
靶向 NIPAL1-HCK-H3K18la 环路可使肿瘤对免疫检查点疗法敏感
02
鉴于乳酸在维持 T 细胞耗竭中的关键作用,靶向乳酸代谢的治疗策略,如乳酸脱氢酶 A 抑制剂或单羧酸转运蛋白 4 抑制剂,可能通过重编程功能失调的 T 细胞并恢复其抗肿瘤活性与免疫检查点抑制剂(ICIs)产生协同作用。鉴于早期的研究发现 NIPAL1-HCK-H3K18la 环路可调节乳酸分泌,研究人员接下来研究了破坏这一调节回路是否能改善免疫治疗效果。事实上,与单药治疗或对照治疗相比,用 HCK 抑制剂或 p300 抑制剂联合抗 PD-1 抗体治疗携带 NIPAL1 过表达 MC38 肿瘤的小鼠,显著抑制了肿瘤生长。
为了评估这些发现的临床相关性,研究人员通过免疫组化(IHC)检测了 60 名随后接受新辅助免疫治疗的食管鳞状细胞癌(ESCC)患者治疗前活检样本中 NIPAL1、p-LDHA(Y10)和 H3K18la 的表达水平。
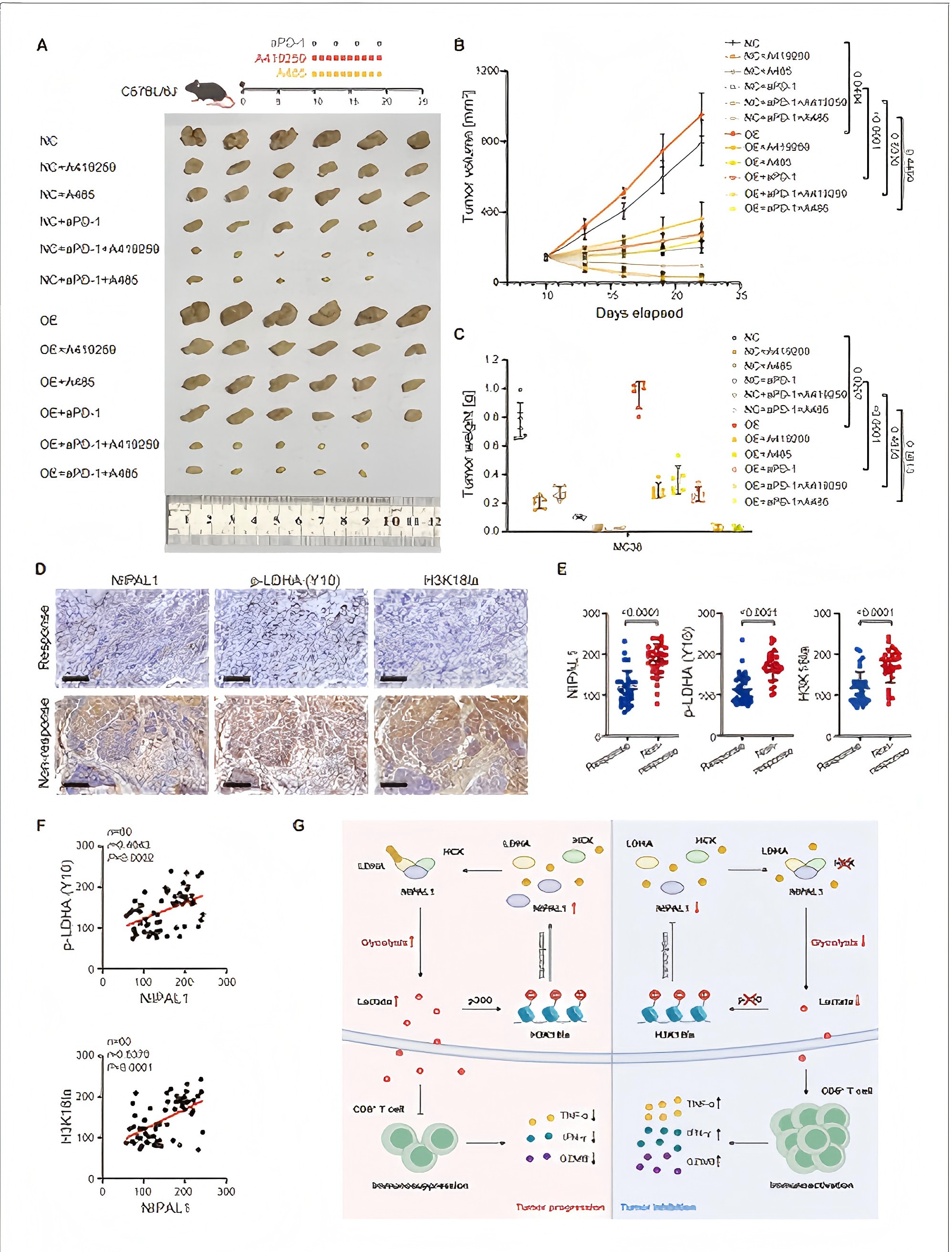
靶向 NIPAL1-HCK-H3K18la 环路可使细胞对检查点疗法敏感
这些数据共同表明,NIPAL1-HCK-H3K18la 信号轴驱动了食管鳞状细胞癌对免疫检查点阻断疗法的耐药性。针对这一正反馈环路进行靶向治疗,可能会提高耐药肿瘤的治疗效果。
结论
03
总之,本研究揭示了食管鳞状细胞癌(ESCC)中由 NIPAL1 驱动的一种此前未被描述的代谢 - 表观遗传 - 免疫交互作用。研究人员确定了 NIPAL1-HCK-p-LDHA-乳酸-p300-H3K18la 级联反应为一个自我强化的信号环路,该环路促进肿瘤生长和免疫逃逸。靶向这一轴不仅重新编程了肿瘤代谢,还恢复了 CD8+T 细胞功能,并使肿瘤对免疫检查点阻断(ICB)敏感。这些发现为在 ESCC 中靶向代谢 - 表观遗传途径,特别是 NIPAL1 驱动的信号级联反应,以增强对免疫治疗的反应性和改善患者预后提供了强有力的依据。
参考资料:
https://advanced.onlinelibrary.wiley.com/doi/10.1002/advs.202520055(转化医学网360zhyx.com)
【关于投稿】
转化医学网(360zhyx.com)是转化医学核心门户,旨在推动基础研究、临床诊疗和产业的发展,核心内容涵盖组学、检验、免疫、肿瘤、心血管、糖尿病等。如您有最新的研究内容发表,欢迎联系我们进行免费报道(公众号菜单栏-在线客服联系),我们的理念:内容创造价值,转化铸就未来!
转化医学网(360zhyx.com)发布的文章旨在介绍前沿医学研究进展,不能作为治疗方案使用;如需获得健康指导,请至正规医院就诊。
责任声明:本稿件如有错误之处,敬请联系转化医学网客服进行修改事宜!
微信号:zhuanhuayixue
 腾讯登录
腾讯登录







还没有人评论,赶快抢个沙发