Cell | 魏炜/马光辉/李玉华/王建祥团队开发“铁蛋白双面胶”,显著增强CAR-T治疗效果,破解耐药难题
| 导读 | 该技术如同为CAR-T细胞装上特制的“双面胶”,能显著增强其对白血病细胞的识别与杀伤能力,为攻克CAR-T疗法临床应用中长期存在的复发与耐药难题,提供了全新、普适且高效的解决方案。 |
近日,中国科学院过程工程研究所魏炜教授/马光辉院士、南方医科大学珠江医院李玉华教授、中国医学科学院血液病医院王建祥教授团队等在国际顶级期刊《Cell》发表一项重磅研究:研究团队成功创制出一种名为“铁蛋白聚集细胞接合器”的仿生新剂型,该技术如同为CAR-T细胞装上特制的“双面胶”,能显著增强其对白血病细胞的识别与杀伤能力,为攻克CAR-T疗法临床应用中长期存在的复发与耐药难题,提供了全新、普适且高效的解决方案。
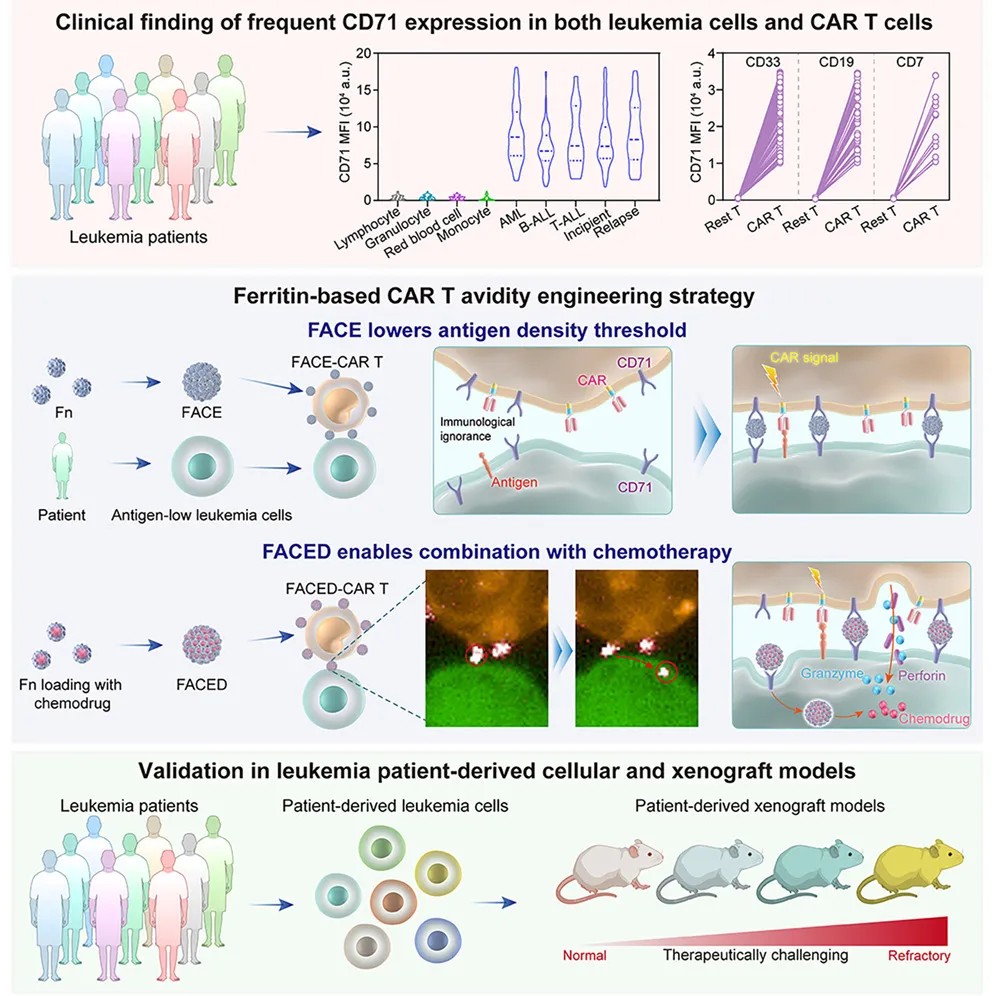
图形摘要
临床困境:抗原调变导致半数患者复发
CAR-T细胞疗法已被公认为白血病治疗领域的里程碑。然而,临床数据显示,超过50%的患者在接受CAR-T治疗后仍会出现疾病复发。其核心原因在于“抗原调变”——在治疗压力下,白血病细胞表面的靶点抗原表达量会主动下调甚至完全丢失,从而隐身逃逸CAR-T细胞的识别与攻击,导致治疗失效。传统应对策略需通过复杂的基因工程重新设计CAR结构或更换靶点,不仅耗时耗力、成本高昂,且难以跟上肿瘤快速演变的步伐。
关键发现:共有的“锚点”CD71
面对这一挑战,研究团队另辟蹊径,从临床样本中寻找共性。他们系统分析了大量来自B细胞急性淋巴细胞白血病、T-ALL及急性髓系白血病患者的骨髓样本,并检测了针对CD19、CD7、CD33等不同靶点的CAR-T细胞。一个关键发现浮出水面:无论是多种类型的白血病细胞,还是对应的CAR-T细胞,都持续、稳定地高表达一种名为CD71的蛋白(转铁蛋白受体)。这提示CD71可能成为一个理想的通用“锚点”,用于构建连接两种细胞的分子桥梁。
创新设计:“铁蛋白双面胶”增强细胞间亲和力
基于这一发现,团队巧妙利用人体内源的铁蛋白(CD71的天然配体),通过精准调控组装条件,创制了“铁蛋白聚集细胞接合器”(FACE)。FACE是由多个铁蛋白颗粒聚集交联形成的约600纳米的球形结构,能像“双面胶”一样,一端通过结合CD71稳固地粘附在CAR-T细胞表面,另一端则在体内精准抓住白血病细胞表面的CD71。
这种物理连接产生了强大的效果。原子力显微镜测定显示,与传统CAR-T细胞相比,经过FACE修饰的CAR-T细胞与白血病细胞之间的作用力最大可增强约24.6倍。这种强化的细胞间亲和力,迫使CAR-T细胞与靶细胞“面对面”,极大地促进了CAR受体对其靶抗原的识别概率,即便在抗原密度很低的情况下也是如此。
显著疗效:降低剂量、突破抗原阈值、实现联合治疗
研究在多种高度贴近临床的白血病患者来源异种移植模型中对FACE策略进行了系统验证,结果令人振奋:
-
高效节能,降低副作用风险:在抗原表达正常的B-ALL模型中,仅需传统CAR-T细胞五分之一的剂量,FACE-CAR T细胞即可达到同等甚至更优的清除效果。同时,治疗小鼠血清中的IL-2、TNF-α、IFN-γ等炎性细胞因子水平更低,体重保持稳定,显示出更好的安全性。
-
攻克耐药,降低抗原阈值:研究人员构建了CD19低表达的白血病模型,以模拟临床耐药情况。此时,传统CAR-T细胞已基本失效。然而,FACE-CAR T细胞仍能有效清除肿瘤,使小鼠生存率达到100%。体外实验也证实,在极低的效应细胞与靶细胞比例下,FACE-CAR T细胞仍保持强大的杀伤力。
-
载药协同,清除漏网之鱼:团队进一步利用铁蛋白天然的笼型空腔结构,开发了载药型连接子(FACED),成功包载临床化疗药物砷(As)。由此构建的FACED-CAR T细胞实现了免疫治疗与化疗的“强强联合”。在含有CD19低表达和CD19阴性白血病细胞的复杂模型中,FACED-CAR T细胞不仅能通过FACE增强对低抗原细胞的识别,还能通过释放药物无差别杀伤抗原阴性细胞,从而实现更彻底、更持久的肿瘤清除。
技术优势:普适、便捷、即插即用
该策略的核心优势在于其平台化特性。无论CAR-T细胞的靶点是CD19、CD7还是CD33,也无论是B-ALL、T-ALL还是AML,只要细胞表达CD71,FACE技术均可适用,展现出强大的普适性。
此外,该技术无需对CAR-T细胞进行任何基因改造,制备过程仅需约30分钟,真正实现了“即插即用”。其成分源于人体内源物质和已批准材料,生物相容性高,为快速临床转化奠定了坚实基础。
研究意义与未来展望
研究团队已在20余种贴近临床的动物模型上完成了系统验证,并初步建立了基于CD71表达水平和抗原密度的疗效预测模型,旨在未来实现针对不同患者的精准治疗。
这项研究标志着CAR-T疗法“亲和力工程”新范式的诞生。它通过一种简单、巧妙的物理化学方法,而非复杂的基因操纵,从根本上提升了CAR-T细胞的功能,突破了当前的技术瓶颈。这一创新策略不仅为难治复发白血病患者带来了新的希望,其“连接+载药”的双功能平台设计思路,也为更广泛的肿瘤免疫治疗乃至其他细胞疗法的发展提供了借鉴。
原文链接:
https://www.cell.com/cell/abstract/S0092-8674(26)00170-4(转化医学网360zhyx.com)
【关于投稿】
转化医学网(360zhyx.com)是转化医学核心门户,旨在推动基础研究、临床诊疗和产业的发展,核心内容涵盖组学、检验、免疫、肿瘤、心血管、糖尿病等。如您有最新的研究内容发表,欢迎联系我们进行免费报道(公众号菜单栏-在线客服联系),我们的理念:内容创造价值,转化铸就未来!
转化医学网(360zhyx.com)发布的文章旨在介绍前沿医学研究进展,不能作为治疗方案使用;如需获得健康指导,请至正规医院就诊。
责任声明:本稿件如有错误之处,敬请联系转化医学网客服进行修改事宜!
微信号:zhuanhuayixue
 腾讯登录
腾讯登录







还没有人评论,赶快抢个沙发