有效逆转抗原逃逸!同济大学附属东方医院发文:克服免疫治疗耐药性可行且有前景的策略
| 导读 | 这项工作凸显了通过调节细胞内运输来克服细胞免疫疗法耐药性的治疗潜力。 |
近日,同济大学附属东方医院研究团队在期刊《Journal for ImmunoTherapy of Cancer》上发表了题为“Targeting endosomal trafficking-mediated antigen escape to resensitize myeloma to CAR-T therapy”的研究论文,本研究确立了由 RRM2 驱动的运输为嵌合抗原受体 T 细胞(CAR-T)疗法中抗原逃逸的一种新型且可靶向的机制。通过重新利用奥沙利铂来恢复 MICA/B 表面表达,研究人员提供了一种可临床转化的策略,该策略能特异性增强 NKG2D CAR-T 细胞在多发性骨髓瘤中的疗效,并有可能增强靶向多种抗原的 CAR-T 疗法的疗效。这项工作凸显了通过调节细胞内运输来克服细胞免疫疗法耐药性的治疗潜力。
CAR-T 疗法挑战:聚焦细胞内运输对靶抗原丰度及疗效的影响
01
嵌合抗原受体(CAR)T 细胞疗法彻底改变了血液系统恶性肿瘤的治疗。然而,CAR-T 疗法面临一个关键挑战,即约 50%的患者在 1 至 2 年内出现复发或耐药,这主要是由于抗原逃逸。此外,临床试验结果表明,许多多发性骨髓瘤患者在接受 CAR-T 治疗后仍无反应,这可能是由于抗原呈递不足,这可能会限制治疗效果。临床前研究证实,增强抗原表达可以提高细胞治疗的疗效。一种新兴的观点认为,细胞表面蛋白的丰度是由细胞内运输动态控制的,这一过程的影响远远超出了转录调控。
尽管存在这种更广泛的范式,但对抗原靶点的研究仍局限于转录和转录后调控,而细胞内运输的关键作用却被忽视了。包括降解和内吞循环在内的细胞内运输途径,可能对治疗靶点在细胞表面的丰度起着决定性作用。近期的研究还强调了嵌合抗原受体(CAR)的内化和循环是决定血液系统恶性肿瘤中 CAR-T 疗法效力的关键因素。然而,通过调节运输和循环途径来提高靶抗原丰度的治疗策略尚未得到探索。
低剂量奥沙利铂在体内与 NKG2D CAR-T 疗法具有协同作用
02
为了进一步评估低剂量奥沙利铂联合 NKG2D CAR-T 细胞在体内多发性骨髓瘤(MM)模型中的治疗效果,研究人员使用了携带 ARP1-荧光素酶异种移植物的 NSG 小鼠,并在多发性骨髓瘤注射后每天给予低剂量奥沙利铂(15 毫克/千克)。
在治疗 1 周后采集血清,发现使用奥沙米特治疗的小鼠体内嵌合抗原受体 T 细胞(CAR-T)扩增以及细胞因子释放(TNF-α、IFN-γ、IL-6 和穿孔素)均有所升高。流式细胞术显示,外周血中多发性骨髓瘤(MM)的 NKG2D CAR-T 细胞扩增显著增加,且 MICA/B 丰度增强。此外,外周血的流式细胞术分析表明,奥沙米特给药显著增加了 NKG2D CAR-T 细胞的比例,降低了 CD4+ 和 CD8+ NKG2D CAR-T 细胞中的耗竭标志物(包括 PD-1)。此外,通过检测 CD69 的平均荧光强度(MFI),发现奥沙米特处理的 NKG2D CAR-T 细胞表现出显著增强的效应功能。对骨髓和脾脏切片进行免疫组化分析显示,与单独使用 NKG2D CAR-T 细胞治疗的小鼠相比,使用奥沙利铂和 NKG2D CAR-T 细胞治疗的小鼠体内 CD138+ 多发性骨髓瘤细胞显著减少。这些发现表明,奥沙利铂在体内增强了 NKG2D CAR-T 细胞的抗肿瘤效力和适应性,为多发性骨髓瘤提供了一种有前景的治疗策略。
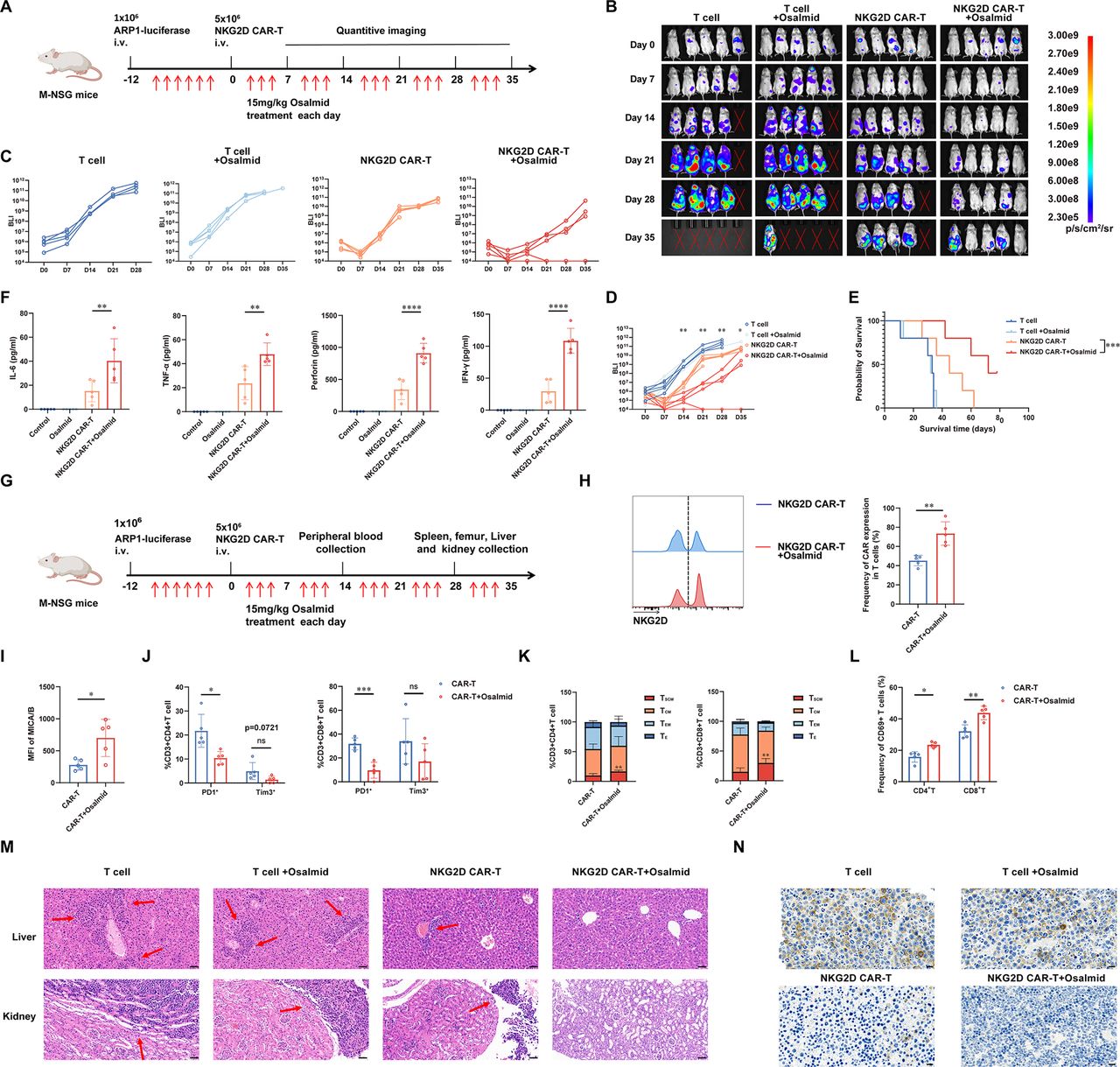
低剂量奥沙利铂介导的体内抗肿瘤疗效增强的验证
结论
03
总体而言,通过确立 RRM2-TBC1D15-RAB7A 轴作为具有临床应用价值的靶点,研究人员开创了一种基于 RRM2 的运输策略以增强细胞疗法的效果,将奥沙米特定位为一种联合用药,以克服抗原逃逸并提高多发性骨髓瘤中 CAR-T 疗法的疗效。(转化医学网360zhyx.com)
参考资料:
https://jitc.bmj.com/content/14/3/e014040
【关于投稿】
转化医学网(360zhyx.com)是转化医学核心门户,旨在推动基础研究、临床诊疗和产业的发展,核心内容涵盖组学、检验、免疫、肿瘤、心血管、糖尿病等。如您有最新的研究内容发表,欢迎联系我们进行免费报道(公众号菜单栏-在线客服联系),我们的理念:内容创造价值,转化铸就未来!
转化医学网(360zhyx.com)发布的文章旨在介绍前沿医学研究进展,不能作为治疗方案使用;如需获得健康指导,请至正规医院就诊。
责任声明:本稿件如有错误之处,敬请联系转化医学网客服进行修改事宜!
微信号:zhuanhuayixue
 腾讯登录
腾讯登录









还没有人评论,赶快抢个沙发