靶向分泌自噬!南京市口腔医院:治疗侵袭性口腔鳞癌有前景的策略
| 导读 | 最差的浸润模式(WPOI)是口腔鳞状细胞癌(OSCC)中一个重要的组织学预后指标,但导致高 WPOI 的潜在机制仍不清楚。 |
近日,南京市口腔医院研究团队在期刊《Clinical And Translational Medicine》上发表了研究论文,题为“Hypoxia-induced secretory autophagy in cancer-associated fibroblasts promotes ECM remodelling through serglycin secretion in oral squamous cell carcinoma”,本研究中,单细胞 RNA 测序(scRNA-seq)显示,在高 WPOI(4 - 5)的口腔鳞状细胞癌(OSCC)组织中,癌相关成纤维细胞(CAFs)显著富集,尤其是表达 SRGN 的肌成纤维细胞亚群。在低氧条件下,CAFs 将 SRGN 分泌从传统的内质网 - 高尔基体途径切换到依赖自噬体形成但独立于溶酶体降解的非传统分泌自噬途径。分泌的 SRGN 直接与细胞外基质(ECM)中的MMP2和MMP9相互作用,增强 ECM 重塑和 OSCC 的侵袭和迁移。在体内,无论是通过基因敲除 CAFs 中的 SRGN 还是通过药物抑制自噬,均显著抑制肿瘤生长,抑制胶原蛋白 I 的降解,并恢复 E-钙粘蛋白的表达。靶向分泌性自噬或丝甘素原糖蛋白的治疗策略有望成为侵袭性口腔鳞状细胞癌的一种有效疗法。

https://onlinelibrary.wiley.com/doi/10.1002/ctm2.70556
口腔鳞状细胞癌预后与浸润模式关联研究
01
口腔鳞状细胞癌(OSCC)是头颈部癌症的主要类型,在 2020 年约占新诊断癌症病例的 2%,并导致 1.8%的癌症相关死亡。研究人员建立了口腔鳞状细胞癌预后的风险分层模型,其中包括浸润模式(POI)——这是在宿主-肿瘤边缘处肿瘤侵袭的一种组织学测量指标。浸润模式有五种类型,前三种为低侵袭性,而后两种则具有更广泛的浸润模式,这也代表着更高的侵袭程度。最差的浸润模式(WPOI)被定义为每位患者的最高得分,是早期口腔鳞状细胞癌最可靠的预后指标。
CAFs 通过体内分泌性自噬促进肿瘤侵袭和细胞外基质降解
02
为了评估癌相关成纤维细胞(CAF)对体内肿瘤侵袭的影响,研究人员使用裸鼠建立了原位异种移植模型,将其随机分为四组:(a)CAL27;(b)CAL27 + 野生型 CAF;(c)CAL27 + 用 3-MA 处理的野生型 CAF;(d)CAL27 + SRGN 基因敲除型 CAF。两周后,肿瘤分析显示,与单独的 CAL27 相比,野生型 CAF 显著促进了 CAL27 肿瘤的生长,但这种促进作用被 3-MA 或 SRGN 基因敲除显著抑制。组织学分析表明,(b)组显示出核异型性、去分化和中心坏死,表明其增殖、侵袭潜能和恶性程度更高。通过免疫组化染色评估了每组肿瘤的侵袭潜能。结果表明,在(b)组中,E-钙粘蛋白表达显著下调,胶原蛋白 I 明显降解,并且在坏死区域观察到广泛的 MMP2/MMP9 浸润,这与活跃的细胞外基质重塑区域一致,表明侵袭性增强。然而,这种增强的侵袭性可以通过 3-MA 处理或 SRGN 基因敲除逆转。值得注意的是,尽管体外实验表明,3-MA 对自噬的抑制作用在药物撤除后 24 至 48 小时内减弱,但其在体内的抑瘤效果却持续存在。通过酶联免疫吸附测定分析,研究人员发现,即使自噬流已恢复,癌相关成纤维细胞(CAFs)仍显著抑制了硫酸软骨素蛋白聚糖(SRGN)的分泌能力。综上所述,这些结果表明,CAFs 通过自噬介导的 SRGN 分泌促进口腔鳞状细胞癌(OSCC)在体内的生长和侵袭,并且靶向这一途径的短期干预能够产生持久的抑瘤效果。
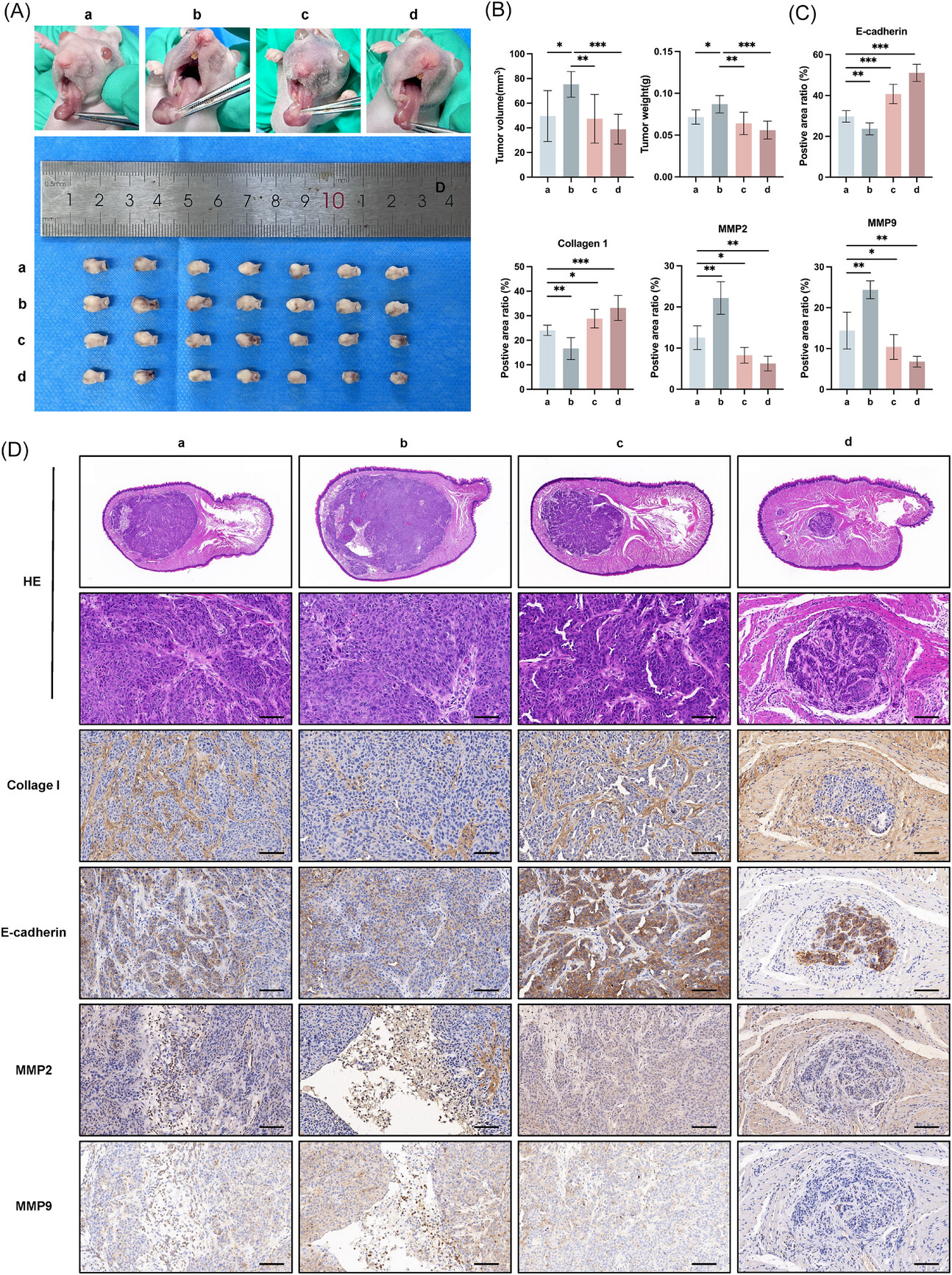
CAF 衍生的 SRGN 通过自噬分泌促进肿瘤侵袭和细胞外基质降解
结论
03
总之,本研究揭示了在低氧口腔鳞状细胞癌(OSCC)微环境中,由癌相关成纤维细胞(CAFs)分泌的关键细胞因子 SRGN 通过自噬依赖性途径进行分泌。在 WPOI 4–5 型 OSCC 中,开发有效的策略来敲低 SRGN 可能有助于克服由 SRGN 分泌所诱导的肿瘤进展。(转化医学网360zhyx.com)
参考资料:
https://onlinelibrary.wiley.com/doi/10.1002/ctm2.70556
【关于投稿】
转化医学网(360zhyx.com)是转化医学核心门户,旨在推动基础研究、临床诊疗和产业的发展,核心内容涵盖组学、检验、免疫、肿瘤、心血管、糖尿病等。如您有最新的研究内容发表,欢迎联系我们进行免费报道(公众号菜单栏-在线客服联系),我们的理念:内容创造价值,转化铸就未来!
转化医学网(360zhyx.com)发布的文章旨在介绍前沿医学研究进展,不能作为治疗方案使用;如需获得健康指导,请至正规医院就诊。
责任声明:本稿件如有错误之处,敬请联系转化医学网客服进行修改事宜!
微信号:zhuanhuayixue
 腾讯登录
腾讯登录







还没有人评论,赶快抢个沙发