脑科学研究新突破!美国得克萨斯大学赵中明团队通过单细胞多组学揭示早发性阿尔茨海默病调控机制
| 导读 | 该研究为理解sEOAD的发病机制提供了高分辨率图谱,并指出神经胶质细胞与神经元之间的通讯异常可能是疾病进展的关键因素。 |
近日,美国得克萨斯大学赵中明团队在知名期刊《Science Advances》发表一项重磅研究:对9名捐赠者的死后脑组织进行了分析,涵盖了前额叶皮层、内嗅皮层和海马体三个关键脑区。通过单细胞核多组学技术,成功解析了76,173个细胞核的转录组和表观基因组信息。系统揭示了散发性早发性阿尔茨海默病(sEOAD)在多脑区的转录组和染色质调控变化。该研究为理解sEOAD的发病机制提供了高分辨率图谱,并指出神经胶质细胞与神经元之间的通讯异常可能是疾病进展的关键因素。
技术突破:单细胞多组学揭示细胞特异性紊乱
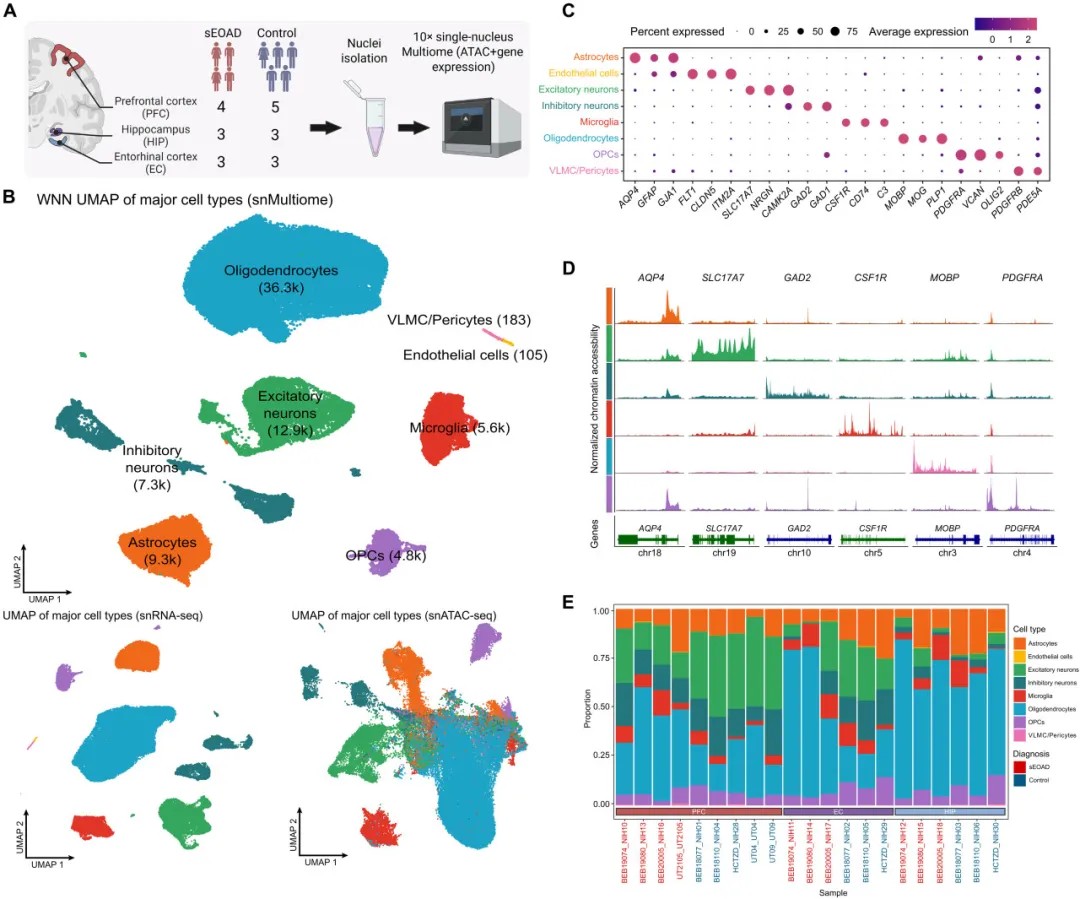
单核多组学分析表征了sEOAD患者三个脑区中的细胞类型特异性表达与调控
研究团队对9例sEOAD患者及健康对照者的7.6万个细胞核进行联合单细胞RNA测序和染色质可及性测序,首次在sEOAD中整合多脑区分析。结果显示,内嗅皮层和海马体作为阿尔茨海默病早期受累区域,其转录组变化比前额叶皮层更显著,差异表达基因数量分别达3348个和2735个,且效应值更大。值得注意的是,少突胶质细胞在sEOAD内嗅皮层中比例升高,提示髓鞘修复可能参与疾病代偿机制。
关键调控因子:RFX4与IKZF1的跨区域作用
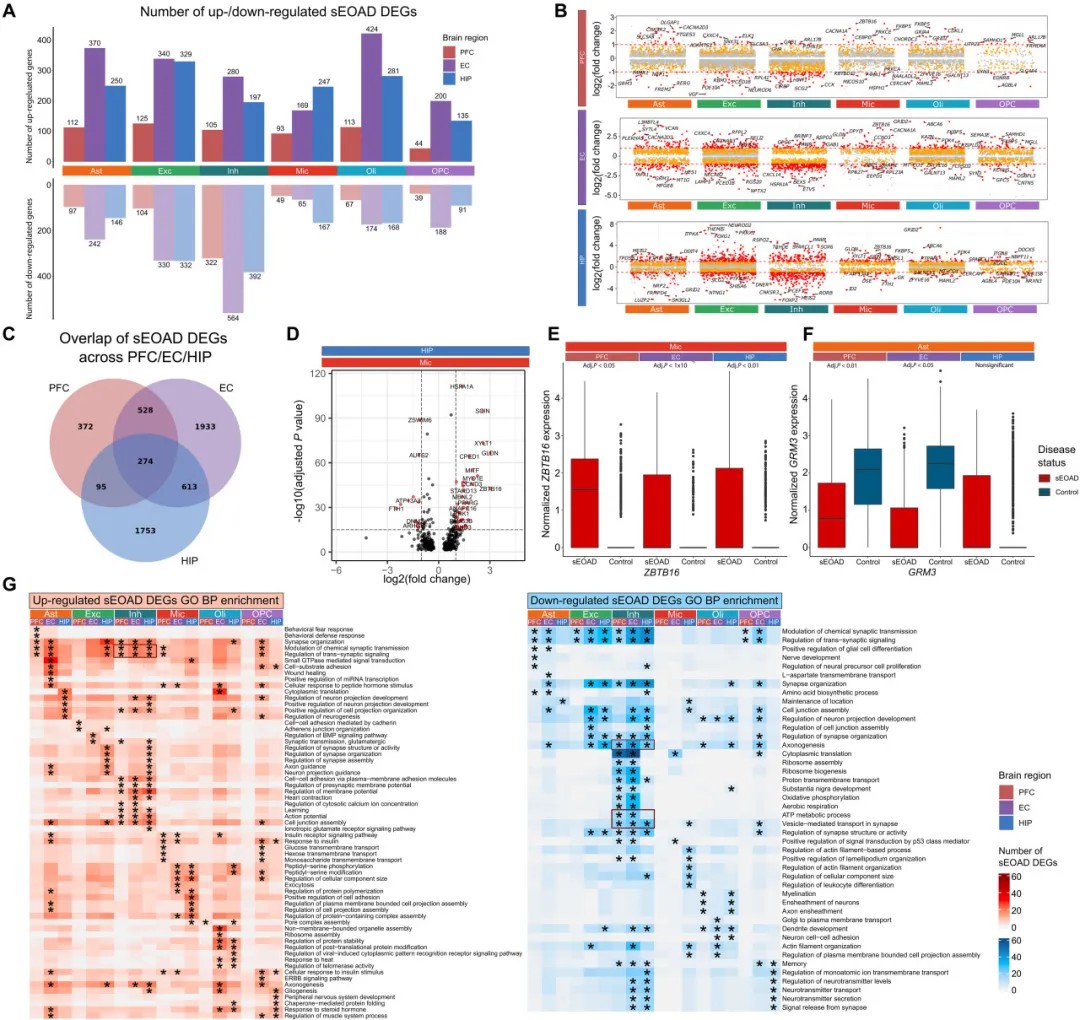
sEOAD中的细胞类型特异性转录组改变揭示了星形胶质细胞和神经元内跨脑区的突触信号相关通路失调
通过染色质可及性-基因关联分析,研究发现了8个保守的转录因子在不同脑区的胶质细胞中调控sEOAD相关基因。其中,星形胶质细胞的RFX4和小胶质细胞的IKZF1 在不同脑区均表现出显著调控活性。RFX4通过增强子驱动与突触信号和Wnt通路相关的基因,而IKZF1则调节小胶质细胞的免疫反应基因。DNA足迹分析进一步验证了这些因子在疾病状态下的结合活性增强。
细胞间通讯异常:神经炎症与突触信号失衡
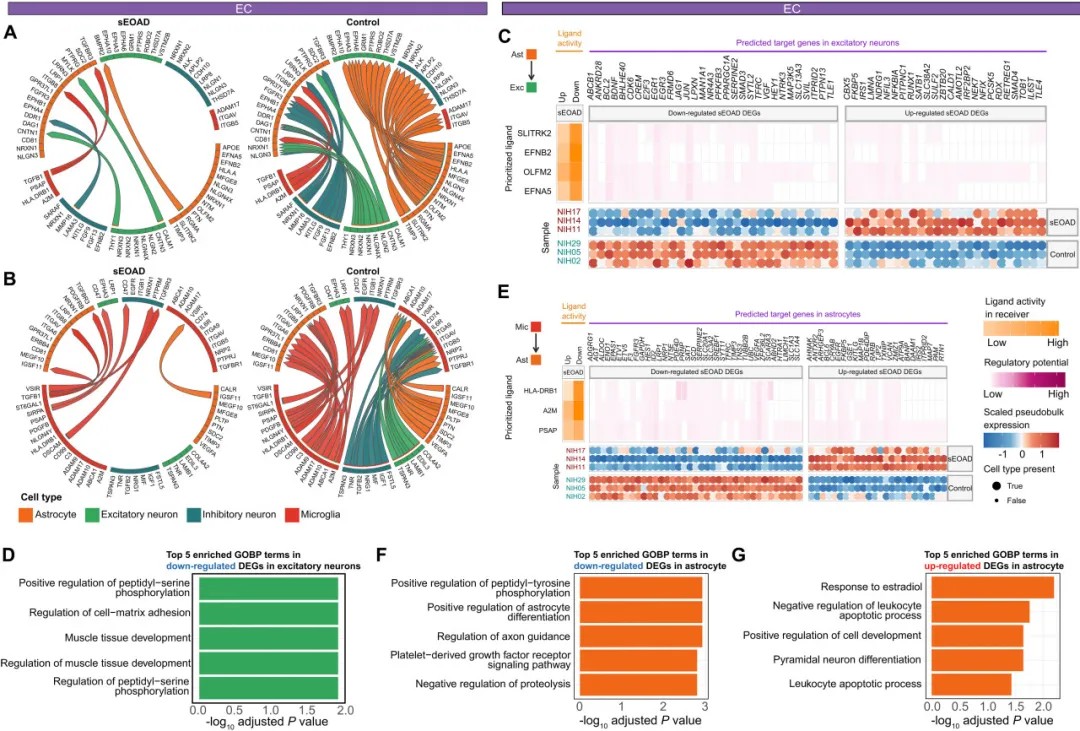
比较性细胞间信号分析揭示了sEOAD与对照组在内嗅皮层中的细胞间通讯信号失调
细胞间信号分析揭示了sEOAD中胶质细胞与神经元通讯的广泛失调。在内嗅皮层,星形胶质细胞向兴奋性神经元发送的25条关键信号均下调。同时,小胶质细胞来源的PSAP-LRP1信号在三个脑区均减弱,而TGFB1-ITGB8信号上调,表明神经炎症与修复平衡被破坏。这些紊乱信号进一步影响神经元内EGR1、JUN等转录因子表达,导致突触功能相关通路异常。
遗传风险交叉:精神疾病与阿尔茨海默病的共享变异
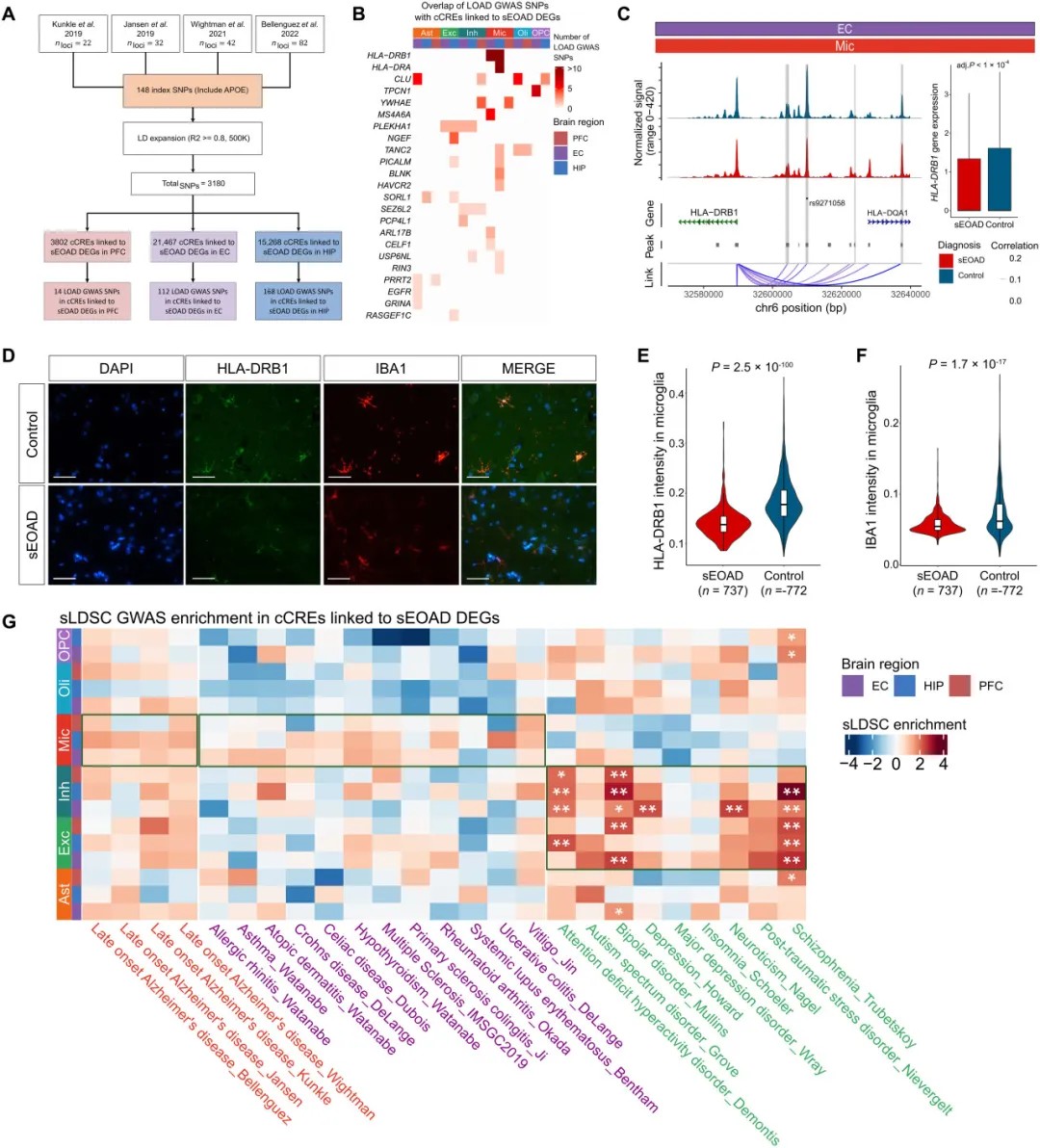
在sEOAD中绘制与细胞类型及区域特异性候选顺式调控元件相关的全基因组关联位点
通过整合晚发性阿尔茨海默病的GWAS数据,研究发现33个sEOAD相关的调控元件与已知风险位点重叠。此外,sEOAD特有的调控元件在兴奋性/抑制性神经元中显著富集精神分裂症、双相情感障碍等精神疾病的风险变异,提示sEOAD与神经精神疾病存在部分共享的遗传基础。(转化医学网360zhyx.com)
该研究不仅提供了sEOAD的多组学资源,还揭示了区域特异性调控网络的重要性。
原文链接:
https://www.science.org/doi/10.1126/sciadv.adw4917
【关于投稿】
转化医学网(360zhyx.com)是转化医学核心门户,旨在推动基础研究、临床诊疗和产业的发展,核心内容涵盖组学、检验、免疫、肿瘤、心血管、糖尿病等。如您有最新的研究内容发表,欢迎联系我们进行免费报道(公众号菜单栏-在线客服联系),我们的理念:内容创造价值,转化铸就未来!
转化医学网(360zhyx.com)发布的文章旨在介绍前沿医学研究进展,不能作为治疗方案使用;如需获得健康指导,请至正规医院就诊。
责任声明:本稿件如有错误之处,敬请联系转化医学网客服进行修改事宜!
微信号:zhuanhuayixue
 腾讯登录
腾讯登录







还没有人评论,赶快抢个沙发