“候选靶点”!剑桥大学发文:揭示胰腺癌转移新机制
| 导读 | 胰腺导管腺癌(PDAC)预后不良,肿瘤相关成纤维细胞(CAFs)是公认的潜在治疗靶点,但对这些异质性细胞群的了解不足,阻碍了有效治疗策略的开发。 |
12月28日,剑桥大学研究人员在《Cancer Cell》杂志上发表了题为“EGFR-activated myofibroblasts promote metastasis of pancreatic cancer”的研究论文,研究人员表明表皮生长因子受体/Erb-B2受体(EGFR/ERBB2)信号是通过双调蛋白介导的自分泌过程在myCAFs中由TGF-β诱导的。在PDAC器官源性培养物和小鼠模型中,对这种EGFR/ERBB2信号网络的抑制对不同的CAF亚型有不同的影响,为它们异质性的机制提供了深入的见解。最后,对其他癌症数据集的分析表明,这些过程可能在其他恶性肿瘤中发生。这些数据为myCAF异质性提供了功能相关性,并确定了预防PDAC肿瘤侵袭的候选靶点。

https://doi.org/10.1016/j.ccell.2023.12.002
研究背景
01
预计到2030年,胰腺导管腺癌(PDAC)将成为癌症相关死亡的第二大常见原因。PDAC通常是致命的,因为它通常在患者发生转移后才被诊断出来。所以,我们迫切需要研究PDAC的转移机制、预防和治疗方法。与其他任何癌症相比,PDAC有一个特点就是具有丰富的非恶性间质,这种间质可以促进肿瘤生长并导致耐药性。其中大部分由不同类型的肿瘤相关成纤维细胞(CAFs)组成,包括具有不同分子特征和潜在功能的肌成纤维细胞CAFs(myCAFs)、炎性CAFs(iCAFs)和抗原呈递CAFs(apCAFs)。
研究人员先前发现白细胞介素1(IL-1)和转化生长因子β(TGF-β)分别是诱导iCAF和myCAF形成的主要恶性细胞源性配体3。虽然IL-1信号通路下游的通路已经揭示了iCAF治疗靶点,但TGF-β诱导的myCAF中活跃的通路在很大程度上仍是未知的。
研究成果
02
研究人员证明了EGFR激活的myCAFs在促进小鼠PDAC转移中的作用,并且揭示了双向恶性细胞-成纤维细胞串联调节PDAC myCAF分子和功能异质性并驱动转移的机制。
观察结果表明其他自分泌或旁分泌介质可能有助于保持myCAFs中EGFR持续激活状态。此外,由恶性细胞和/或免疫细胞(包括巨噬细胞)产生的AREG可能进一步促进myCAFs中EGFR/ERBB2的激活。研究人员验证了一个模型: 活化 TGF-β 通路对下游 AREG 的诱导和有效 EGFR 信号都是必需的。最后, 研究人员发现 EGFR 和 ERBB2 在 PSCs 中均被 TGF-β 或 PDAC 类器官 CM 处理所激活。抑制 EGFR/ERBB2 比单纯抑制 EGFR 更深入地降低了 myCafs 中 AREG 的表达,并且 Erbb2 缺失损害了 EGFr 的激活。因此, 可见 EGFr 和 ERBB2 协同诱导 AREG 表达并在 TGF-beta 引起 myCafs 下游信号传递方面发挥重要作用。
虽然研究人员确定了EGFR激活的myCAFs的肿瘤促进作用,但之前的研究提出了αSMA阳性或HH激活的肌成纤维细胞的肿瘤抑制作用,这在很大程度上归因于myCAF介导的胶原沉积。在这里,研究人员表明,与CD90+ myCAFs相比,EGFR激活的CD90- myCAFs表达较低的胶原水平,因此,EGFR/ERBB2抑制并不影响胶原丰度或整体纤维化。总之,这些观察结果强调了PDAC中myCAF群体以前未被重视的复杂性,需要进一步了解它们的分子和功能异质性,以制定有效的组合策略。
研究结果表明在myCAFs中EGFR信号的遗传缺失或药理学抑制通过下调EMT信号来损害恶性细胞的转移潜力,这已被证明在某些情况下促进PDAC恶性细胞可塑性和转移。
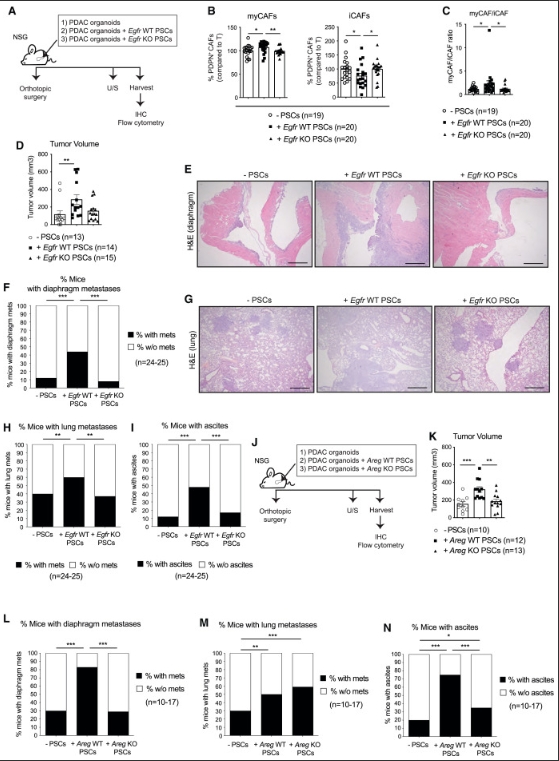
EGFR激活的myCAFs促进PDAC的转移
研究表明,在PDAC中抑制EGFR可能有助于与免疫疗法相结合, 有利于EGFR野生型病例并逆转对KRAS抑制剂的耐药性,本研究可能对PDAC患者具有临床意义。此外,研究人员的观察可能具有更广泛的影响。AREG/EGFR信号可能是许多纤维化疾病的共同特征,其中肌成纤维细胞发挥着重要作用。
研究结论
03
本研究揭示了EGFR/ERBB2信号通路在PDAC myCAFs的一个子集中是活跃的,强调了以前未被重视的EGFR/ERBB2信号抑制对PDAC间质的影响,这可能也发生在其他恶性肿瘤中,并确定了EGFR激活的myCAFs在促进PDAC转移中的作用。(转化医学网360zhyx.com)
参考资料:
https://doi.org/10.1016/j.ccell.2023.12.002
注:本文旨在介绍医学研究进展,不能作为治疗方案参考。如需获得健康指导,请至正规医院就诊。
 腾讯登录
腾讯登录









还没有人评论,赶快抢个沙发