战肠癌,破译癌转移“罪魁祸首”!中山大学最新发文
| 导读 | 转移是癌症死亡的主要原因。然而,原发性肿瘤中有哪些类型的异质性癌细胞以及它们如何转移到靶器官在很大程度上仍未被发现。 |
近日,中山大学郑健、林东昕等在期刊《Gut》上发表题为“Single-cell transcriptomic analysis deciphers heterogenous cancer stem-like cells in colorectal cancer and their organ-specific metastasis”的研究论文,研究破译了原发性结直肠癌组织、结直肠癌肝和卵巢转移组织中异质性癌细胞的亚型,以及单细胞分辨率下器官特异性结直肠癌转移的特征。

https://gut.bmj.com/content/early/2023/11/30/gutjnl-2023-330243
研究背景
01
结直肠癌(CRC)是世界上第三大最常见和致命的癌症。肿瘤转移占结直肠癌死亡的 90%,据报道 5 年生存率为 <20%。虽然结直肠癌最常见的转移部位是淋巴结、肝脏和肺,但一部分结直肠癌可以转移到骨骼和卵巢。结直肠癌的卵巢转移被认为是由恶性细胞通过腹水从浆膜表面扩散到腹膜腔直接定植的。在过去的五十年中,对各种类型癌症的研究表明,尽管肿瘤中存在许多异质性细胞,但只有某些类型的恶性细胞才能驱动复发和远处转移。然而,迄今为止,似乎还没有关于哪种亚型异质性结直肠癌细胞更适合远处转移的系统研究。
单细胞RNA测序(scRNA-seq)可以解剖异质性肿瘤并破译细胞组成。最近的研究比较了原发性结直肠癌及其肝转移性结直肠癌(lCRC)微环境中的细胞组成,发现与原发性结直肠癌相比,某些免疫细胞亚型(如肿瘤相关巨噬细胞和周细胞)在lCRC中显著富集。另一项研究报告称,与原发性结直肠癌相比,lCRC 中未成熟浆细胞增加,但活化的 B 细胞减少。尽管这些研究表明了不同免疫特征在结直肠癌和l结直肠癌微环境中的重要性,但仍未揭示哪种恶性细胞亚型是转移罪魁祸首。此外,据我们所知,卵巢转移性结直肠癌(oCRC)的肿瘤微环境和细胞组成从未被探索过。
研究进展
02
我们对 7 例远处转移的 CRC 患者的 29 份样本进行了 scRNA-seq,包括 8 例原发性 CRC、5 例 oCRC、2 例 lCRC、7 例邻近正常组织和 7 例外周血单核细胞 (PBMC)。我们还下载了来自 24 名患者的 41 个样本的公开 scRNA-seq 数据,包括 29 个 CRC 和 12 个邻近正常组织,以增加统计功效。在这 24 例患者中,有 3 例有远处转移,但无法获得详细的转移信息。因此,在最终分析中,我们有 31 例 CRC 患者,包括 10 例远处转移。所有结直肠癌均被诊断为微卫星稳定型(MSS)结直肠癌。患者和组织样本的工作流程和详细信息如图1A所示。
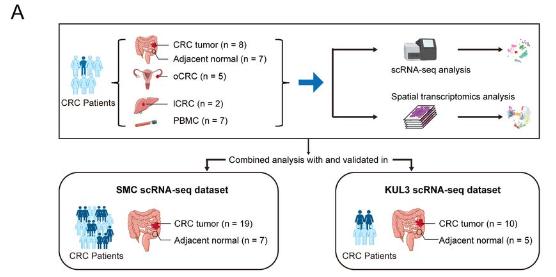
CRC样本采集、scRNA-seq和空间转录组学分析的示意图,以及与公开数据集的联合分析
我们对表达EPCAM和KRT18的上皮细胞进行了亚分类,发现所有患者都存在14种细胞亚型(图2A)。这14种细胞亚型的标记基因如图2B所示。 在14种细胞亚型中,我们鉴定了5种恶性细胞亚型,包括高表达ASCL2和PTPRO的干细胞样细胞、表达DNAJB1和RND3的DNAJB1恶性细胞、表达FDPS和SCD的FDPS恶性细胞、表达GPRC5A和SLC2A1的GPRC5A恶性细胞以及表达IL32和S100A11的IL32恶性细胞(图2B)。我们发现肠细胞在正常结直肠组织中富集,胆管细胞在lCRC和干细胞样细胞中富集,其他恶性细胞亚型在原发性和转移性CRC样本中富集(图2C)。来自原发性结直肠癌和转移性结直肠癌的干细胞样恶性细胞亚型的DNA拷贝数变异明显高于邻近正常组织的上皮细胞(图2D-E)。然后,我们应用CytoTRACE14预测了5种恶性细胞亚型的分化状态,结果显示干细胞样细胞在lCRC或oCRC中具有明显高于其他细胞类型的分化潜力。基于分区的图抽象分析表明,与其他上皮细胞亚型相比,干细胞样细胞与恶性细胞亚型的进化关系更密切(图2F)。RNA速度分析表明,流动方向是从干细胞样细胞到其他恶性细胞亚型(图2F)。此外,在所有上皮细胞亚型中,干细胞样细胞具有最高的干性特征评分(图2G)。这些结果表明,干细胞样细胞可能是CRC转移的始作俑者。
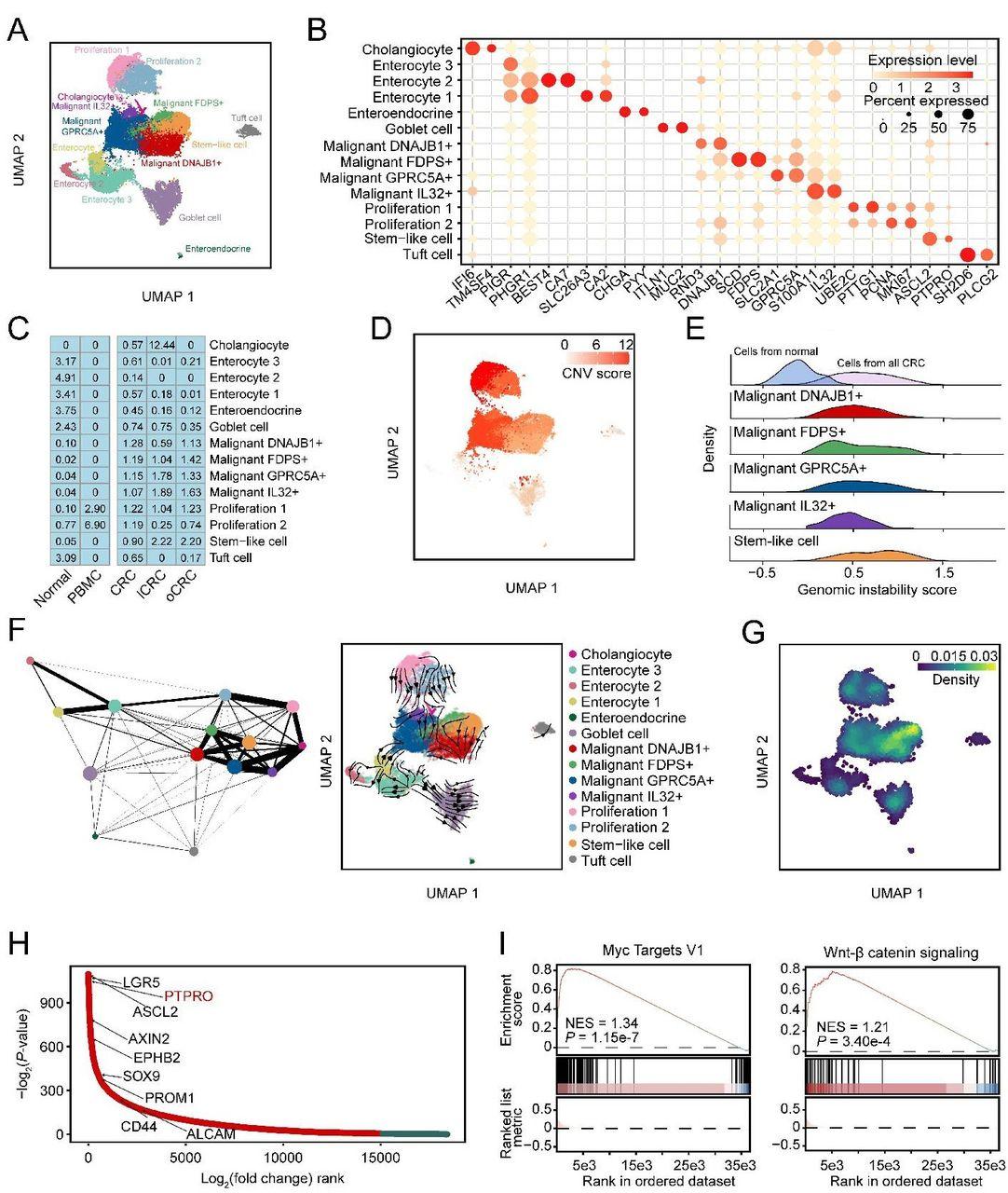
干细胞样细胞是结直肠癌转移的始作俑者
研究结论
03
总之,通过使用整合scRNA-seq、空间转录组分析和功能测定,我们发现了一个以PTPRO和ASCL2为转移罪魁祸首的干细胞样细胞簇,其亚群显示出进一步不同的肝脏或卵巢器官趋性。在原发性结直肠癌中,转移的结直肠癌细胞通过NOTCH信号通路与CAF和D内皮细胞相互作用,为其转移获取营养和能量。我们的研究结果揭示了器官特异性CRC转移的转移罪魁祸首。此外,先前的研究报道了包括 LGR5 和 AXIN2 在内的 Wnt 靶基因是上皮组织中的功能性干细胞标志物,而 ASCL2 仅限于胃和肠道干细胞。Wang 等人表明,高水平的 ASCL2 表达对于维持胃 CSC 的自我更新特性和致癌性至关重要。 因此,我们的发现也可能与其他胃肠道癌症有关,尤其是胃癌,这值得深入研究。(转化医学网360zhyx.com)
参考资料:
https://gut.bmj.com/content/early/2023/11/30/gutjnl-2023-330243
注:本文旨在介绍医学研究进展,不能作为治疗方案参考。如需获得健康指导,请至正规医院就诊。
 腾讯登录
腾讯登录









还没有人评论,赶快抢个沙发