【Nature子刊】王红阳院士等联合复旦学者发文揭示肝癌治疗新策略
| 导读 | 由于耐药性,基于酪氨酸激酶抑制剂(TKI)的全身治疗晚期肝细胞癌(HCC)的临床获益有限。 |
10月7日,海军医科大学王红阳院士等联合复旦大学研究人员共同通讯在《Nature Communications》上发表题为“URI alleviates tyrosine kinase inhibitors-induced ferroptosis by reprogramming lipid metabolism in p53 wild-type liver cancers”的研究论文,展示了URI在HCC脂质代谢重编程中的作用,部分是通过以p53依赖性方式维持异常的SCD1表达,这反过来又促进了HCC对TKI诱导的铁死亡的抗性。除此之外,本研究还为测试SCD1抑制剂和TKIs联合治疗野生型p53晚期HCC提供了强有力的理由。

https://www.nature.com/articles/s41467-023-41852-z#Abs1
研究背景
01
在世界范围内,原发性肝癌是第六大常见诊断癌症,也是癌症死亡的第三大原因。肝细胞癌(HCC)占所有肝癌病例的75-80%。据估计,大约50-60%的肝细胞癌患者,尤其是晚期肝细胞癌患者,在其一生中接受全身治疗。目前,基于酪氨酸激酶抑制剂(TKIs)的全身疗法广泛用于巴塞罗那诊所肝癌(BCLC)-B/C分期的HCC患者,包括索拉非尼、瑞戈非尼、仑伐替尼和多纳非尼。不幸的是,这些药物作为单一药物只能适度提高生存率。最近的研究表明,联合治疗,例如TKIs和免疫检查点抑制剂(ICIs)的组合,显示出光明的前景。同样,需要最佳的联合疗法和新的生物标志物来提高基于TKIs的HCC疗法的临床益处。
研究进展
02
首先,我们进行了RNA测序(RNA-seq)分析以表征URI依赖性转录组改变。我们发现,在shRNA(Ctrl)和shURI HepG2细胞之间共有1676个基因差异表达。使用京都基因和基因组百科全书(KEGG)途径进行的功能富集分析显示,铁死亡是URI调节的最大改变途径之一(图1a)。铁死亡相关基因的表达随着URI敲低而增加。基因集富集分析(GSEA)显示,与对照组相比,shURI细胞中的铁死亡(而非细胞凋亡信号传导)呈正富集。(图 1b)。这些结果表明,URI可能在铁死亡中起重要作用。同时,包括EGFR酪氨酸激酶抑制剂耐药、脂解调节、p53信号通路和癌症转录错误调节在内的通路也受到URI的调控(图1a)。
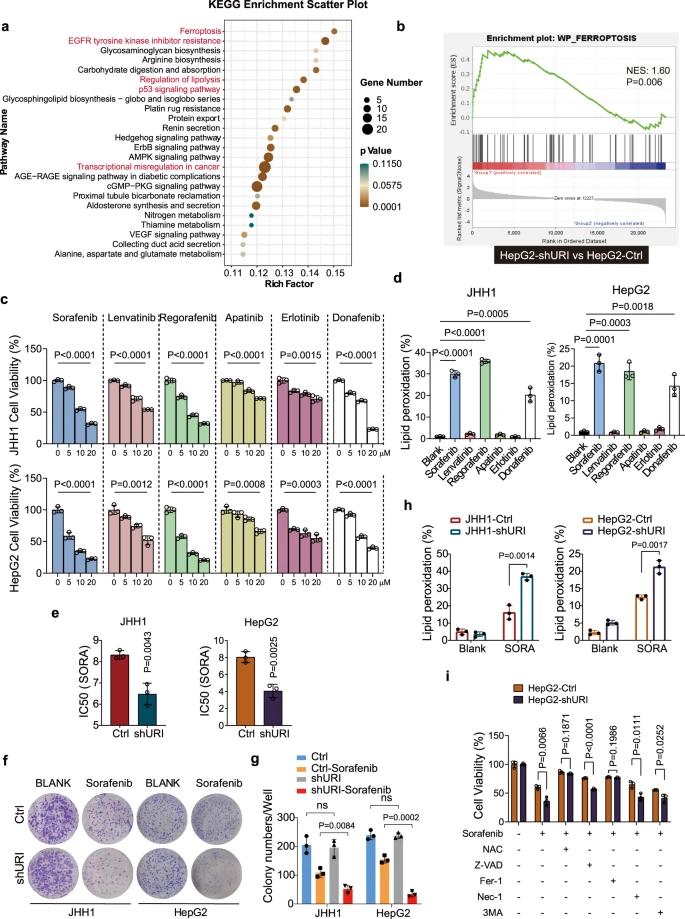
URI耗竭促进TKI诱导的癌细胞铁死亡
已经有许多临床试验评估TKIs治疗晚期肝细胞癌。与细胞毒性作用一致,这些TKIs有效地降低了测试的各种癌细胞系中的肿瘤活力(图1c)。值得注意的是,以B-RAF为共同靶标的索拉非尼,瑞戈非尼和多纳非尼有利于铁死亡样细胞死亡,而其他测试药物对细胞脂质过氧化几乎没有影响(图1d)。
然后,我们测试了URI是否调节TKI诱导的细胞毒性。用增加浓度的索拉非尼处理JHH1和HepG2细胞48小时,并评估细胞增殖。URI耗竭显著增加了JHH1和HepG2细胞对索拉非尼的敏感性,JHH1细胞的IC50(引起50%的活力抑制)从8.324μM(Ctrl)降低到6.480μM(shURI),HepG2细胞的IC50(引起50%的活力抑制)分别从8.047μM(Ctrl)降低到4.069μM(shURI)(图1e)。在HepG2-shURI和对照细胞之间,也发现了对瑞戈非尼或多那非尼的类似剂量效应曲线模式。克隆形成测定证实了URI在索拉非尼耐药中的作用(图1f,g)。有趣的是,JHH1和HepG2细胞中的URI敲低显著增加了索拉非尼诱导的脂质过氧化(图1h),表明URI可能抑制TKI诱导的铁死亡。此外,当用抗氧化剂N-乙酰半胱氨酸(NAC)或铁死亡抑制剂铁抑素-1(Fer-1;脂质过氧化清除剂)预处理时,索拉非尼诱导的URI敲低细胞的细胞毒性作用可以被拯救,而细胞凋亡、坏死或自噬抑制剂几乎没有影响(图1i)。此外,URI耗竭也增强了RSL3(一种GPX4抑制剂)诱导的铁死亡。总之,这些结果表明,URI与肝癌细胞中对TKI诱导的铁死亡的抵抗有关。
研究结论
03
总之,URI以TRIM28-MDM2依赖的方式保持低水平的p53,维持SCD1活性和MUFAs的积累,随后促进癌细胞对TKI的耐药性。URI-p53-SCD1轴介导TKI的抗性,并可能解释为什么p53-野生型HCC仍然显示出对TKI的内在抗性。此外,对于大约41%的野生型p53和高水平URI/SCD1的晚期HCC患者,这里确定的联合治疗可能是一种有希望的策略(图9)。本研究为我们后续的临床试验提供了理论依据。(转化医学网360zhyx.com)
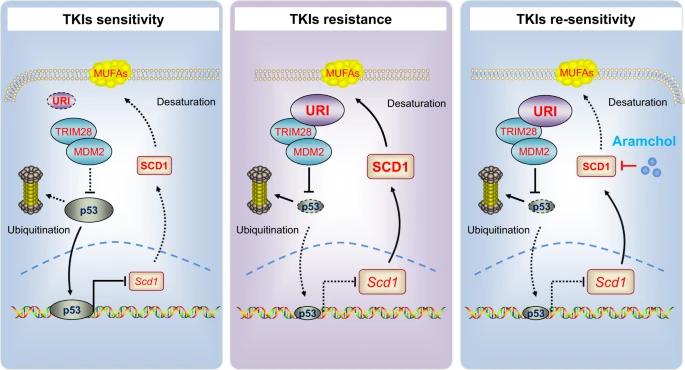
URI-p53-SCD1轴介导TKIs耐药和施用aramchol肝癌细胞对TKIs再敏的模型。
参考资料:
https://onlinelibrary.wiley.com/doi/10.1002/advs.202303378
注:本文旨在介绍医学研究进展,不能作为治疗方案参考。如需获得健康指导,请至正规医院就诊。
 腾讯登录
腾讯登录









还没有人评论,赶快抢个沙发