【Nature子刊】信号通路——助力免疫细胞打通治疗胰腺癌中的路障
| 导读 | 胰腺导管腺癌(PDAC)是最致命的肿瘤,治疗选择有限,5年生存率低至10%,由于侵袭性进展,只有20-30%的PDAC患者在诊断时适合切除,尽管手术切除原发性肿瘤是唯一的治愈性治疗方法。虽然多模式治疗后PDAC患者的生存结局有所改善,但全身治疗的疗效仍然有限,高效疗法的开发是PDAC患者的紧迫问题。 |
胰腺导管腺癌(PDAC)由于侵袭性进展,只有20-30%的PDAC患者在诊断时适合切除,尽管手术切除原发性肿瘤是唯一的治愈性治疗方法。虽然多模式治疗后PDAC患者的生存结局有所改善,但全身治疗的疗效仍然有限,高效疗法的开发是PDAC患者的紧迫问题。免疫检查点阻滞(ICB)彻底改变了癌症治疗,并改善了各种癌症患者的生存结果。然而,PDACs中对ICB的反应令人失望,部分原因是密集的基质作为肿瘤抑制微环境的存在,阻碍了肿瘤血管生成和治疗药物的递送。
近日,来自东京医科齿科大学的研究者们针对实体瘤免疫检查点阻滞(ICB)治疗的局限性做了题为“cGAS-STING signaling encourages immune cell overcoming of fibroblast barricades in pancreatic cancer”的相关研究,并发布在《 Scientific Reports 》杂志上。解释了干扰素基因的环GMP-AMP合酶(cGAS)刺激物(STING)途径是一种先天免疫途径,可导致免疫细胞招募细胞因子和抗肿瘤功效的上调。促浸润信号(如cGAS-STING)和CAF的表征对于击败CAF路障和鼓励PDAC中的免疫细胞浸润至关重要。
 https://www.nature.com/articles/s41598-022-14297-5
https://www.nature.com/articles/s41598-022-14297-5
胰腺导管腺癌
01
胰腺的导管腺癌是胰腺癌的主要肿瘤类型,占80%~90%的胰腺癌应该都是导管腺癌。从病理学角度讲,导管腺癌是指癌的组织里,看到了导管上皮来源的细胞成分,称之为导管腺癌。 胰腺的导管腺癌癌组织中,除了导管上皮细胞成分之外,还有大量的纤维组织。这种纤维组织的存在,造成了胰腺癌血供比较差,化疗药物的进入比较困难,预后也会比较差,治疗效果也不理想。
胰腺导管腺癌(PDAC)是最致命的肿瘤,治疗选择有限,5年生存率低至10%,由于侵袭性进展,只有20-30%的PDAC患者在诊断时适合切除,尽管手术切除原发性肿瘤是唯一的治愈性治疗方法。虽然多模式治疗后PDAC患者的生存结局有所改善,但全身治疗的疗效仍然有限,高效疗法的开发是PDAC患者的紧迫问题。
免疫检查点阻滞
02
免疫检查点阻滞(ICB)彻底改变了癌症治疗,并改善了各种癌症患者的生存结果。然而,PDACs中对ICB的反应令人失望,部分原因是密集的基质作为肿瘤抑制微环境的存在,阻碍了肿瘤血管生成和治疗药物的递送。
环GMP-AMP合酶(cGAS)-STING通路通过诱导型干扰素(IFN)和各种炎症细胞因子的产生来响应细胞质DNA来介导先天免疫。一种连接蛋白STING被环状二核苷酸(CDN)激活,cGAS从细胞质DNA产生,随后激活TANK结合激酶1(TBK1)和干扰素调节转录因子3(IRF3)。IRF3向细胞核的易位上调免疫刺激基因(ISG)和免疫细胞招募细胞因子,随后免疫细胞的活化和迁移,包括树突状细胞(DC),T细胞和自然杀伤(NK)细胞。cGAS-STING通路现在也被认为是调节各种肿瘤免疫力的关键机制。然而,cGAS 和/或 STING 的表达经常丢失或下调,从而导致内在胞质 DNA 介导的先天免疫系统受到抑制。该途径的刺激提供了克服肿瘤的免疫抑制环境并使患者对ICB治疗敏感的能力。
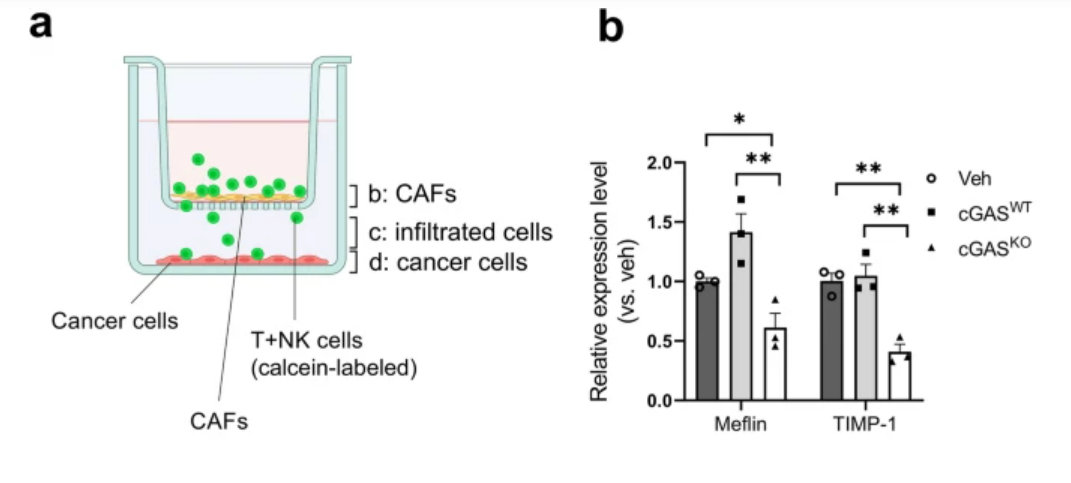
表达cGAS-STING的肿瘤显示出肿瘤抑制性CAFs的标志物升高,以及抗肿瘤免疫细胞在组织基质成分中的强浸润。此外,Transwell共培养实验表明,CAFs的存在减弱了免疫细胞对癌细胞的浸润,但通过激活cGAS-STING信号传导而被废除。这些结果表明,肿瘤中cGAS-STING信号传导的互补将是击败PDACs中CAF路障的有希望的治疗策略。
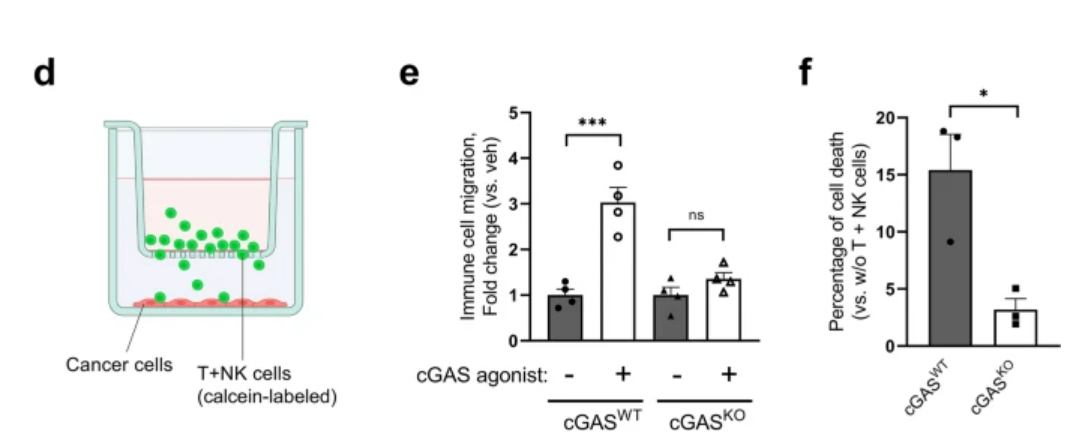 cGAS-STING通路
cGAS-STING通路
03
在90%的PDAC病例中观察到STING表达,在cGAS和STING双表达肿瘤中PDAC患者的总生存率更高;在cGAS-STING双阳性组织中,细胞毒性CD8 +细胞从基质到癌组织持续浸润,并且它们含有更多的rCAFs;在共培养系统中,cGAS-STING信号传导通过维持CAF的rCAF特性来促进免疫细胞浸润和随后的癌细胞死亡.
cGAS-STING信号传导的丢失会减弱rCAFs的特征。然而,目前尚不清楚这是否是由于cGAS的直接影响,募集免疫细胞的间接作用。需要进一步的研究来揭示确定CAF特征的机制,包括cGAS-STING信号传导。
由于丰富的基质的存在是PDAC中的潜在屏障并降低ICB的疗效,因此建立靶向肿瘤促进CAF的治疗策略是一项重大挑战。我们证明了cGAS-STING信号传导的激活对于免疫细胞浸润以及CAFs的特征是重要的。异源CAFs的进一步表征和cGAS-STING信号传导的互补将鼓励免疫细胞克服CAF,这最终可以提高PDAC对IB的敏感性.(转化医学网360zhyx.com)
参考资料:
https://www.nature.com/articles/s41598-022-14222-w
注:本文旨在介绍医学研究进展,不能作为治疗方案参考。如需获得健康指导,请至正规医院就诊。
 腾讯登录
腾讯登录









还没有人评论,赶快抢个沙发