抑癌?促癌?这个蛋白还有两副面孔!
| 导读 | 乳腺癌是最常见的女性恶性肿瘤之一,数据显示50%的患者在治疗后5年内出现复发导致治疗失败,其中远处转移是乳腺癌患者的主要死亡原因。 |

乳腺癌是最常见的女性恶性肿瘤之一,数据显示50%的患者在治疗后5年内出现复发导致治疗失败,其中远处转移是乳腺癌患者的主要死亡原因。现今,由于乳腺癌转移机制的特殊性,如何根据乳腺癌的转移情况进行精准治疗已经成为相关研究的一大难题。
近日,美国约翰霍普金斯大学的研究人员发现常见细胞“粘合剂”——E-钙粘蛋白(E-cad)对乳腺癌转移“功不可没”。他们指出在乳腺侵袭性导管癌中,E-cad可限制癌细胞内的分子应力,使细胞在转移后继续存活并形成新的肿瘤!而E-cad又是公认的可以限制肿瘤转移的分子,难道这个蛋白竟然有两副面孔?

抑癌——“绑住”癌细胞
E-cad是一种同亲型结合、Ca依赖的细胞粘着糖蛋白,是参与细胞间粘附连接的主要分子,发挥着维持细胞极性和组织结构完整性的功能。癌症的发展和转移皆牵涉了E-cad功能的表达或缺失,包括转录阻遏、表观遗传沉默、失活突变、增强退化、内吞作用和蛋白水解裂解。E-cad的功能缺失可降低肿瘤组织中细胞粘附的强度,导致细胞活动性增加,允许癌细胞穿过基底膜,获得分化和高侵袭性。
同时,E-cad的下调是上皮间质转化(EMT)的显著性特征,而EMT是肿瘤恶性表型的重要标志。换言之,E-cad就是一条将癌细胞“绑”于局部组织中的“绳索”,当“绳索”被切断(E-cad功能不足),癌细胞就挣脱了束缚,开始了转移之旅。
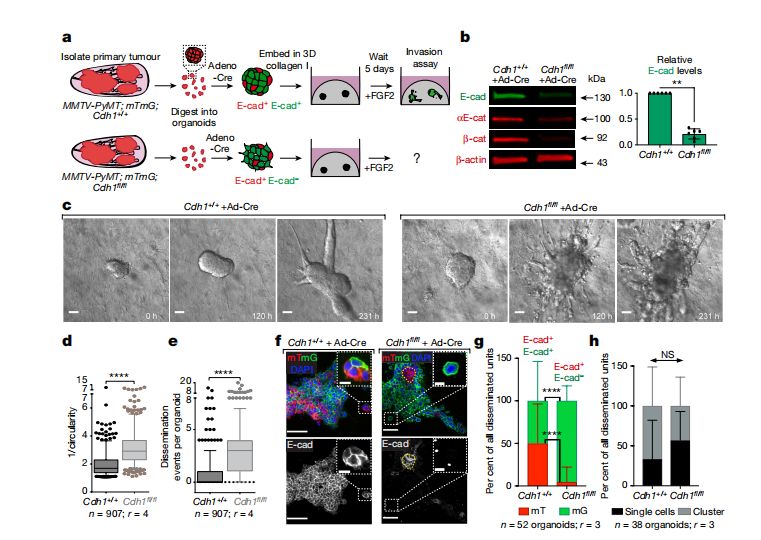
E-cad缺失增强癌细胞侵袭性
但是,研究人员发现,在占乳腺癌极高比例的亚型——侵袭性导管癌患者中,无论是原发灶还是转移灶,都有不少E-cad表达。他们使用了管腔和基底浸润性导管癌的小鼠模型,发现减少E-cad表达的确可以显著增强癌细胞的侵袭性,也就是说E-cad“抑癌”的结论并没有错。那为什么侵袭性导管癌中E-cad的表达没受到限制呢?
促癌——癌细胞的“保护伞”
在小鼠实验中,研究人员有了出乎意料的发现——E-cad竟然可以促进侵袭性导管癌的转移!结果显示,E-cad缺失后,肿瘤细胞离开原发灶不久就大量死亡。侥幸未死亡的肿瘤细胞也没有形成新肿瘤灶的能力,而仍有E-cad活性的肿瘤细胞则成功转移定植。这就意味着E-cad是乳腺侵袭性导管癌转移的关键。
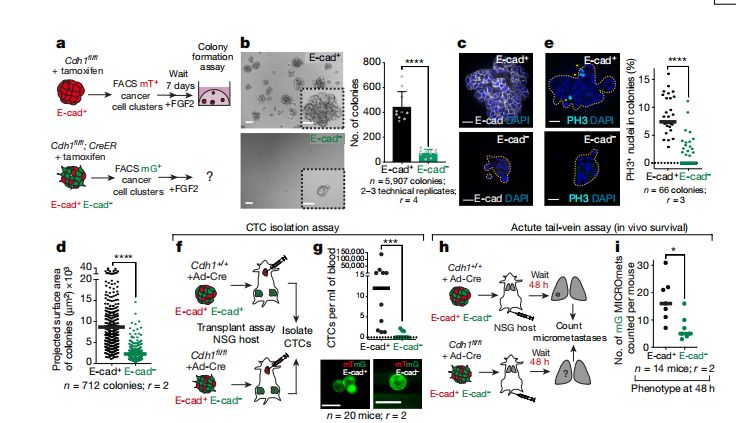
E-cad功能缺失抑制肿瘤转移
进一步的研究发现,E-cad的功能缺失虽可引发肿瘤侵袭,却也同时导致癌细胞的增殖和存活受到严重限制,使得循环肿瘤细胞数量显著下降,进而遏制了癌细胞的繁殖和转移生长。
E-cad功能缺失可上调TGF-β、活性氧浓度和凋亡信号传导途径基因的表达,进而引发SMAD2/3蛋白的核富集,导致氧化应激和细胞凋亡的增加。也就是说,E-cad正是通过限制活性氧介导的细胞凋亡成为了癌细胞名副其实的“保护伞”。
总而言之,在乳腺侵袭性导管癌中,E-cad是一把双刃剑,当其需要转移时,E-cad的表达会受限,但并未完全消失,从而赋予癌细胞侵袭能力。在“解放”了癌细胞后,E-cad又化身为癌细胞的“守护神”,保证癌细胞转移的“一路平安”。这就提示若能进一步掌握E-cad作用的时相,在相应的时间内控制E-cad的功能,也许能为转移性乳腺癌患者带来一线生机。(转化医学网360zhyx.com)
参考文献:
Veena Padmanaban, et al.E-cadherin is required for metastasis in multiple models of breast cancer.Nature (2019).

 腾讯登录
腾讯登录







还没有人评论,赶快抢个沙发