一针治癌!一日两文同登《Nature》,揭开癌症疫苗绝杀“冷肿瘤”之谜!
| 导读 | WHO国际癌症研究机构(IARC)发布的数据显示,仅2018年一年,世界范围内新增了1810万病例癌症患者,死亡人数高达960万。不难想象,不远的将来,癌症将成为全球头号杀手,“谈癌色变”早非杞人忧天,尤其是一些死亡率极高、预后极差的“冷肿瘤”,更是人类健康的巨大威胁 |
WHO国际癌症研究机构(IARC)发布的数据显示,仅2018年一年,世界范围内新增了1810万病例癌症患者,死亡人数高达960万。不难想象,不远的将来,癌症将成为全球头号杀手,“谈癌色变”早非杞人忧天,尤其是一些死亡率极高、预后极差的“冷肿瘤”,更是人类健康的巨大威胁,如何铲除癌症这一拦路虎是全世界科学家必须面对的难题。12月19日,两篇文章同登著名学术期刊《Nature》,美德科学家竟分别研制出了癌症疫苗,成功完成了I期临床试验,实现了对“冷肿瘤”的绝杀!一针治癌的时代,是否将临?

什么是“冷肿瘤”?
我们知道,多数肿瘤细胞表面存在因基因突变产生的新抗原,机体免疫系统正是通过识别这些抗原来准确“铆定”肿瘤细胞,进而发生免疫反应,杀灭肿瘤。肿瘤自然也不会坐以待毙,PD-1/PD-L1等免疫检查点就是肿瘤自我掩护,抑制T细胞、NK细胞功能的“秘密武器”。魔高一尺道高一丈,科学家多年研究下,免疫检查点抑制剂应运而生,成了攻克多数癌症的“生物导弹”,效果之佳令人雀跃。但是,既然免疫检查点抑制剂面向的是“多数”癌症,那就存在可在“生物导弹”下安然无恙的肿瘤,它们就是“冷肿瘤”。
为什么说这些肿瘤“冷”呢?
肿瘤因突变而生,突变的多寡就决定了肿瘤细胞表面新抗原的多少。对免疫检查点抑制剂无动于衷的肿瘤本身突变较少,本就难以吸引足够的免疫细胞浸润,而免疫检查点抑制剂是通过解除肿瘤对免疫系统的“蒙蔽”,让免疫系统恢复对肿瘤的识别和杀伤能力,“解放”后的免疫细胞对这些表面抗原不足的肿瘤细胞根本无法有效识别,更谈不上将其消灭,所以“生物导弹”便失去了无用武之地。“冷肿瘤”中的翘楚,就是生存率仅为30%的胶质母细胞瘤。
让“冷肿瘤”“变热”
想要“唤醒”“冷肿瘤”,最重要的事情就是让其“变热”,也就是让肿瘤细胞表面有足够的抗原,才能有效激活免疫系统。怎样“变热”呢?总不能让肿瘤发生更多突变吧,突变的不可控性让科学家们瑟瑟发抖,直接排除了这一想法。既然增加抗原的路行不通,那么提升免疫细胞对肿瘤抗原的识别能力就是当务之急了,而癌症疫苗就是实现目标的最佳途径。
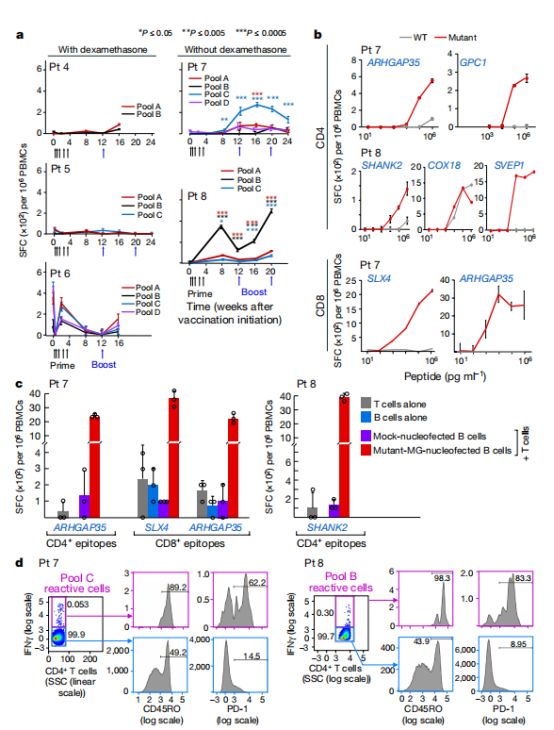
癌症疫苗诱导循环中的新抗原特异性T细胞应答
肿瘤疫苗的奇效
肿瘤表面抗原少?没关系,打一针足够唤醒免疫系统的相似抗原入体,只要免疫系统苏醒,肿瘤自然无处可逃,这就是癌症疫苗。德国海德堡大学附属医院的研究人员用从预制抗原文库中提取的癌症疫苗和根据患者癌症相关突变定制的个性化疫苗对新诊断的胶质母细胞瘤患者进行了治疗,结果显示15名患者的无进展生存期(PFS)达到了14.2个月!
患者最长生存期甚至超过了38.9个月!同时,美国波士顿达纳-法伯癌症研究所的研究人员用个性化的新抗原靶向疫苗治疗III到V级的胶质母细胞瘤患者,没使用过地塞米松的患者PFS也达到了16.8个月!这就意味着癌症疫苗在“冷肿瘤”的治疗中取得了重要成就!
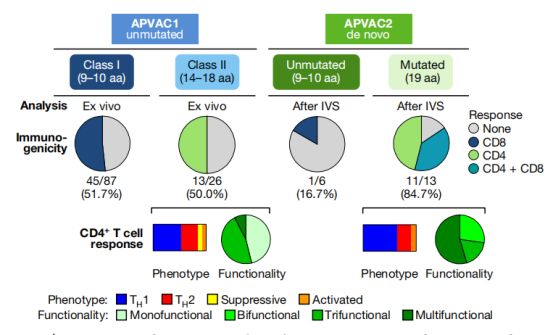
预制抗原文库中提取的癌症疫苗诱导的免疫反应
如何一针治癌?
研究人员发现,癌症疫苗可激活循环中的T细胞,让其进入大脑,实现最大程度地杀灭胶质母细胞瘤。从预制抗原文库中提取的癌症疫苗可以使机体产生CD8+T细胞的免疫应答,导致血液中相应的特异性CD8+T细胞数量增加,出现记忆表型,而个性化疫苗则主要使机体产生新抗原特异性CD4+T细胞的Th1型应答。正是这些被唤醒的免疫反应,让“冷肿瘤”彻底“变热”,进而被强力扼杀。
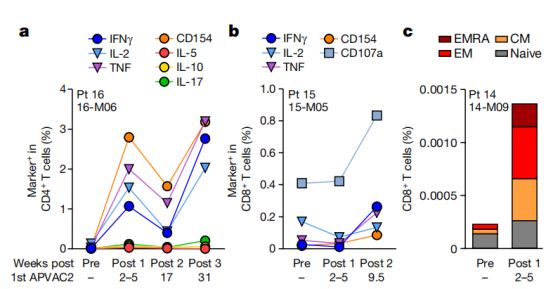
个性化疫苗主要诱导新抗原特异性CD4+T细胞的Th1型应答
仍有忧愁,仍需努力
虽然两项研究成果令人振奋,但最终大多数参与治疗的患者皆死于癌症。究其缘由或是因为体内被唤醒的免疫细胞已被耗尽,才会导致癌症再次复发。因此,联合疗法将是未来癌症疗法的关键,如何在唤醒免疫系统的同时长期保证免疫系统的活性,将是研究人员接下来必须克服的难题。万事开头难,既然已有方向,相信未来之途会逐渐顺遂,会有更多好消息等着我们。
参考文献:
1.Immune cells track hard-to-target brain tumours
2.Norbert Hilf,et al.Actively personalized vaccination trial for newly diagnosed glioblastoma.Nature (2018)
3.Derin B. Keskin,et al.Neoantigen vaccine generates intratumoral T cell responses in phase Ib glioblastoma trial
(转化医学网360zhyx.com)
 腾讯登录
腾讯登录









还没有人评论,赶快抢个沙发