CRISPR换乘新工具直冲临床!Nature Biotechnology重磅报导纳米递送实现“安全运载”!
| 导读 | 更高的编辑效率,更有效的递送方式。这两者无疑是大多数基因编辑科学家最基本的追求。目前,最常用的基因编辑递送系统则是以腺伴随病毒(AAV)为代表的病毒递送系统。 |

更高的编辑效率,更有效的递送方式。这两者无疑是大多数基因编辑科学家最基本的追求。目前,最常用的基因编辑递送系统则是以腺伴随病毒(AAV)为代表的病毒递送系统。

AAV的缺陷
昨天,一篇发表于Nature Biotechnology 杂志研究所指出的,理想的CRISPR-Cas9传递系统应该限制细胞暴露于基因组编辑技术体系的时间,以便将潜在的脱靶效应降至最低。此外,spCas9(化脓性链球菌Streptococcus pyogenes,Cas9)难以适应具有强启动子的典型AAV构建体,同时,患者对AAV衣壳的免疫反应也会在一定程度上限制重复给药,从而最终影响以AAV为递送的临床基因编辑治疗疗效。而在这篇研究中,MIT科学家则在这篇文章中着手解决了这些问题和挑战,文章名为Structure-guided chemical modification of guide RNA enables potent non-viral in vivo genome editing。

sgRNA的化学修饰。
e-sgRNA:加强的单链向导RNA
为了应对这些挑战,MIT科学家开发了一种全新的非病毒传递系统。他们确定了一个特定的单链向导RNA(sgRNA)区域。在对sgRNA的这一部分进行化学修饰后,sgRNA与Cas9蛋白的相互作用并不会得到抑制。研究人员通过对这一区域的化学修饰增强基因组编辑的总体效率。
随后,研究人员实验验证了单剂量的增强sgRNA(e-sgRNA)Cas9 mRNA复合体能够在活体小鼠的肝细胞中对靶基因进行有效编辑。
至此,研究人员便开始通过对sgRNA结构的进一步分析来寻找那些不会影响其与Cas9蛋白结合的可修饰区域。他们设计了稳定表达GFP和spCas9的HEK293细胞株,并通过插入缺失标记引入了一种功能性sgRNA,从而消除了GFP的表达。研究人员指出,这个实验能够帮助人们确定sgRNA对哪些具体的化学修饰具有良好的耐受性以及CRISPR/Cas9的编辑能力将如何受到化学修饰的影响。
研究人员可以通过对未修饰sgRNA靶向GFP与他们自己开发的“增强”化学修饰sgRNA的比较来确定对sgRNA的特定修饰是否能够提高CRISPR/Cas9系统的编辑效率。
“我们将Cas9 mRNA和这种修饰后的sgRNA同时被递送至稳定表达GFP的HEK293细胞中,实验结果表明这种e-sgRNA产生的编辑效率显着高于5'和3'-sgRNA以及天然sgRNA的编辑效率(43%,22%和20%)。”文章作者写道。
纳米颗粒提送系统
随后,研究人员将GFP靶向的不同sgRNA制成了脂质纳米颗粒(LNP),并通过静脉注射将包裹后的sgRNA脂质纳米颗粒传送到了组成性表达Cas9和GFP(Cas9-2A-GFP)的小鼠肝脏中。
研究人员指出,在单次注射后,未修饰的GFP-sgRNA在肝脏组织细胞GFP基因座处能够引起约5%的编辑,相比之下,5'和3'修饰sgRNA的编辑率则约为22%,而e-sgRNA治疗则能够导致约46%的甚至显着更高编辑率。在两次同剂量的LNP包被e-sgRNA治疗后,小鼠肝脏细胞中的GFP基因编辑比率增加到了77%。
非病毒递送系统的临床潜力
为了评估非病毒递送e-sgRNA编辑系统对于活体靶向病治疗的潜能,研究小组设计了两种靶向小鼠Pcsk9基因的e-sgRNA,Pcsk9基因是治疗家族性高胆固醇血症的重要靶标。他们将Cas9 mRNA和两种e-sgRNA包裹在LNP中,发现小鼠在单次静脉给药5天后的血清Pcsk9几乎检测不到,总胆固醇率也会同时发生35%-40%的降低。
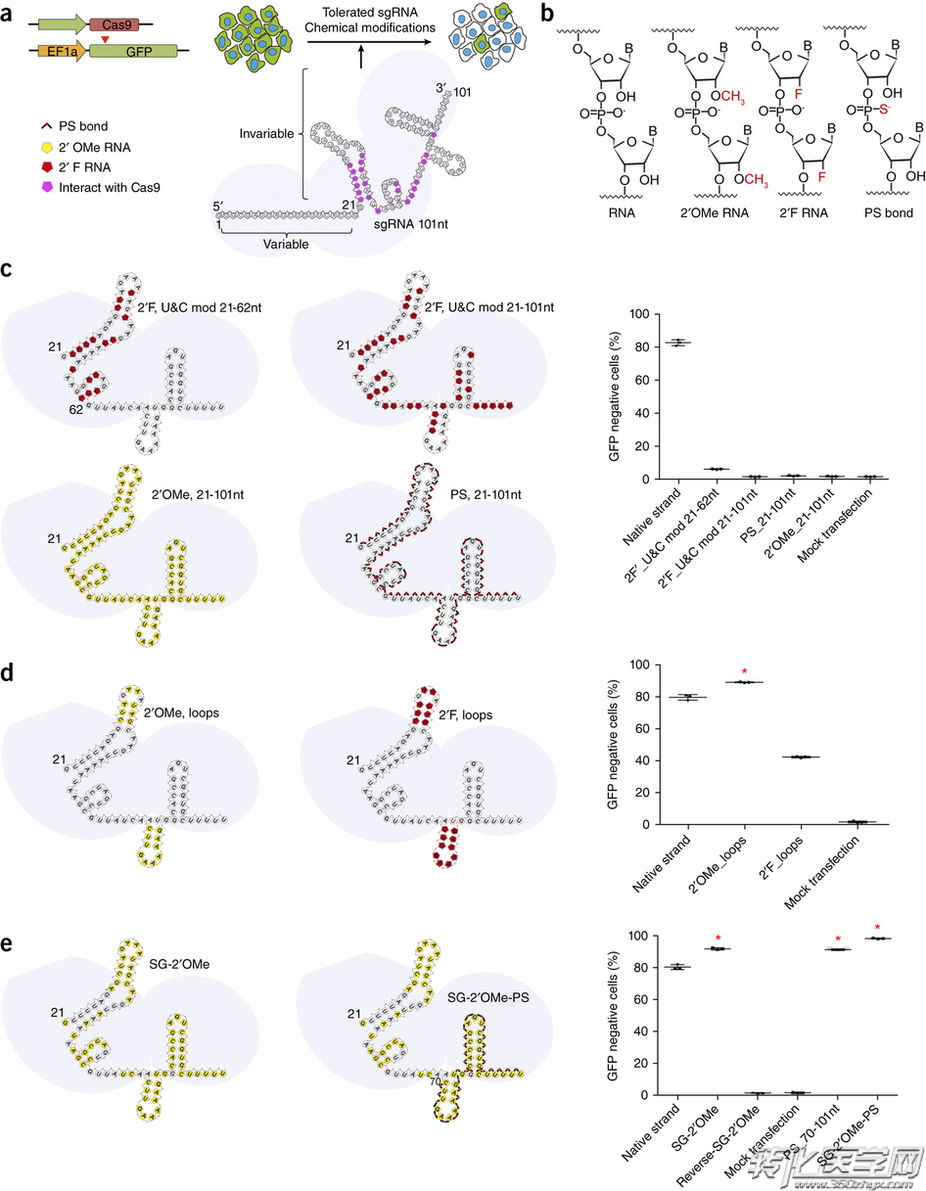 sgRNA不变部分的化学修饰。
sgRNA不变部分的化学修饰。
研究人员写道:“我们在这些小鼠的肝脏基因组DNA中发现了总计约83%(±3%)的编辑事件,其中包括小的indels,两个sgRNA引起的主要基因组缺失以及较低水平的倒位。”

化学修饰的sgRNA和Cas9 mRNA的体内递送诱导小鼠肝脏中靶向基因的敲除
除此之外,研究人员还对这种新型基因编辑递送系统在肺脏和脾脏细胞中的基因编辑效率进行了比较,进一步确定了Pcsk9基因经过靶向Cas9和e-sgRNA处理后可能会出现的脱靶事件。研究结果表明e-sgRNACas9系统在肝脏细胞中的脱靶几乎检测不到,具有极强的组织特异性。
“鉴于非病毒传递系统的潜在优势,非病毒基因组编辑在治疗环境中更具吸引力,包括易于扩大规模,定制速度快,不需要额外的免疫抑制并且能够限制核算暴露于基因编辑系统的时间。”研究人员总结说。 “除了e-sgRNA的潜在治疗应用外,我们预计高度修饰的sgRNA还可以整合到一系列CRISPR相关技术中,如CRISPR介导的成像,活化和靶基因抑制。”
“我们相信,纳米粒子递送系统对活体动物基因组的编辑能够为CRISPR/Cas9基因编辑技术的临床转化打开一扇新的大门,进一步推动了CRISPR/Cas9基因组编辑系统的实用性。”研究人员表示。
原文:Structure-guided chemical modification of guide RNA enables potent non-viral in vivo genome editing
Nature Biotechnology doi:10.1038/nbt.4005
(转化医学网360zhyx.com)
 腾讯登录
腾讯登录









还没有人评论,赶快抢个沙发