Autophagy|拦截肿瘤的“脂肪消耗指令”:山东大学陈安静/王建波揭示放疗如何通过“特洛伊木马”远程分解脂肪,并找到阻断键
| 导读 | 2026年4月16日,山东大学陈安静和王建波共同通讯在Autophagy 在线发表题为“PBK-Loaded secretory autophagosomes drive radiotherapy-induced systemic adipose depletion via MAPK/ERK-PRKA/PKA-LIPE/HSL signaling: a therapeutic target for esophageal cancer cachexia”的研究论文 |
放疗虽然是食管鳞状细胞癌(ESCC)的基石性治疗方法,但矛盾的是,它与显著的体重下降相关,这预示着患者预后不良。驱动这种代谢并发症的机制仍不清楚。
2026年4月16日,山东大学陈安静和王建波共同通讯在Autophagy 在线发表题为“PBK-Loaded secretory autophagosomes drive radiotherapy-induced systemic adipose depletion via MAPK/ERK-PRKA/PKA-LIPE/HSL signaling: a therapeutic target for esophageal cancer cachexia”的研究论文。该研究确定脂肪耗竭——而非肌肉萎缩——是ESCC放疗诱导的体重下降的主要因素。通过整合的体外和体内研究,作者证明放疗后释放的分泌性自噬体(SAPs)介导了全身性的脂肪丢失。蛋白质组学分析揭示放疗诱导的SAPs中富集了PBK(PDZ结合激酶),功能研究确定PBK是脂肪细胞脂解的主要调节因子。
在机制上,SAP递送的PBK激活了MAPK1/ERK2(丝裂原活化蛋白激酶1),触发下游PRKA/PKA-LIPE/HSL信号级联反应,从而增加脂解速率。临床上,在一个ESCC队列中,循环SAPs水平升高预示着严重的脂肪丢失和中位生存期缩短。关键的是,在临床前模型中,使用OTS-514对PBK进行药理学抑制可恢复脂肪质量,同时增强肿瘤的放射敏感性。作者的工作将放疗诱导的恶病质重新定义为由SAPs orchestrates的以脂肪为中心的过程,揭示了PBK作为治疗靶点,并为早期干预提供了可操作的生物标志物。这些发现弥合了局部放疗与全身性代谢后遗症之间的差距,为提高ESCC患者的生存率和生活质量提供了一种双重策略方法。
 食管癌仍然是全球范围内的一个重大公共卫生挑战,每年估计有604,000例新诊断病例和544,000例死亡报告。这种恶性肿瘤主要分为两种组织学类型:食管腺癌(EAC)和食管鳞状细胞癌(ESCC),后者占全球所有病例的近85%。其中,ESCC以其快速进展和与癌症相关恶病质的强关联性而著称——恶病质是一种多因素代谢综合征,其特征为持续性体重下降、显著的脂肪耗竭和骨骼肌丢失。恶病质影响50-80%的晚期ESCC患者,严重损害治疗疗效和长期生存。尽管恶病质在历史上被认为与肿瘤引起的吞咽困难有关,但最近的研究强调全身性炎症和代谢失调是主要因素。
食管癌仍然是全球范围内的一个重大公共卫生挑战,每年估计有604,000例新诊断病例和544,000例死亡报告。这种恶性肿瘤主要分为两种组织学类型:食管腺癌(EAC)和食管鳞状细胞癌(ESCC),后者占全球所有病例的近85%。其中,ESCC以其快速进展和与癌症相关恶病质的强关联性而著称——恶病质是一种多因素代谢综合征,其特征为持续性体重下降、显著的脂肪耗竭和骨骼肌丢失。恶病质影响50-80%的晚期ESCC患者,严重损害治疗疗效和长期生存。尽管恶病质在历史上被认为与肿瘤引起的吞咽困难有关,但最近的研究强调全身性炎症和代谢失调是主要因素。
在肿瘤微环境中,ESCC细胞释放促炎细胞因子(例如IL-6、TNF/TNF-α),通过刺激脂解通路触发脂肪组织分解代谢。此过程中的一个关键酶是LIPE/HSL(脂肪酶E,激素敏感型),其活性通过涉及MAPK/ERK(丝裂原活化蛋白激酶)和PRKA/PKA(cAMP依赖性蛋白激酶)的信号级联反应进行调节。重要的是,在ESCC相关恶病质的进展中,脂肪组织耗竭发生在肌肉降解之前,这强调了脂解作为一个潜在的治疗靶点。
放疗(RT)是ESCC治疗的基石,却矛盾地通过全身性“远隔效应”加剧恶病质。放疗诱导的远隔效应(RIAEs)于1953年首次被描述,涵盖了超出照射肿瘤场之外的远处代谢改变。临床研究报告显示,40.3%的ESCC患者出现放疗相关的体重下降,其特征为加速的脂解和肌肉分解代谢。虽然RIAEs部分由放疗触发的免疫原性细胞死亡和炎症因子释放介导,但最近的研究确定细胞外囊泡(EVs)是传播代谢紊乱的关键载体。EVs——特别是小EVs(sEVs)和新近被表征的分泌性自噬体(SAPs)——将肿瘤来源的货物(例如蛋白质、miRNA)运输到远处的脂肪库。SAPs以MAP1LC3/LC3表面标志物和自噬体起源为特征,在放疗诱导的应激下优先释放,并参与全身性代谢失调。然而,放疗诱导的SAPs分泌与脂肪消耗之间的联系机制仍未得到探索。
原文链接:
https://doi.org/10.1080/15548627.2026.2661313
iNature汇集了4万名生命科学的研究人员及医生。我们组建了80个综合群(16个PI群及64个博士群),同时更具专业专门组建了相关专业群(植物,免疫,细胞,微生物,基因编辑,神经,化学,物理,心血管,肿瘤等群)。温馨提示:进群请备注一下(格式如学校+专业+姓名,如果是PI/教授,请注明是PI/教授,否则就直接默认为在读博士,谢谢)。可以先加小编微信号(love_iNature),或者是长按二维码,添加小编,之后再进相关的群,非诚勿扰。
2026年4月16日,山东大学陈安静和王建波共同通讯在Autophagy 在线发表题为“PBK-Loaded secretory autophagosomes drive radiotherapy-induced systemic adipose depletion via MAPK/ERK-PRKA/PKA-LIPE/HSL signaling: a therapeutic target for esophageal cancer cachexia”的研究论文。该研究确定脂肪耗竭——而非肌肉萎缩——是ESCC放疗诱导的体重下降的主要因素。通过整合的体外和体内研究,作者证明放疗后释放的分泌性自噬体(SAPs)介导了全身性的脂肪丢失。蛋白质组学分析揭示放疗诱导的SAPs中富集了PBK(PDZ结合激酶),功能研究确定PBK是脂肪细胞脂解的主要调节因子。
在机制上,SAP递送的PBK激活了MAPK1/ERK2(丝裂原活化蛋白激酶1),触发下游PRKA/PKA-LIPE/HSL信号级联反应,从而增加脂解速率。临床上,在一个ESCC队列中,循环SAPs水平升高预示着严重的脂肪丢失和中位生存期缩短。关键的是,在临床前模型中,使用OTS-514对PBK进行药理学抑制可恢复脂肪质量,同时增强肿瘤的放射敏感性。作者的工作将放疗诱导的恶病质重新定义为由SAPs orchestrates的以脂肪为中心的过程,揭示了PBK作为治疗靶点,并为早期干预提供了可操作的生物标志物。这些发现弥合了局部放疗与全身性代谢后遗症之间的差距,为提高ESCC患者的生存率和生活质量提供了一种双重策略方法。

在肿瘤微环境中,ESCC细胞释放促炎细胞因子(例如IL-6、TNF/TNF-α),通过刺激脂解通路触发脂肪组织分解代谢。此过程中的一个关键酶是LIPE/HSL(脂肪酶E,激素敏感型),其活性通过涉及MAPK/ERK(丝裂原活化蛋白激酶)和PRKA/PKA(cAMP依赖性蛋白激酶)的信号级联反应进行调节。重要的是,在ESCC相关恶病质的进展中,脂肪组织耗竭发生在肌肉降解之前,这强调了脂解作为一个潜在的治疗靶点。
放疗(RT)是ESCC治疗的基石,却矛盾地通过全身性“远隔效应”加剧恶病质。放疗诱导的远隔效应(RIAEs)于1953年首次被描述,涵盖了超出照射肿瘤场之外的远处代谢改变。临床研究报告显示,40.3%的ESCC患者出现放疗相关的体重下降,其特征为加速的脂解和肌肉分解代谢。虽然RIAEs部分由放疗触发的免疫原性细胞死亡和炎症因子释放介导,但最近的研究确定细胞外囊泡(EVs)是传播代谢紊乱的关键载体。EVs——特别是小EVs(sEVs)和新近被表征的分泌性自噬体(SAPs)——将肿瘤来源的货物(例如蛋白质、miRNA)运输到远处的脂肪库。SAPs以MAP1LC3/LC3表面标志物和自噬体起源为特征,在放疗诱导的应激下优先释放,并参与全身性代谢失调。然而,放疗诱导的SAPs分泌与脂肪消耗之间的联系机制仍未得到探索。

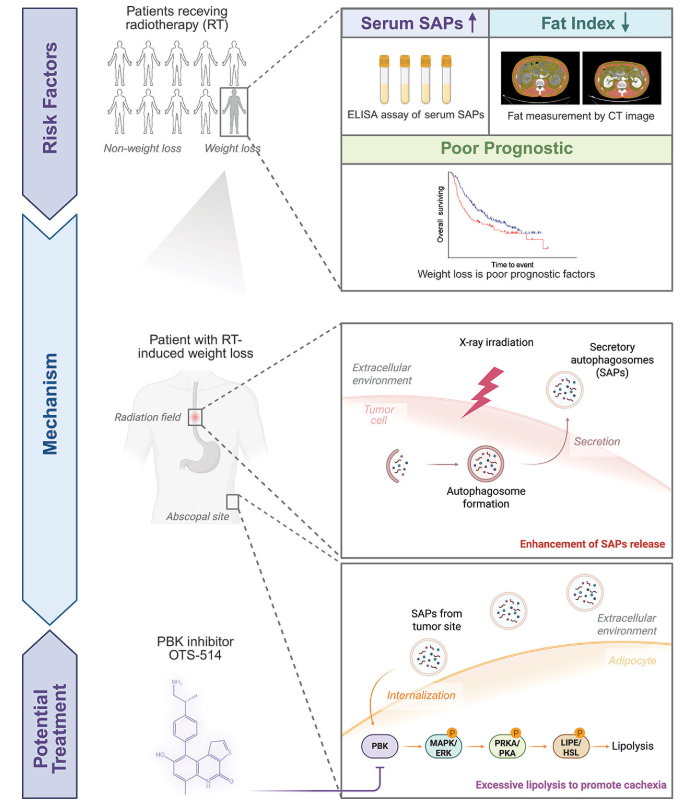
模式机理图(图片源自Autophagy )
在本研究中,作者通过临床和机制研究解决了这一知识空白。对接受根治性放疗的ESCC患者的纵向分析揭示,进行性脂肪丢失是恶病质的主要因素。对受照射ESCC细胞来源的SAPs进行的蛋白质组学分析鉴定出PBK(PDZ结合激酶)作为一种放疗诱导的货物蛋白。使用遗传学和药理学方法,作者证明富含PBK的SAPs激活脂肪细胞中的MAPK-PRKA-LIPE脂解轴,驱动远隔脂肪耗竭。此外,作者建立了一个循环SAPs定量系统作为放疗诱导恶病质的预测性生物标志物,并验证了PBK抑制作为一种可行的治疗策略。这些发现重新定义了作者对放疗全身性代谢后果的理解,同时提出了可行的临床干预措施。原文链接:
https://doi.org/10.1080/15548627.2026.2661313
—END—
内容为【iNature】公众号原创,
转载请写明来源于【iNature】
微信加群iNature汇集了4万名生命科学的研究人员及医生。我们组建了80个综合群(16个PI群及64个博士群),同时更具专业专门组建了相关专业群(植物,免疫,细胞,微生物,基因编辑,神经,化学,物理,心血管,肿瘤等群)。温馨提示:进群请备注一下(格式如学校+专业+姓名,如果是PI/教授,请注明是PI/教授,否则就直接默认为在读博士,谢谢)。可以先加小编微信号(love_iNature),或者是长按二维码,添加小编,之后再进相关的群,非诚勿扰。


投稿、合作、转载授权事宜
请联系微信ID:Love_iNatures
 腾讯登录
腾讯登录







还没有人评论,赶快抢个沙发