从抗菌肽到新肺癌驱动基因!复旦中山医院胸外科蒋伟/梁嘉琪团队揭示 DEFB1 新功能与靶向治疗潜力
| 导读 | 该研究通过全基因组CRISPR筛选、多组学整合分析及抗体转化研究,首次系统揭示抗菌肽DEFB1在肺腺癌中的致癌作用,并开发出具有显著抗肿瘤活性的抗DEFB1单克隆抗体,为肺腺癌治疗提供了全新靶点与策略。 |
近日,复旦大学附属中山医院胸外科蒋伟/梁嘉琪团队在肺腺癌研究领域取得重要进展,发表题为《Unveiling DEFB1 as a Novel Driver and Promising Therapeutic Target in Lung Adenocarcinoma》的研究论文。该研究通过全基因组CRISPR筛选、多组学整合分析及抗体转化研究,首次系统揭示抗菌肽DEFB1在肺腺癌中的致癌作用,并开发出具有显著抗肿瘤活性的抗DEFB1单克隆抗体,为肺腺癌治疗提供了全新靶点与策略。
从全基因组筛选出发:锁定肺腺癌新驱动基因 DEFB1
肺腺癌是最常见的肺癌亚型之一,但仍有大量患者缺乏有效靶向治疗。为寻找新的致癌驱动因子,研究团队开展了体内外全基因组CRISPR/Cas9敲除筛选,并结合TCGA生存数据进行交叉分析,最终筛选出15个潜在关键基因,其中DEFB1因其新颖性和潜在功能脱颖而出。进一步单细胞测序分析发现,DEFB1主要在肿瘤上皮细胞中高表达;多重免疫组化队列验证其在肿瘤组织中显著上调;TCGA与GEO数据进一步证实DEFB1高表达与不良预后密切相关,并在多因素分析中表现为独立预后因子。这些结果首次提示,传统抗菌肽DEFB1可能具有明确的肿瘤驱动功能。
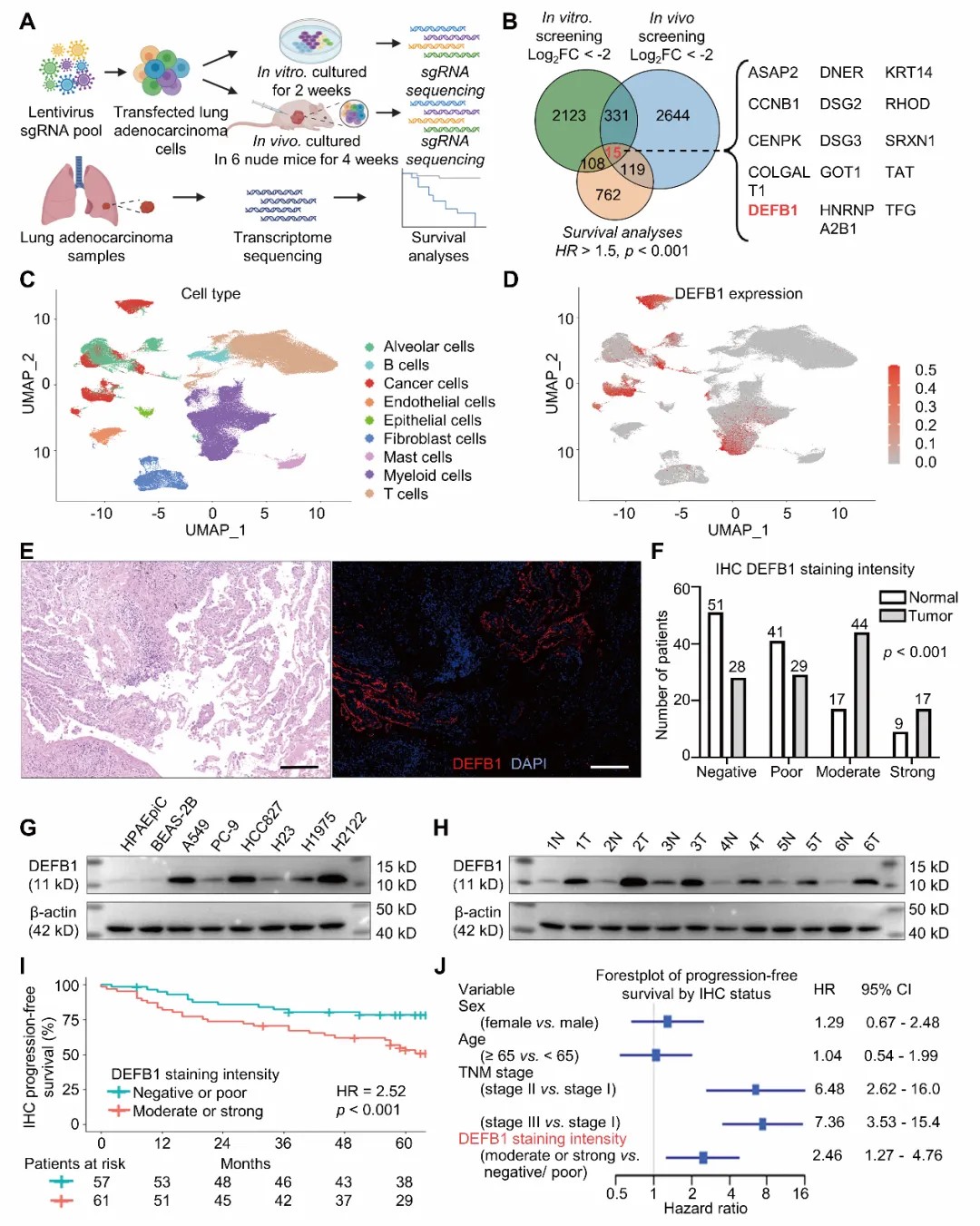
功能验证:DEFB1显著促进肿瘤恶性表型
在功能验证层面,研究团队通过CRISPR敲除、回补表达及外源蛋白补充等策略系统评估DEFB1作用。结果显示,敲除DEFB1可显著抑制肺腺癌细胞增殖,而重新表达或外源添加DEFB1可恢复其增殖能力;同时细胞迁移与侵袭能力明显下降,小鼠异种移植瘤体积显著减小。这些结果提示,DEFB1不仅是相关分子,更是具有明确功能的致癌驱动因子。
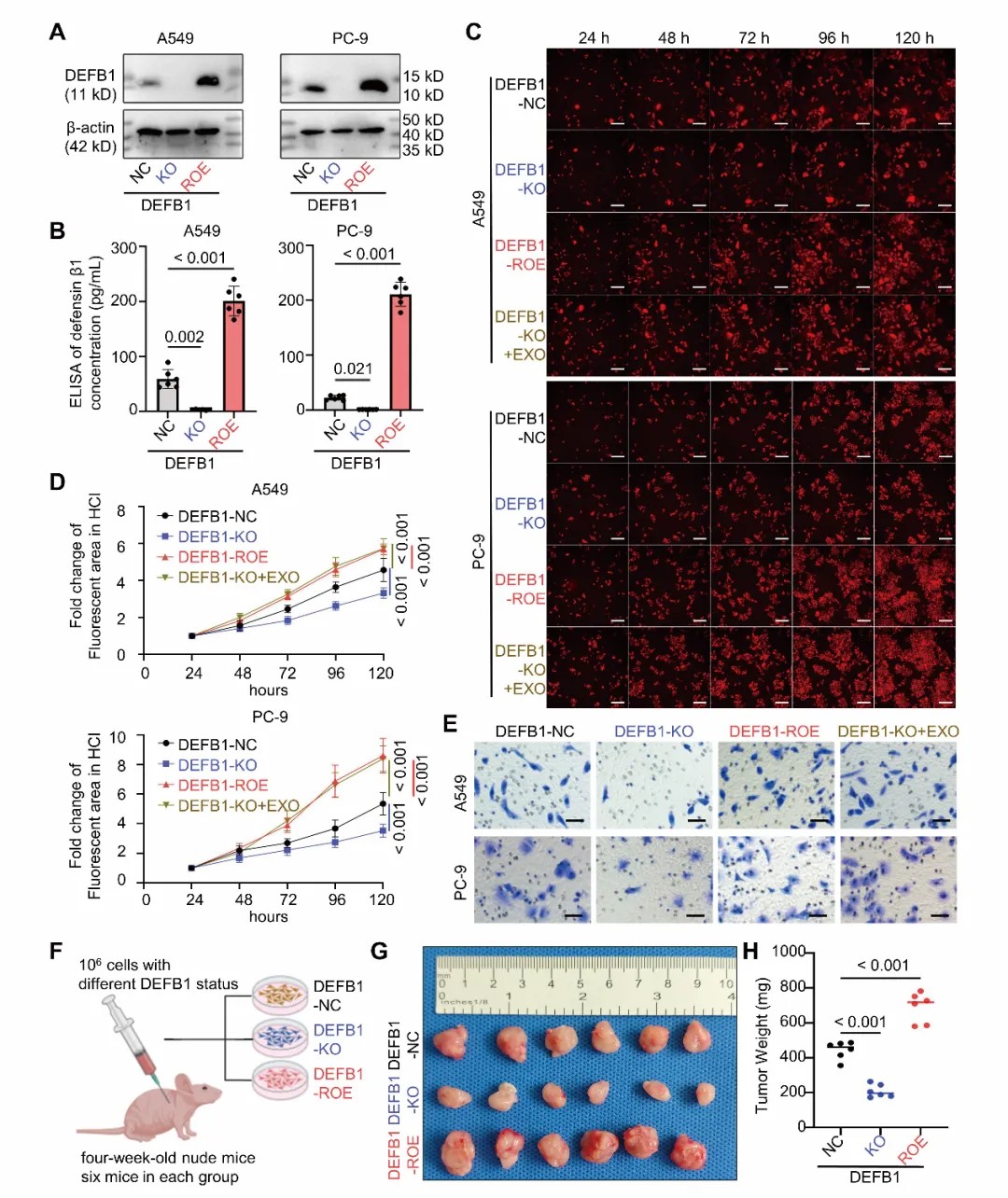
双机制驱动肿瘤进展:肿瘤细胞与免疫微环境协同
机制研究显示,DEFB1通过“双通路”驱动肺腺癌进展。一方面,通过Co-IP质谱筛选,团队发现DEFB1可与膜蛋白PPL结合,进而促进上皮-间质转化(EMT),表现为E-cadherin下调、Vimentin与Snail上调,并显著增强细胞增殖、迁移与侵袭能力;而敲除PPL后,DEFB1的促肿瘤效应明显消失,提示PPL是关键介导因子。另一方面,研究进一步发现DEFB1还能结合炎症因子MIF,调控巨噬细胞极化,抑制M1型巨噬细胞并促进M2型免疫抑制表型,从而重塑促肿瘤免疫微环境。使用MIF抑制剂可部分逆转这一过程,而同时阻断PPL与MIF则几乎完全消除DEFB1的促瘤效应,揭示其“双机制驱动”的生物学本质。
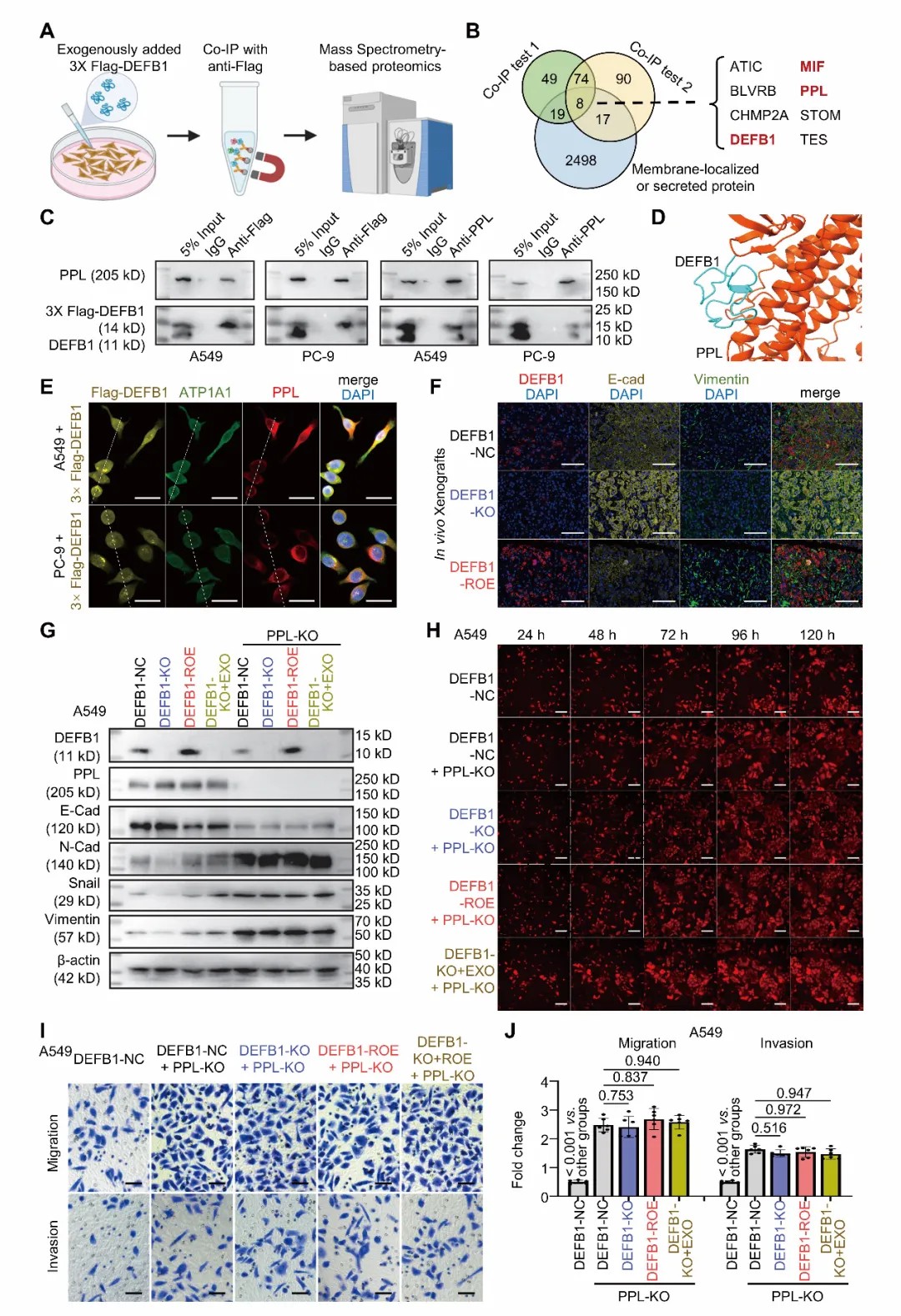
靶向DEFB1:抗体治疗展现强大转化潜力
鉴于DEFB1为分泌蛋白,具有良好的药物可及性,研究团队进一步开展转化研究,成功开发多株抗DEFB1单克隆抗体。其中mAb-5表现最优,可显著抑制肿瘤细胞增殖、迁移与侵袭,抑制EMT过程,并逆转M2型巨噬细胞极化。在肺腺癌类器官、异种移植瘤以及自发性KRAS驱动肺癌模型中,mAb-5均表现出一致的抗肿瘤活性,显著抑制肿瘤生长并延长小鼠生存。同时安全性评估显示,该抗体无明显毒性或器官损伤,具有良好耐受性,提示其具备潜在临床转化价值。
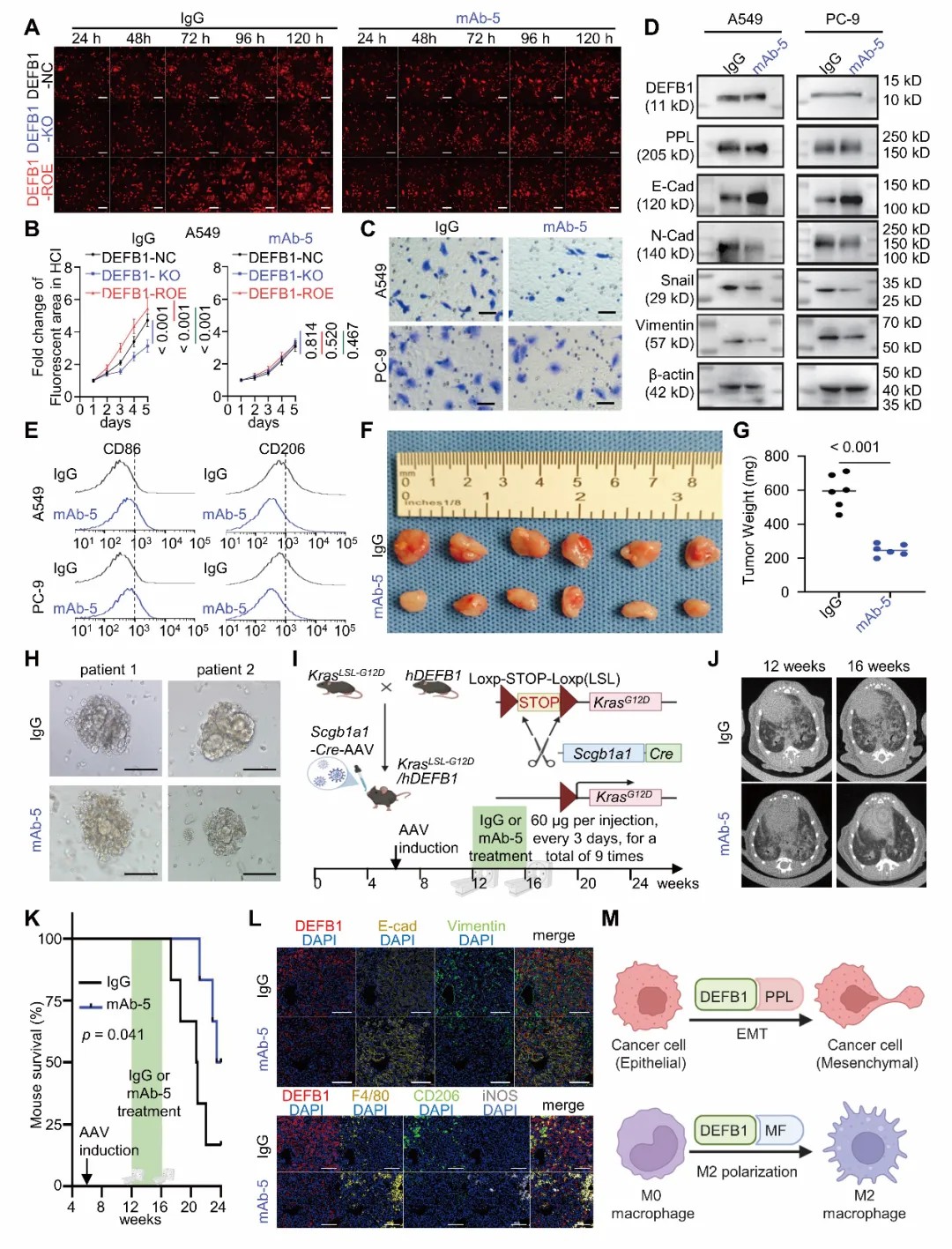
总结
总体而言,本研究首次系统阐明DEFB1是肺腺癌的新型驱动因子与可成药靶点,揭示其通过PPL介导EMT及MIF介导免疫抑制的双机制促瘤模式,并开发出具有转化潜力的中和抗体mAb-5。该工作不仅拓展了我们对肿瘤相关抗菌肽的认知,也为肺腺癌靶向治疗提供了全新方向。
原文链接:
https://www.nature.com/articles/s41419-026-08748-4(转化医学网360zhyx.com)
【关于投稿】
转化医学网(360zhyx.com)是转化医学核心门户,旨在推动基础研究、临床诊疗和产业的发展,核心内容涵盖组学、检验、免疫、肿瘤、心血管、糖尿病等。如您有最新的研究内容发表,欢迎联系我们进行免费报道(公众号菜单栏-在线客服联系),我们的理念:内容创造价值,转化铸就未来!
转化医学网(360zhyx.com)发布的文章旨在介绍前沿医学研究进展,不能作为治疗方案使用;如需获得健康指导,请至正规医院就诊。
责任声明:本稿件如有错误之处,敬请联系转化医学网客服进行修改事宜!
微信号:zhuanhuayixue
 腾讯登录
腾讯登录









还没有人评论,赶快抢个沙发