Cell Stem Cell | 复旦大学附属肿瘤医院郭小毛/俞晓立/陈飞/沈敏洪团队合作构建乳腺癌类器官多组学图谱,解析四种表观状态,揭示驱动乳腺癌淋巴结转移的关键转录因子
| 导读 | 本研究通过建立乳腺癌 PDO 生物库并开展系统性多组学分析,描绘了乳腺癌进展过程中的表观遗传变化图谱,提出了四种具有不同生物学特征的表观遗传状态。 |
乳腺癌是全球女性最常见的恶性肿瘤之一,其临床表现和分子特征高度异质。尽管目前临床已形成较成熟的分型体系,并广泛用于指导治疗,但这些方法更多反映的是肿瘤的静态分子特征,仍难以揭示肿瘤在进展、状态转换和播散过程中的动态调控规律,也难以充分解释同一分型患者之间明显不同的治疗反应和临床结局。
近年来,越来越多研究提示,染色质可及性变化和转录因子调控网络重塑,是肿瘤细胞获得可塑性、侵袭性和治疗抵抗能力的重要基础。患者来源类器官(patient-derived organoids,PDOs)因能够较好保留原始肿瘤的组织病理、转录及表观遗传特征,正成为研究乳腺癌发生发展和转移机制的重要工具。
2026年3月16日,复旦大学附属肿瘤医院郭小毛、俞晓立、陈飞、沈敏洪团队合作在《Cell Stem Cell》发表题为 Paired patient-derived organoids reveal transcription factor-driven epigenetic remodeling in breast cancer metastasis 的研究论文。研究团队建立了大规模乳腺癌原发肿瘤、癌旁正常组织及淋巴结转移灶的配对PDOs活体生物库,并整合基因组、转录组和染色质可及性等多组学数据,系统揭示了乳腺癌进展过程中的表观遗传重编程规律,识别出四种不同的表观遗传状态,并阐明了转录因子协同网络驱动淋巴结转移的关键分子机制,为突破传统乳腺癌分型局限、推进精准治疗提供了新的理论依据和实验平台。
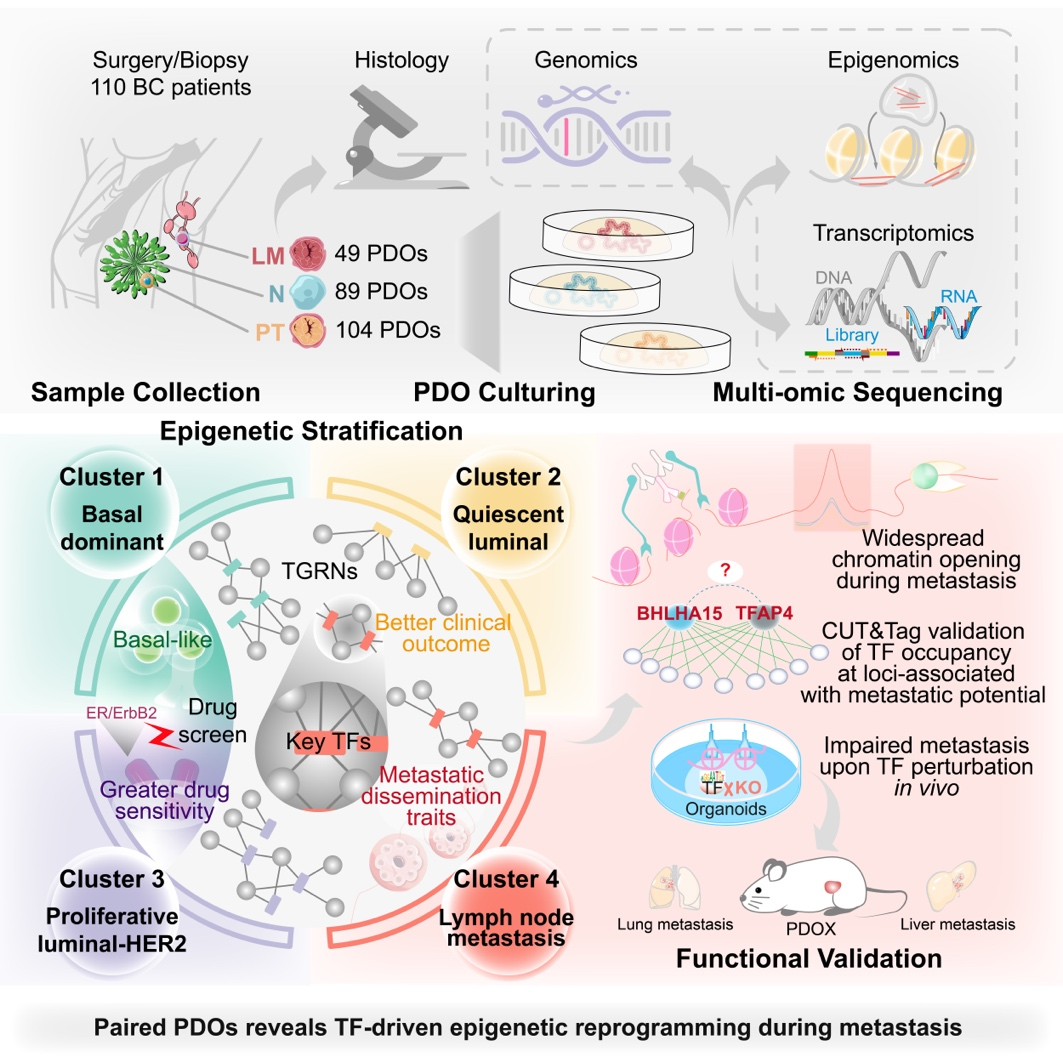
图形摘要
乳腺癌PDOs活体生物库的构建与多维度验证
为解决传统模型难以真实还原乳腺癌进展过程中动态分子变化这一难题,研究团队系统优化了PDOs的培养与建系流程,针对原发灶、淋巴结转移灶及正常乳腺组织的不同生物学特性,设计了定制化培养基配方,显著提高了类器官建系效率和长期培养稳定性。
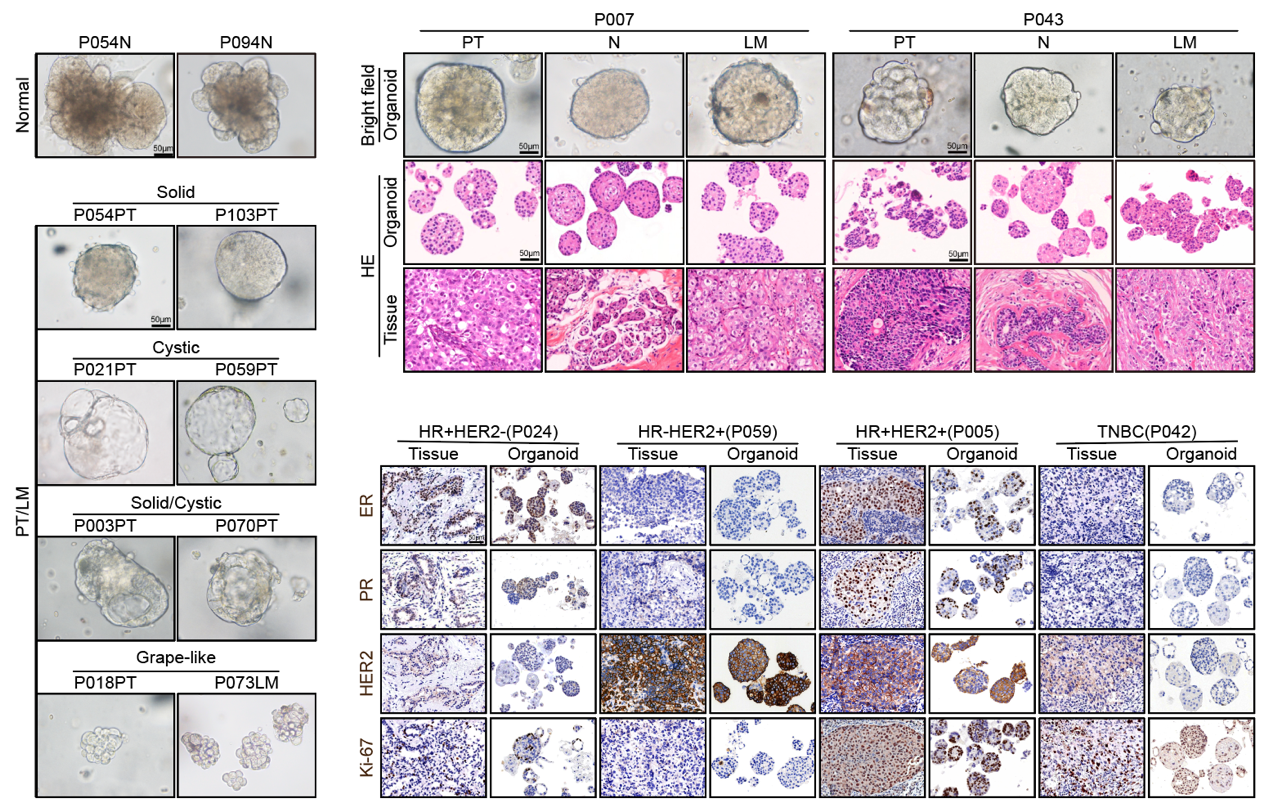
乳腺癌类器官组织病理学特征
研究团队最终建立了涵盖原发乳腺肿瘤、癌旁正常组织及淋巴结转移灶的配对PDOs活体生物库。多维度验证结果显示,该生物库具有较高的生物学保真度。肿瘤PDOs保留了原始肿瘤实性、囊性及葡萄状等异质性形态,正常乳腺组织 PDOs 则表现出更均一的形态特征。H&E染色和免疫组化进一步表明,PDOs 在组织学结构及ER、PR、HER2、Ki-67等关键临床标志物表达方面与来源组织高度一致,说明其能够较好保留乳腺癌的核心分子和组织学特征,是研究肿瘤进展和转移的重要模型。
在此基础上,研究团队对来源于正常组织、原发肿瘤和淋巴结转移灶的PDOs进行了系统性的转录组、基因组和表观遗传特征分析,构建了覆盖乳腺癌发生、进展与转移过程的多组学功能模型资源库。
四种表观遗传状态勾勒乳腺癌异质性新图谱
基于染色质可及性与转录组联合分析,研究团队在乳腺癌PDOs中识别出四种具有独特生物学特征的表观遗传状态。这四种状态具有明显不同的调控元件开放模式和转录程序,提示乳腺癌在表观遗传层面存在独立于传统分类的状态维度。
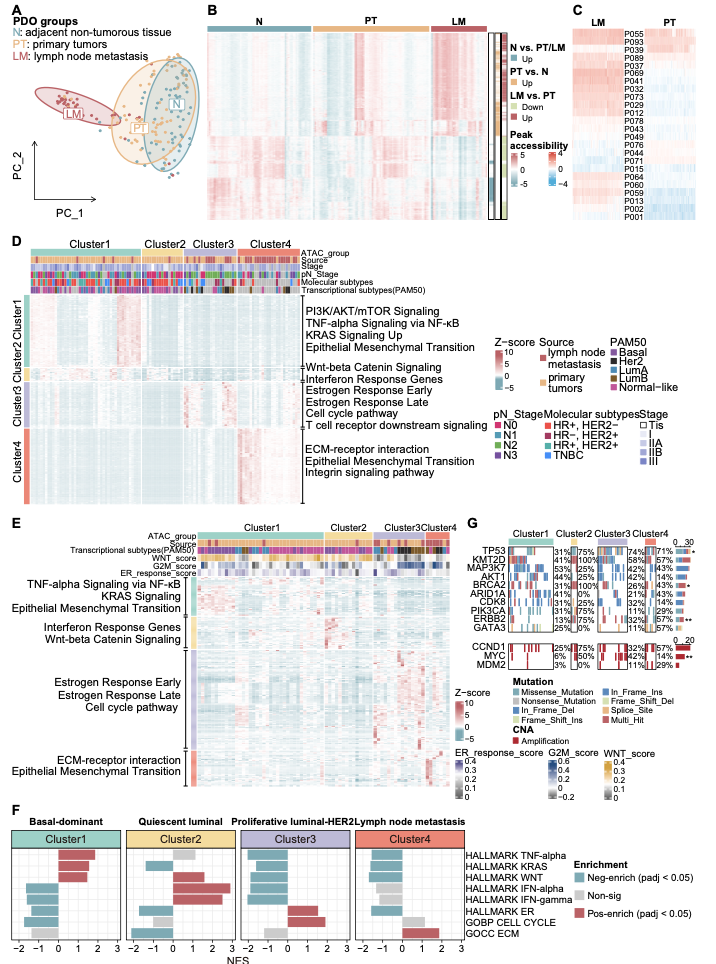
Cluster 1(Basal-dominant cluster) 为基底样主导状态。该状态富集 PI3K/AKT/mTOR、TNF-α、KRAS 及 EMT 等信号通路,呈现更强的侵袭性和干细胞样特征。TP63、SOX9 和 FOSL1 被鉴定为该状态的重要调控转录因子,患者预后相对较差。
Cluster 2(Quiescent luminal cluster) 为静息 luminal 样状态。该状态更接近正常乳腺上皮,以 Normal-like PAM50 特征为主,主要来源于淋巴结阴性患者的原发肿瘤,整体增殖活性较低。HOXA 家族转录因子在该状态中发挥关键调控作用,对应患者总体预后最佳。
Cluster 3(Proliferative luminal-HER2 cluster) 为高增殖 luminal-HER2 相关状态。该状态以激素应答和细胞周期活化为主要特征,并常伴 MYC 扩增。ESR1、FOXA1 和 FOXO6 是其重要调控因子,提示这一状态可能对内分泌治疗和 HER2 靶向治疗更为敏感。
Cluster 4(Lymph node metastasis cluster) 为淋巴结转移相关状态。该状态主要由淋巴结转移灶来源的PDOs构成,ECM-受体相互作用和 EMT 通路显著富集,代表了乳腺癌转移相关的特异性表观遗传状态,也是本研究重点关注的转移相关状态。
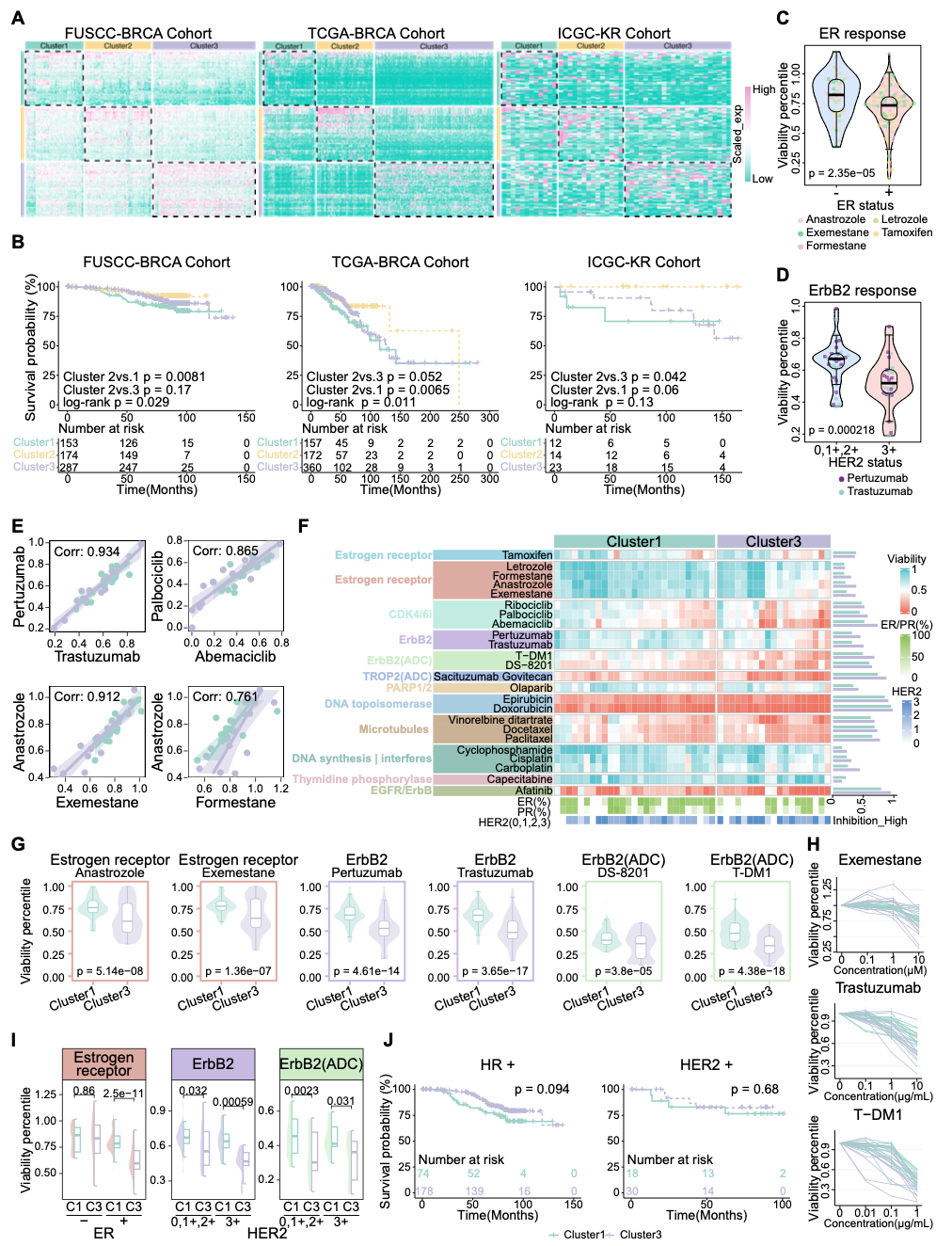
表观遗传状态预测乳腺癌患者预后并提示潜在治疗策略
为了验证这一表观遗传状态框架的稳健性,研究团队进一步将PDOs中提取出的状态特异基因特征应用于多个独立乳腺癌患者队列。结果显示,前三种主要来源于原发灶的表观遗传状态在外部人群中均可被稳定识别,其对应的通路特征也得到重复验证,提示这一状态框架具有较好的可重复性和可推广性。
进一步分析发现,这些状态与患者临床结局密切相关。Cluster 2(静息 luminal 样状态)患者预后最好;Cluster 1(基底样主导状态)和 Cluster 3(高增殖 luminal-HER2 相关状态)则与更高复发风险相关,其中 Cluster 1 还与更差总生存相关。这说明,表观遗传状态不仅能够反映乳腺癌内部更深层次的生物学差异,也具有明确的预后意义。
在治疗层面,基于PDOs的药物筛选结果显示,不同表观遗传状态对应不同治疗脆弱性。其中,Cluster 3对内分泌治疗、HER2靶向治疗及部分CDK4/6抑制剂表现出更高敏感性。进一步分层分析显示,在ER阳性样本中,Cluster 3相较Cluster1而言对内分泌治疗反应更好。上述结果提示,表观遗传状态框架不仅有助于刻画乳腺癌的生物学异质性,也有望为精准治疗提供新的分层依据。

ATAC-seq 与 RNA-seq 整合分析揭示驱动转移相关表观状态的关键转录因子
关键转录因子网络驱动乳腺癌淋巴结转移相关状态
在四种状态中,最值得关注的是 Cluster 4,即淋巴结转移相关状态。这一状态主要由淋巴结转移灶来源类器官构成,具有鲜明的ECM重塑、细胞运动和EMT相关特征,提示其与乳腺癌淋巴结转移密切相关。为进一步解析这一状态背后的调控机制,研究团队整合 ATAC-seq 和 RNA-seq 构建了转录因子—靶基因调控网络,并结合网络拓扑特征、染色质可及性和基因表达变化,筛选出一组驱动淋巴结转移相关状态的核心转录因子,包括MEF2A、NR2F1、NR2F2、NFATC4、ZNF148、TFAP4 和 BHLHA15等。研究发现,这些转录因子不仅在 Cluster 4 中显著活跃,其结合位点区域的染色质开放程度也同步增强。其中,TFAP4和BHLHA15表现出最强的协同调控特征,不仅在开放染色质区域显著富集,还共享大量基因组结合位点,并与下游转录程序高度相关。
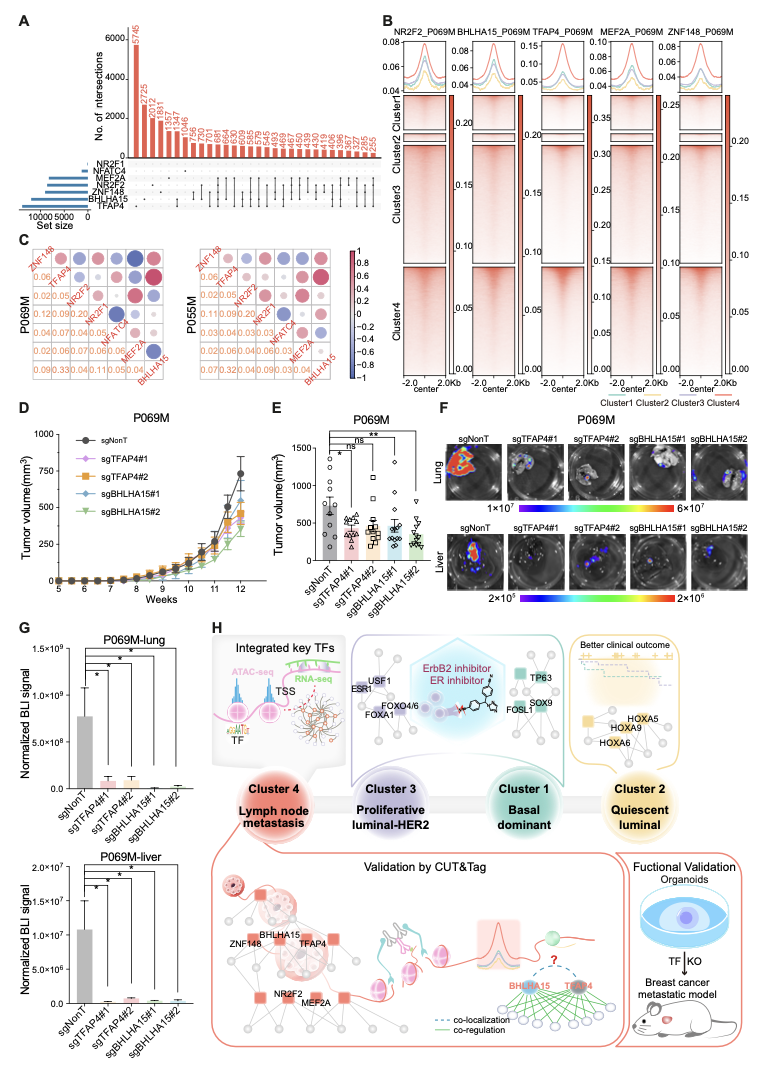
TFAP4–BHLHA15协同转录因子网络驱动乳腺癌转移
进一步的 CUT&Tag、CRISPR 敲除和体内功能实验表明,TFAP4 或 BHLHA15 缺失后,EMT、细胞外基质组织和细胞黏附等转移相关程序明显下调。体内移植实验进一步显示,敲除 TFAP4 或 BHLHA15 可显著降低PDO移植瘤的肺和肝转移负担;在免疫健全小鼠的4T1乳腺癌模型中,这一结果同样得到验证。上述结果提示,Cluster 4 并非仅仅在表型上“像转移”,而是由一套可操作、可验证的表观遗传调控网络驱动的淋巴结转移相关状态。这一发现为理解乳腺癌淋巴结转移提供了更具体的机制框架,也提示 TFAP4、BHLHA15 等转录因子可能成为干预转移过程的潜在靶点。
研究意义与未来展望
本研究通过建立乳腺癌 PDO 生物库并开展系统性多组学分析,描绘了乳腺癌进展过程中的表观遗传变化图谱,提出了四种具有不同生物学特征的表观遗传状态。研究不仅深化了对乳腺癌异质性和转移机制的认识,也为患者分层和精准治疗提供了新的思路。
研究团队表示,未来将进一步依托 PDO 模型,探索建立新辅助放疗分层体系并解析局部晚期乳腺癌放疗抵抗的分子机制,为乳腺癌患者精准治疗策略的优化提供新的研究基础。
复旦大学附属肿瘤医院陈飞、俞晓立、郭小毛、沈敏洪教授为论文的共同通讯作者,复旦大学肿瘤医院博士后饶欣欣、王静雯为论文的共同第一作者。
附简历:
郭小毛教授(通讯作者)
上海市质子重离子医院(复旦大学附属肿瘤医院质子重离子中心)临床技术委员会 主任
复旦大学附属肿瘤医院放射治疗中心教授,主任医师,博士生导师
历任上海市质子重离子医院 院长
历任复旦大学附属肿瘤医院院长,党委书记
上海市优秀学科带头人
享受国务院“政府特殊津贴”专家
中国抗癌协会副理事长
中国抗癌协会放射治疗专业委员会第五届委员会 主任委员
承担国家科技部“863”计划、国家自然科学基金、上海张江国家自主创新示范区专项发展资金重大项目等多项科研项目,先后在JAMA Oncology,Cell Stem Cell,Advanced Science,molecular cancer,International Journal of Radiation Oncology&Biology&Physics 等肿瘤权威杂志发表论文百余篇
俞晓立教授(通讯作者)
复旦大学附属肿瘤医院,放射治疗中心主任,教授,主任医师,博士,博士生导师。
2002-2004在美国Duke大学医学中心从事放疗相关正常组织损伤的研究工作,2012.4-2012.8在意大利国家粒子治疗中心(CNAO)进修质子重离子放疗技术。2011年经资格考试及相关资格认证获得欧洲放疗学会(ESTRO)的 Fellow,成为该学会在中国地区首批唯一的Fellow资格获得者。
主要学术任职:国家卫健委人才交流服务中心肿瘤精准放疗专项技能培训项目专家委员会委员,中国抗癌协会肿瘤放射治疗专业委员会常务委员,中华医学会放射治疗专业委员会乳腺学组副组长,中国医院协会肿瘤医院分会委员,中国抗癌协会乳腺癌专业委员会委员,中国抗癌协会肿瘤整形外科专业委员会委员,中国研究型医院学会乳腺癌专业委员会委员,上海市医学会放射治疗专业委员会副主任委员,上海市抗癌协会乳腺癌专业委员会常务委员,上海市抗癌协会放疗专业委员会委员。
主要研究方向为乳腺癌及软组织肿瘤的放射治疗相关临床及转化性研究,主持国自然项目三项,国家卫生健康委医药卫生科技发展研究中心“四大慢病”重大专项子课题负责人,国家重点研发计划“基于国产创新放疗设备的肿瘤放疗应用示范”专项子课题负责人,上海市卫健委“重中之重”-上海市肿瘤放射治疗临床医学中心建设主要负责人,担任ESTRO的英文杂志Clinical & Translational Radiation Oncology的编委,共发表论文80余篇,其中以第一作者及通讯作者发表SCI论文40余篇,其中发表在国际医学及放疗专业顶级杂志JAMA Oncology,Cell Stem Cell,Advanced Science,International Journal of Surgery,International Journal of Radiation Oncology&Biology&Physics,Cancer,Oncologist, Annals of Surgical Oncology等。
陈飞教授(通讯作者)
中国科学院分子细胞科学卓越创新中心、复旦大学附属肿瘤医院教授,博士生导师。
曾获“尚思探索学者”项目(2024年)、国家杰出青年科学基金(2024年)、科技部重点研发计划青年科学家项目(2022年)、国家高层次人才青年项目(2020年)等基金支持。自2020年初建立实验室以来,以通讯(含共同)作者身份在Nature、Science、Cell Stem Cell、Cell Research、Molecular Cell(3篇)、Nature Chemical Biology、Science Advances、Nature Communication、Cell Reports等杂志上发表论文。
沈敏洪教授(通讯作者)
复旦大学附属肿瘤医院青年研究员,博士研究生导师。
主要研究方向为肿瘤微环境在肿瘤转移和耐药过程中的作用机制。曾获国家海外高层次青年引进人才项目(2023年)、DoD LCRP创新理念发展奖(2023年)、Susan G. Komen博士后奖学金(2017年)、NJCCR博士后奖学金(2015年)等项目支持。近年来,以第一或通讯作者(含共同)身份在 Cancer Cell、Nature Cancer、Trends in Cancer、Signal Transduction and Targeted Therapy、Cell Stem Cell、Cancer Research、Advanced Science 等国际期刊发表多篇代表性论文。
饶欣欣博士(第一作者)
复旦大学附属肿瘤医院放射治疗中心基地住培医师、“卓医计划”临床博士后。主要从事乳腺癌、肿瘤放射治疗及基于类器官模型的基础与转化研究。以第一作者(含共同第一作者)在 Cell Stem Cell、International Journal of Radiation Oncology, Biology, Physics、Clinical and Translational Medicine、Stem Cell Reports 等期刊发表 SCI论文多篇。主持中国博士后科学基金面上项目1项。
王静雯博士(第一作者)
复旦大学系统生物学博士,复旦大学附属肿瘤医院博士后。
主要研究方向为单细胞转录组学及多组学整合分析。以第一作者(含共同第一作者)在 Cell Stem Cell、Journal of Translational Medicine 等期刊发表多篇研究论文。
 腾讯登录
腾讯登录







还没有人评论,赶快抢个沙发