突破性研究!上海交通大学医学院附属第六人民医院贾伟/郑晓皎团队揭示高糖饮食如何通过肠道菌群加速脂肪肝恶化,开发工程益生菌
| 导读 | 与此同时,该研究团队成功开发出一种能高效清除乙醛的工程化益生菌,在临床前模型中有效阻断了肝纤维化进程,为防治这一全球高发肝病提供了全新的干预策略。 |
近日,上海交通大学医学院附属第六人民医院贾伟/郑晓皎团队在国际知名期刊《Cell Metabolism》发表一项突破性研究:系统性阐明了过量摄入糖分,尤其是果糖,如何通过重塑肠道菌群功能,导致内源性乙醛大量产生,从而驱动代谢相关脂肪性肝病向更严重的肝炎阶段快速进展。与此同时,该研究团队成功开发出一种能高效清除乙醛的工程化益生菌,在临床前模型中有效阻断了肝纤维化进程,为防治这一全球高发肝病提供了全新的干预策略。
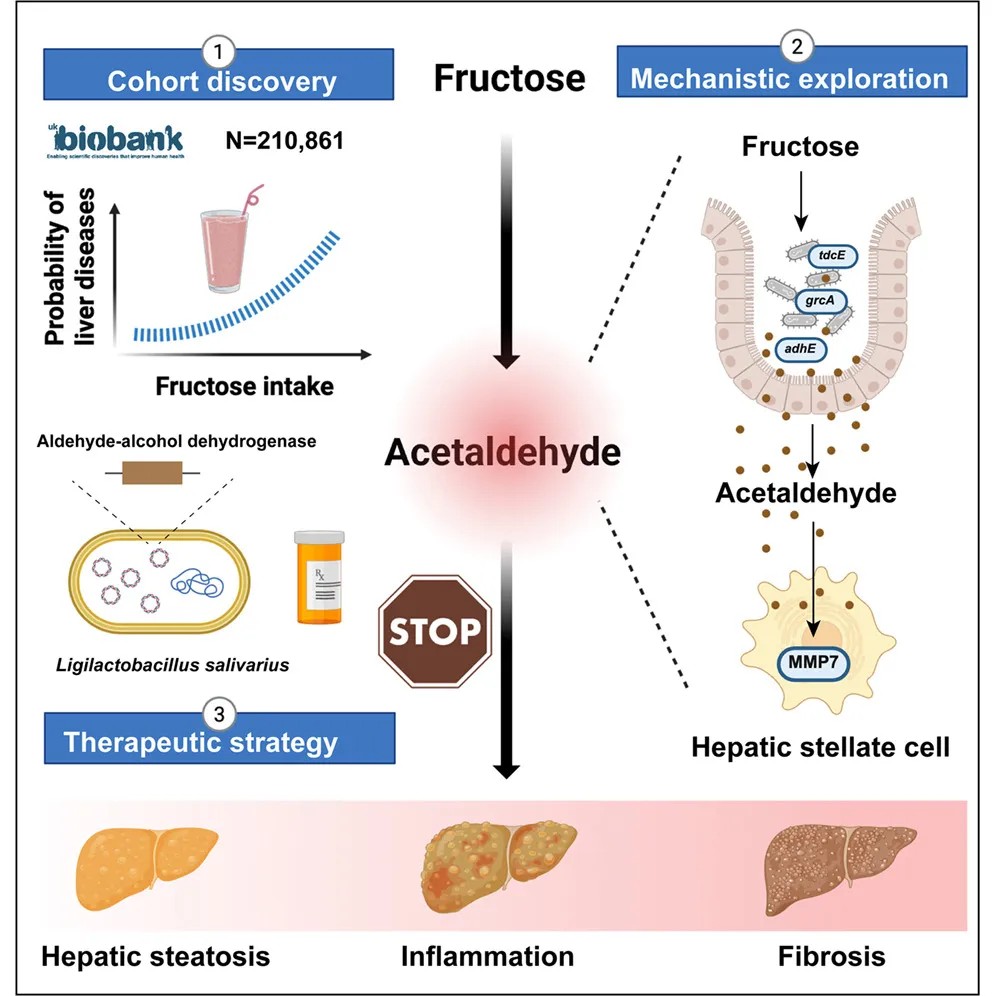
图形摘要
高糖摄入与肝病恶化直接相关
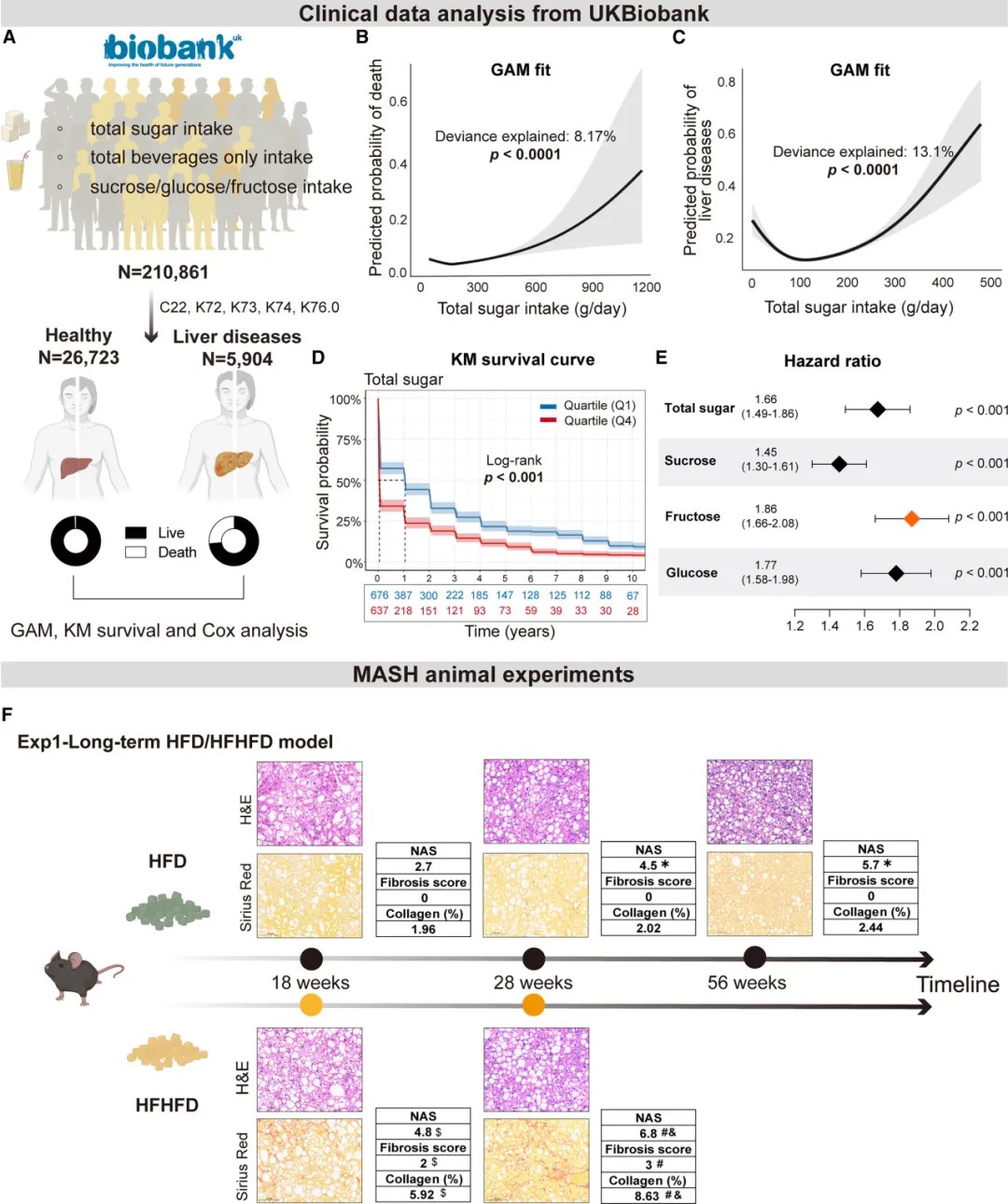
高糖摄入与MASLD-MASH的疾病进展相关
研究团队首先对英国生物银行超过21万参与者的数据进行了分析,发现糖分摄入量与肝脏相关死亡风险呈剂量依赖性正相关,其中果糖的影响尤为显著。在动物实验中,给予高脂高果糖饮食的小鼠,其肝脏纤维化的发展速度和严重程度远高于仅给予高脂饮食的小鼠,证实了膳食糖是加速疾病进展的关键环境因素。
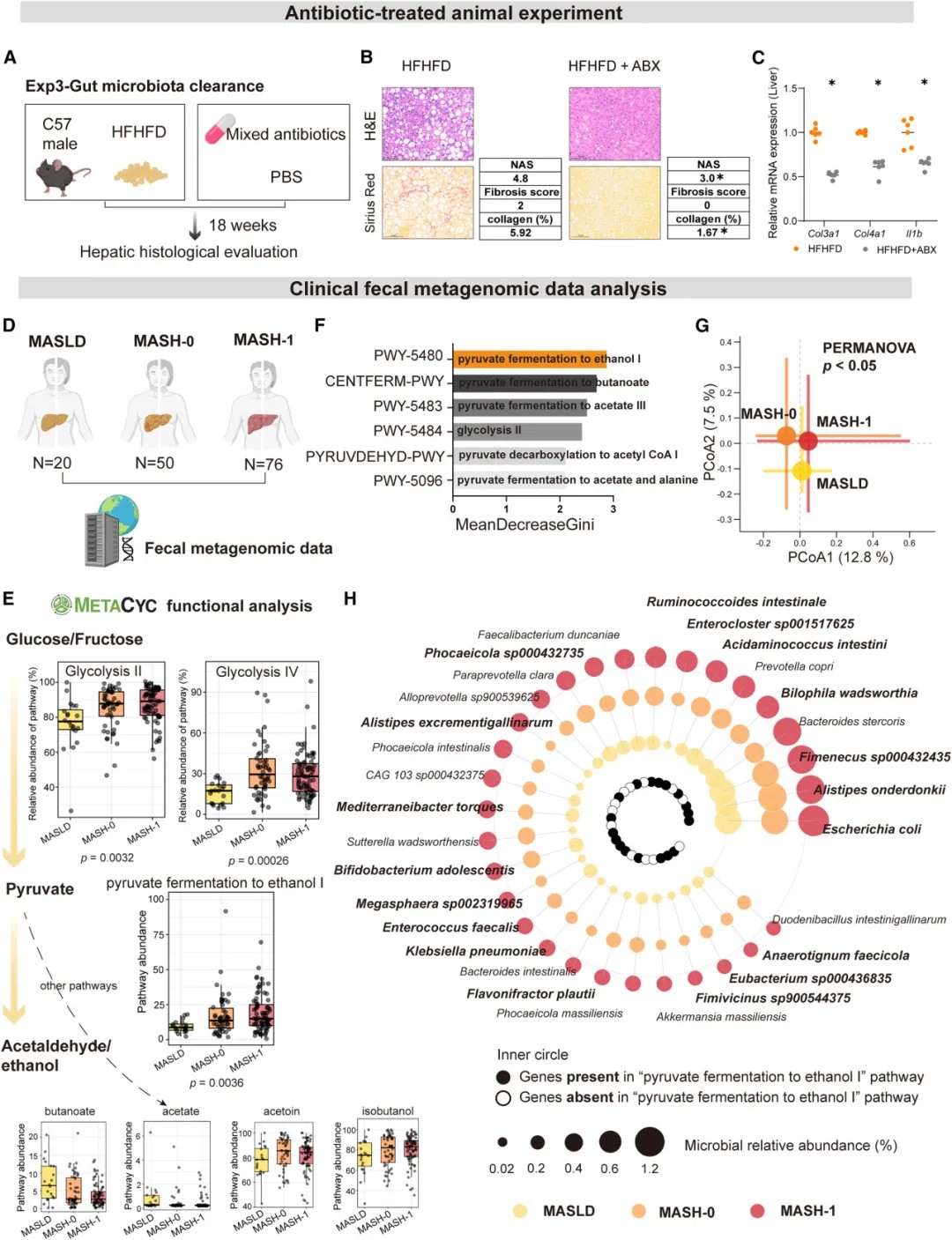
MASLD-MASH进展中的肠道菌群功能转变
肠道菌群是关键的“转化器”
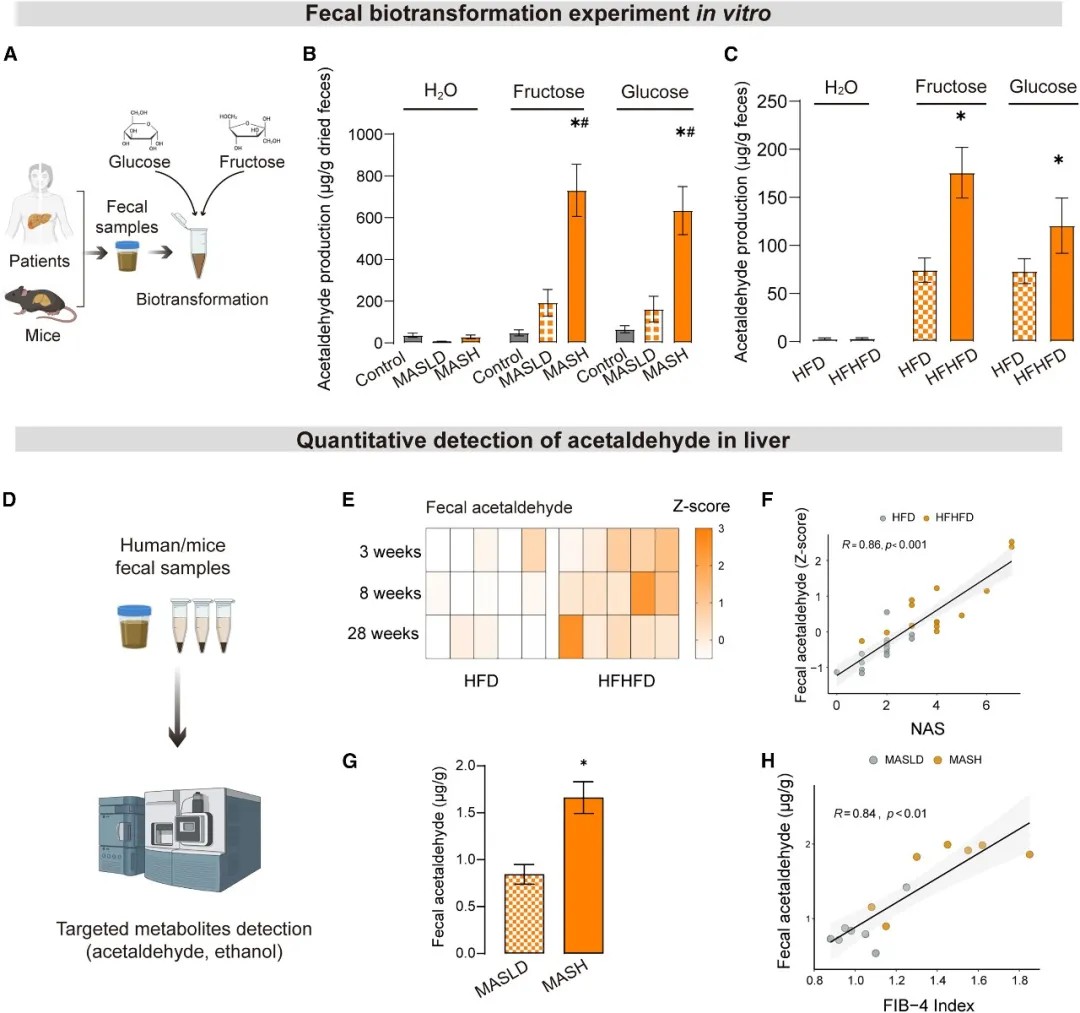
肠道菌群介导内源性乙醛的体外转化实验
机制研究表明,肠道微生物在此过程中扮演了核心角色。通过对患者队列的宏基因组分析,科学家发现,当疾病进展至脂肪性肝炎阶段时,患者肠道菌群的功能发生显著重塑,倾向于通过“丙酮酸发酵生成乙醇I”等途径大量产生乙醛和乙醇。体外粪便转化实验进一步证实,来自肝炎患者的粪便样本利用果糖或葡萄糖产生乙醛的能力显著增强。
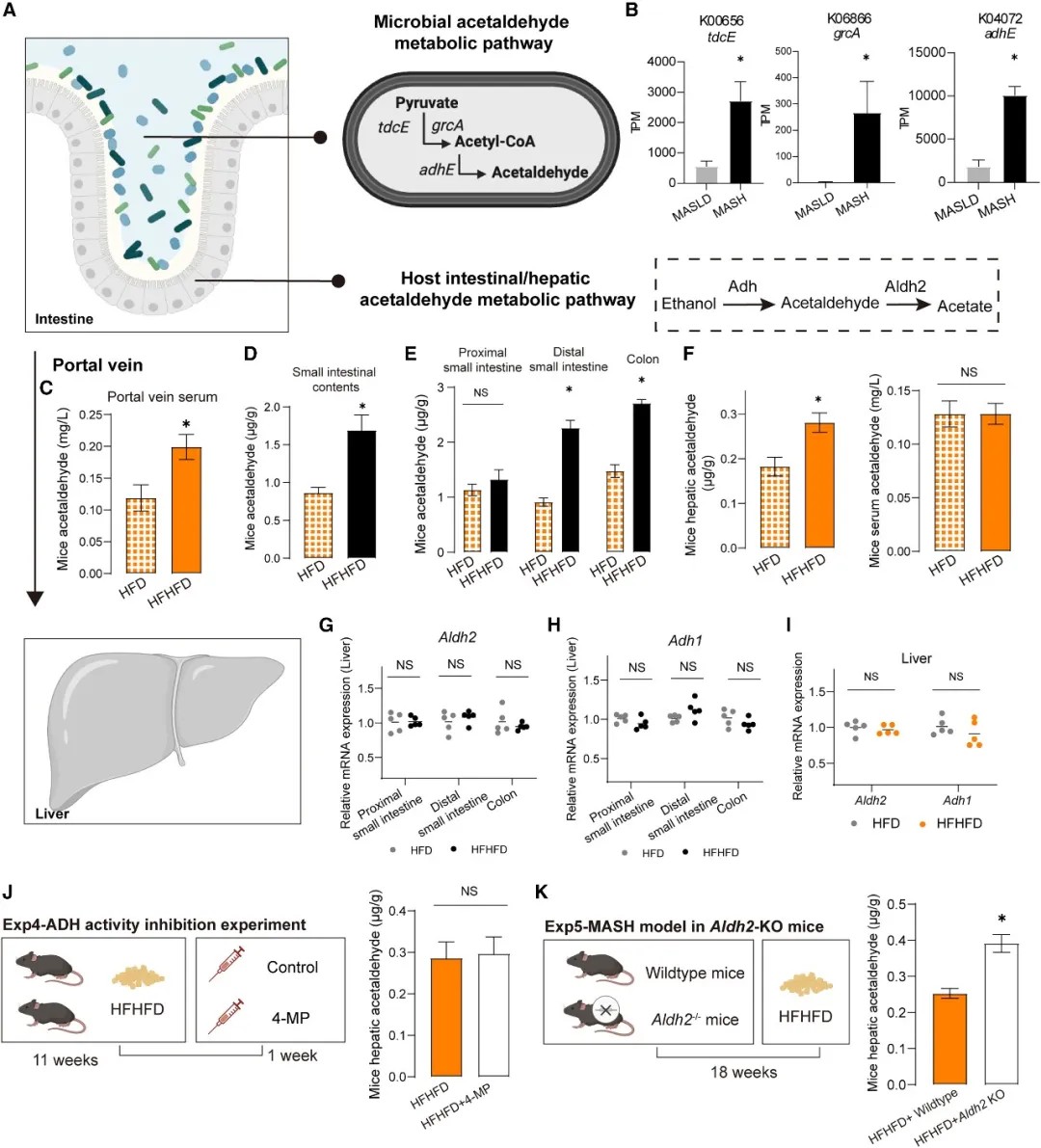
内源性乙醛来源于肠道菌群
乙醛直接驱动肝纤维化
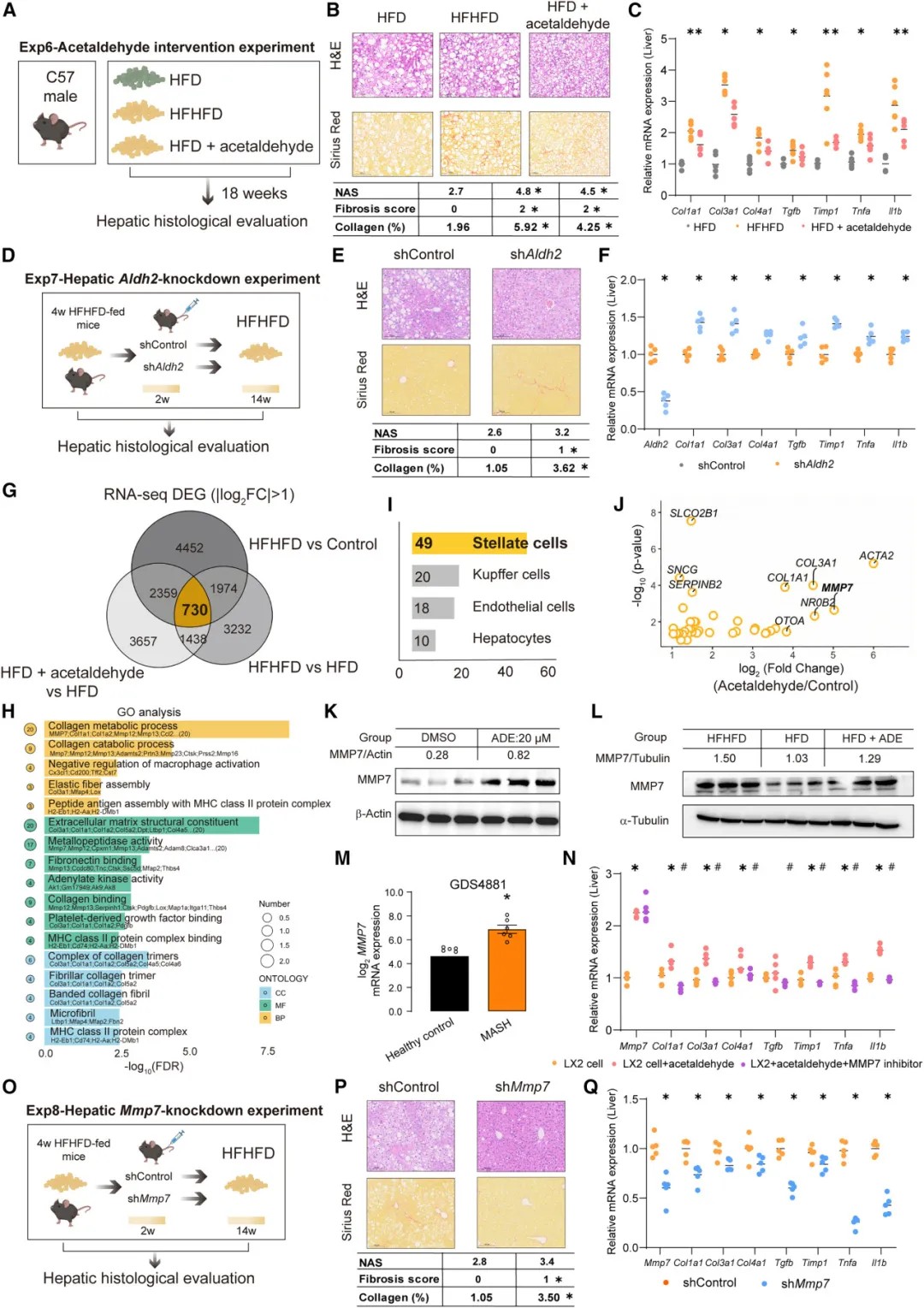
乙醛通过上调HSCs中MMP7表达驱动肝纤维化
这些由肠道菌群产生的乙醛能够进入血液循环并到达肝脏。研究揭示,乙醛会激活肝星状细胞,通过上调基质金属蛋白酶7的表达,直接驱动肝脏纤维化的发生。在动物模型中,补充低剂量乙醛或特异性敲低肝脏清除乙醛的关键酶,均会加剧肝纤维化;而抑制MMP7则可有效缓解纤维化。
工程益生菌提供治疗新方案
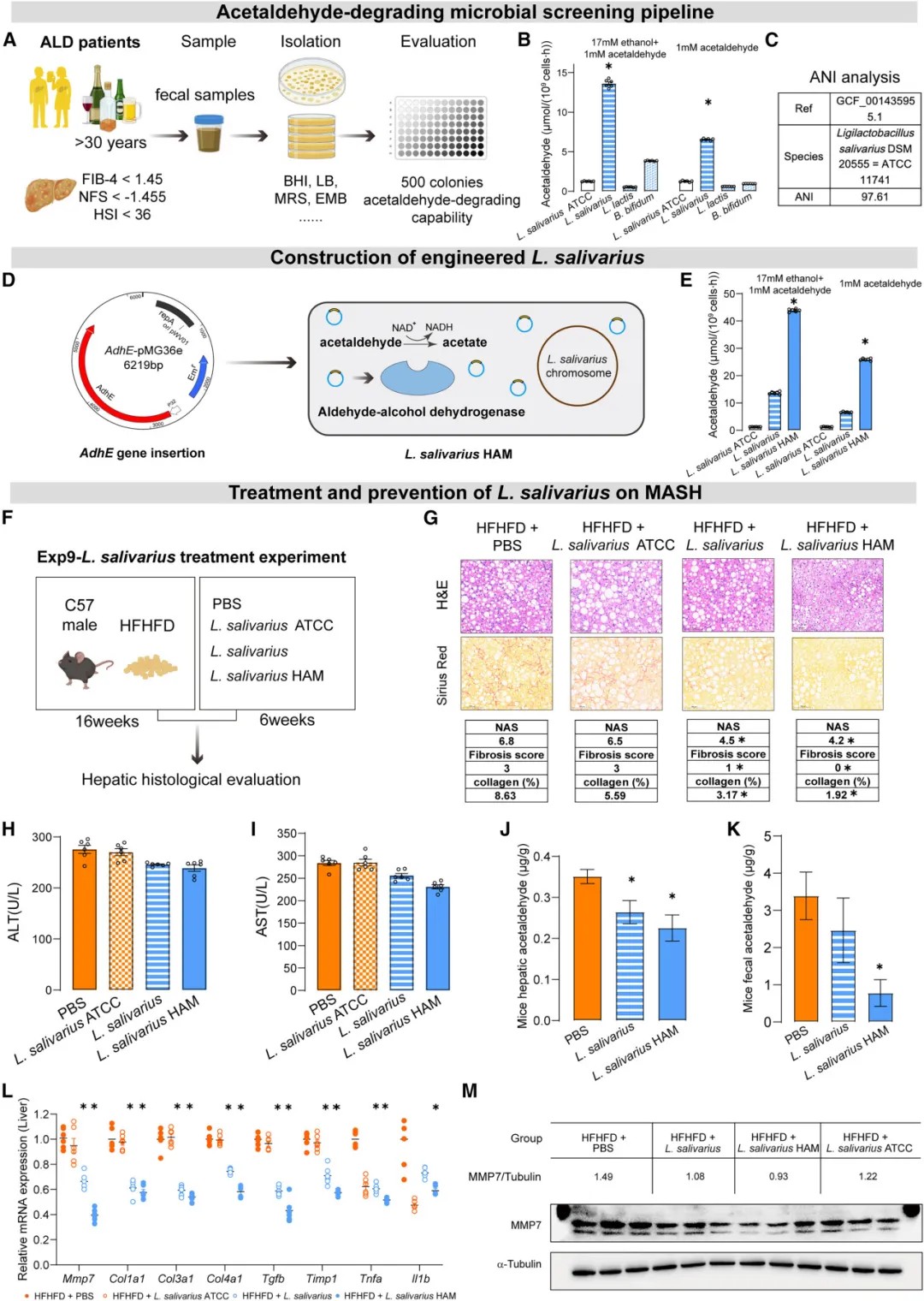
益生菌干预显著阻遏MASLD-MASH进展
基于上述机制,研究团队从长期饮酒但肝脏健康者的粪便中,筛选出一株具有较强乙醛降解能力的唾液乳杆菌。通过基因工程手段使其过表达微生物来源的双功能醛-醇脱氢酶,得到了代谢能力大幅增强的工程菌株“HAM”。在饮食诱导的肝病小鼠模型中,口服这种工程益生菌能显著降低肝脏和粪便中的乙醛水平,有效改善肝脏炎症和纤维化,且对整体肠道菌群生态影响微小,安全性良好。
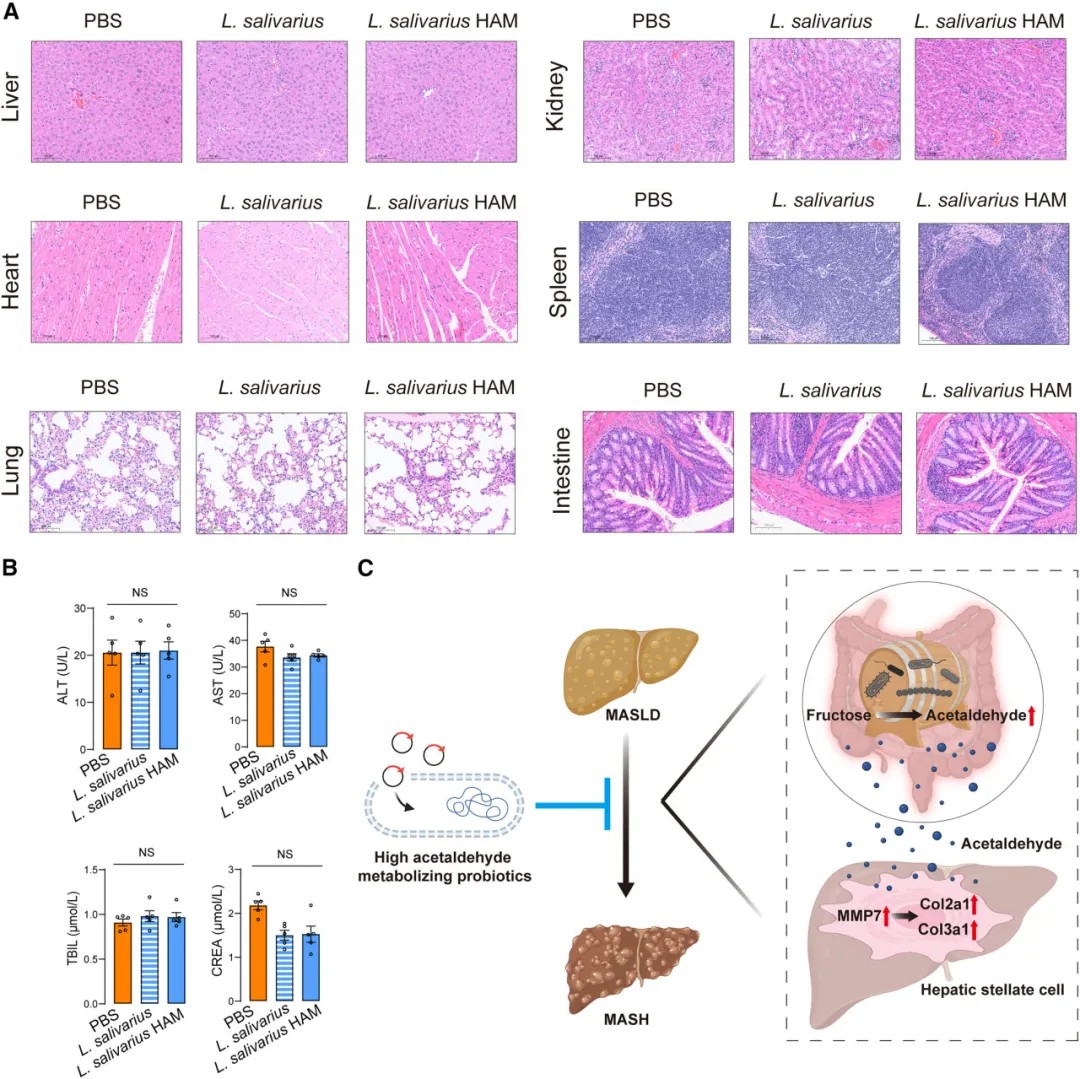
唾液乳杆菌的安全性评估
研究意义与未来展望
这项研究不仅揭示了从普通脂肪肝向肝炎转变的一条关键致病轴——“糖-菌群-乙醛-纤维化”,还创新性地提出了以肠道菌群代谢为靶点的治疗新思路。工程益生菌的应用,为阻止脂肪肝的恶性进展带来了充满希望的微生态治疗策略。(转化医学网360zhyx.com)
原文链接:
https://www.cell.com/cell-metabolism/fulltext/S1550-4131(26)00043-4
【关于投稿】
转化医学网(360zhyx.com)是转化医学核心门户,旨在推动基础研究、临床诊疗和产业的发展,核心内容涵盖组学、检验、免疫、肿瘤、心血管、糖尿病等。如您有最新的研究内容发表,欢迎联系我们进行免费报道(公众号菜单栏-在线客服联系),我们的理念:内容创造价值,转化铸就未来!
转化医学网(360zhyx.com)发布的文章旨在介绍前沿医学研究进展,不能作为治疗方案使用;如需获得健康指导,请至正规医院就诊。
责任声明:本稿件如有错误之处,敬请联系转化医学网客服进行修改事宜!
微信号:zhuanhuayixue
 腾讯登录
腾讯登录









还没有人评论,赶快抢个沙发