靶向铁死亡通路或破坏免疫抑制!中山大学/杭州医学研究所:可行的食管鳞癌治疗策略
| 导读 | 本研究结果表明 PRDM1 是与 nICRT 耐药性相关的关键因素,并提示靶向铁死亡通路或破坏 PRDM1+ 细胞介导的免疫抑制可能代表了食管鳞状细胞癌(ESCC)的一种可行策略。 |
1月20日,中山大学/杭州医学研究所合作共同在期刊《Advanced Science》上发表了研究论文,题为“PRDM1+ Malignant Cells Mediate an Immunosuppressive Landscape and Resistance to Neoadjuvant Chemoradiotherapy and Immunotherapy in Esophageal Squamous Cell Carcinoma”,本研究中,研究人员发现 NMPR 患者中存在 PRDM1+恶性细胞亚群,与治疗耐药相关。这些细胞表现出强烈的脂质过氧化特征,这种状态与 PRDM1 介导的 CTSB 和 MFSD12 转录激活有关。这种状态使 PRDM1+恶性细胞群更易诱导铁死亡。PRDM1+细胞通过 IL1A-IL1R2 相互作用进一步招募免疫抑制性调节性 T 细胞(Tregs),并通过 CD47-SIRPA 信号激活脂质代谢 TREM2+巨噬细胞,从而营造出免疫逃逸微环境。相反,MPR 患者表现出扩增的细胞毒性 T 效应克隆,具有更强的肿瘤杀伤能力。本研究结果表明 PRDM1 是与 nICRT 耐药性相关的关键因素,并提示靶向铁死亡通路或破坏 PRDM1+ 细胞介导的免疫抑制可能代表了食管鳞状细胞癌(ESCC)的一种可行策略。
食管鳞状细胞癌治疗现状与新策略需求
01
食管癌在全球范围内是第七大常见癌症,也是癌症相关死亡的第六大原因。食管鳞状细胞癌(ESCC)是主要的组织学亚型,在东欧和亚洲尤为普遍。目前,尽管诊断和治疗方面取得了进展,但 ESCC 患者的预后仍然不佳,5 年生存率为 10% 至 30%。大约 50% 的食管癌患者在确诊时已处于局部晚期,适合接受可能治愈的治疗。目前,根据试验结果,新辅助放化疗(nCRT)加食管切除术被推荐为局部晚期、可手术 ESCC 的标准治疗方案。然而,鉴于局部或远处复发率高,nCRT 加食管切除术治疗 ESCC 的长期生存率仍远不能令人满意。因此,建立新的有效治疗策略对于进一步提高 ESCC 患者的长期生存率至关重要。
PRDM1+ 上皮细胞脂质过氧化物升高并与nICRT治疗耐药性相关
02
铁死亡是一种最近发现的非凋亡性细胞死亡方式,其机制依赖于脂质过氧化。鉴于 PRDM1 高表达细胞会促进脂质过氧化的上调,这使得铁死亡具有特别重要的意义。这引发了一个关键的治疗假设:能否通过药物诱导铁死亡来选择性地清除这些过度过氧化的细胞,从而逆转治疗耐药性?MTT 检测表明,虽然 PRDM1 的缺失会减弱 RSL3 诱导的细胞死亡,但其过表达则相反,会促进 KYSE-30 和 KYSE-150 细胞的死亡。值得注意的是,这种促死效应在与铁死亡抑制剂 Ferrostatin-1(Fer-1)或半胱氨酸补充剂 N-乙酰半胱氨酸联合治疗时得到了显著逆转。
研究人员共同发现了一个 PRDM1 阳性的细胞亚群,其通过直接转录调节半胱氨酸代谢与脂质过氧化物积累相关,这可能是食管癌对新辅助放化疗耐药的关键机制。此外,功能研究表明,通过药物诱导铁死亡可选择性清除 PRDM1 高表达细胞,这表明靶向这一通路可能是逆转该背景下治疗耐药性的有前景的策略。
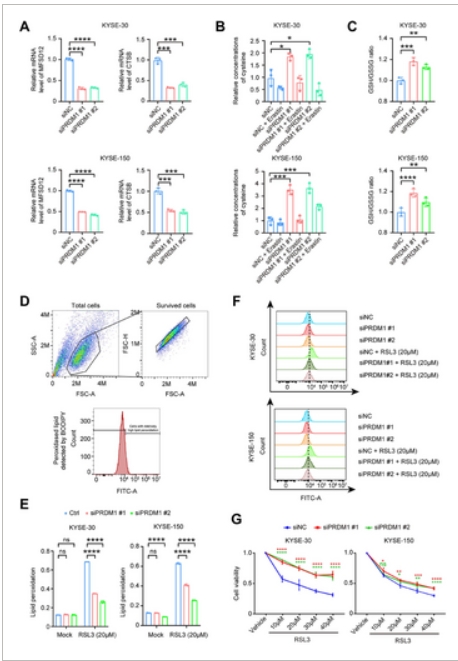
PRDM1 阳性细胞亚群通过直接转录调节半胱氨酸代谢,对脂质过氧化物的积累起着关键作用
结论
03
综上,研究人员提出了逆转 nICRT 治疗耐药性的潜在新策略:(1)将铁死亡诱导剂与 nICRT 联合使用,以增强 PRDM1+肿瘤细胞的铁死亡。(2)使用 IL1A 或 CD47 的抑制剂或抗体来阻断 PRDM1+肿瘤细胞与 Treg 细胞或 LAMs 之间的相互作用,从而逆转免疫抑制状态。
参考资料:
https://advanced.onlinelibrary.wiley.com/doi/10.1002/advs.202515207(转化医学网360zhyx.com)
【关于投稿】
转化医学网(360zhyx.com)是转化医学核心门户,旨在推动基础研究、临床诊疗和产业的发展,核心内容涵盖组学、检验、免疫、肿瘤、心血管、糖尿病等。如您有最新的研究内容发表,欢迎联系我们进行免费报道(公众号菜单栏-在线客服联系),我们的理念:内容创造价值,转化铸就未来!
转化医学网(360zhyx.com)发布的文章旨在介绍前沿医学研究进展,不能作为治疗方案使用;如需获得健康指导,请至正规医院就诊。
责任声明:本稿件如有错误之处,敬请联系转化医学网客服进行修改事宜!
微信号:zhuanhuayixue
 腾讯登录
腾讯登录









还没有人评论,赶快抢个沙发