联合靶向!兰州大学第二医院(第二临床医学院):克服肺腺癌免疫逃逸有前景的协同策略
| 导读 | 联合靶向 GZMK/F2RL1 轴和 PD-1/PD-L1 通路代表了一种有前景的协同策略,可克服 LUAD 中的免疫逃逸。 |
1月12日,兰州大学第二医院(第二临床医学院)研究团队在期刊《Journal for ImmunoTherapy of Cancer》上发表了研究论文,题为“Extracellular granzyme K enhances PD-L1 transcription and stability via F2RL1 activation to facilitate tumor immune evasion in lung adenocarcinoma”,本研究中,为了探究 GZMK 在肺腺癌(LUAD)中的临床相关性及其与程序性死亡配体 1(PD-L1)的关联,研究人员整合了多组学数据集。在肿瘤细胞与 CD8+ T 细胞共培养系统中应用了重组人 GZMK(rhGzmK),通过流式细胞术评估其对 PD-L1 表达和 CD8+ T 细胞功能的影响,并通过蛋白质印迹法分析关键信号蛋白。为了评估 GZMK 抑制的治疗潜力,研究人员在 C57BL/6 小鼠和人外周血单个核细胞(huPBMC)重建的 NVSG 人源化小鼠模型中,将一种选择性 GZMK 抑制剂与抗 PD-1疗法联合使用。最后,对接受免疫治疗的 LUAD 患者临床队列的配对治疗前和治疗后标本进行了多重免疫荧光分析,以评估 GZMK 表达对治疗的时空动态反应。本研究表明,联合靶向 GZMK/F2RL1 轴和 PD-1/PD-L1 通路代表了一种有前景的协同策略,可克服 LUAD 中的免疫逃逸。
颗粒酶:T细胞抗肿瘤免疫的核心效应分子
01
颗粒酶是一类丝氨酸蛋白酶,储存在细胞毒性颗粒中,在细胞介导的免疫中作为细胞毒性 T 淋巴细胞(CTL)的关键效应分子发挥作用,在经典的抗肿瘤免疫反应中发挥着核心作用。当通过 T 细胞受体识别抗原时,CTL 会极化并释放这些颗粒进入免疫突触。随后,在穿孔素形成的靶细胞膜孔道的帮助下,颗粒酶被递送至细胞质中,诱导细胞凋亡。这种穿孔素依赖的细胞毒性途径构成了基于 T 细胞的免疫疗法的基础。
GZMK 抑制肽 ACYRFKCMK 在体内增强抗 PD-1 疗法的效果
02
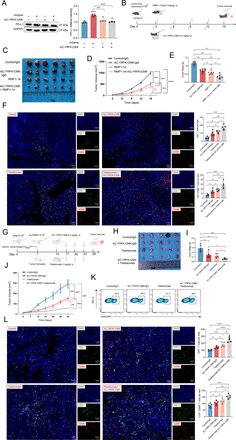
基于先前 AC-YRFK-CMK 是 GZMK 特异性抑制剂的证据,研究人员进一步探究了抑制 GZMK 信号传导是否能改善 LUAD 模型对 PD-1 抗体治疗的反应。体外实验首先表明,AC-YRFK-CMK 能有效阻断重组人 GzmK 诱导的肿瘤细胞 PD-L1 表达上调。为了评估其体内治疗潜力,研究人员在免疫功能正常的 C57BL/6 模型和人源化 NVSG 小鼠模型中进行了联合治疗实验。研究显示,与单药治疗组或对照组相比,GZMK 抑制肽 AC-YRFK-CMK 与抗 PD-1 抗体 PMP1-14 联合使用显著抑制了肿瘤生长,这从肿瘤体积曲线的减小和最终肿瘤重量的降低中可见一斑。免疫荧光分析进一步显示,联合治疗组肿瘤微环境中 CD8+T 细胞浸润显著增强,CD8+T 细胞中细胞毒性效应分子 GZMB 的表达也有所增加。这些发现表明,联合治疗同时促进了肿瘤细胞凋亡,增强了 CD8+T 细胞的细胞毒性功能,同时抑制了免疫逃逸和肿瘤增殖。
敲除 BPGM 可抑制体内肝细胞癌肿瘤生长
总之,通过其抑制肽特异性抑制 GZMK 活性与 PD-1 检查点阻断疗法协同作用,显著增强了 CD8+ T 细胞介导的抗肿瘤免疫反应,从而在体内模型中有效抑制肿瘤生长。
参考资料:
https://jitc.bmj.com/content/14/1/e013170#abstract-1(转化医学网360zhyx.com)
【关于投稿】
转化医学网(360zhyx.com)是转化医学核心门户,旨在推动基础研究、临床诊疗和产业的发展,核心内容涵盖组学、检验、免疫、肿瘤、心血管、糖尿病等。如您有最新的研究内容发表,欢迎联系我们进行免费报道(公众号菜单栏-在线客服联系),我们的理念:内容创造价值,转化铸就未来!
转化医学网(360zhyx.com)发布的文章旨在介绍前沿医学研究进展,不能作为治疗方案使用;如需获得健康指导,请至正规医院就诊。
责任声明:本稿件如有错误之处,敬请联系转化医学网客服进行修改事宜!
微信号:zhuanhuayixue
 腾讯登录
腾讯登录









还没有人评论,赶快抢个沙发