动脉粥样硬化治疗新选择!华西医院魏全/付琛颖团队首次系统揭示脉冲电磁场治疗动脉粥样硬化的分子机制,非药物、非侵入性治疗
| 导读 | 这一发现为心血管疾病治疗提供了全新思路:一种非药物、非侵入性的物理疗法可能成为未来动脉粥样硬化治疗的新选择。 |
近日,四川大学华西医院魏全/付琛颖团队一项发表于国际知名期刊《信号转导与靶向治疗》(Signal Transduction and Targeted Therapy,IF=52.7)的最新研究成果:首次系统揭示了脉冲电磁场(PEMFs)治疗动脉粥样硬化的分子机制。脉冲电磁场可通过调节细胞膜张力改善线粒体功能,从而抑制NLRP3炎症小体活化,减少内皮细胞焦亡,最终延缓动脉粥样硬化进展。这一发现为心血管疾病治疗提供了全新思路:一种非药物、非侵入性的物理疗法可能成为未来动脉粥样硬化治疗的新选择。
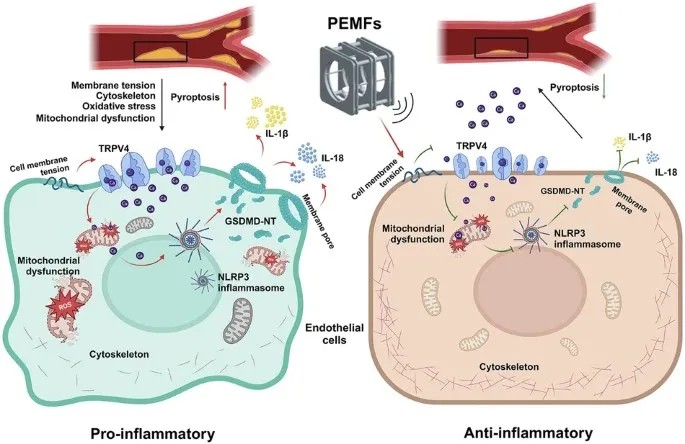
研究设计:脉冲电磁场的选择

脉冲电磁场(PEMFs)通过减轻细胞焦亡和炎症反应来抑制动脉粥样硬化斑块的形成
研究团队通过动物实验发现,15Hz/1.5mT的PEMFs参数方案效果最佳,能显著减轻动脉粥样硬化斑块形成,降低血管通透性,减少主动脉弓斑块面积。
在细胞实验中,PEMFs处理可显著恢复氧化低密度脂蛋白损伤的内皮细胞活力,降低乳酸脱氢酶释放,抑制炎症因子IL-1β、IL-18等的分泌。
进一步机制研究表明,PEMFs能抑制NLRP3炎症小体活化,减少gasdermin D(GSDMD,细胞焦亡的核心执行者)的切割活化,从而减轻内皮细胞焦亡。
核心机制一:细胞膜张力与机械敏感通道的关键作用
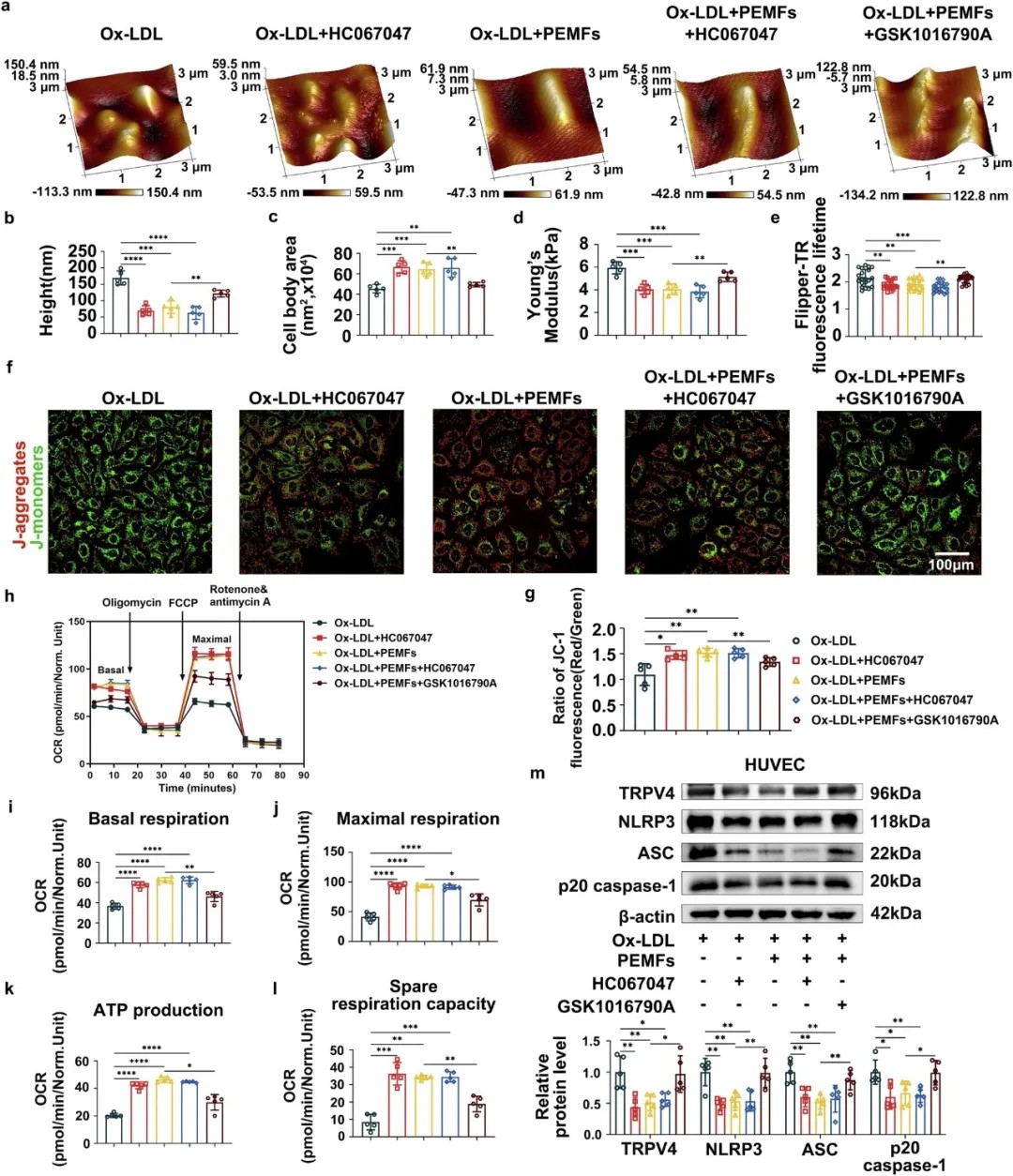
TRPV4的过度激活会加剧细胞僵硬和线粒体功能障碍,而抑制TRPV4则能赋予细胞保护作用
为探究外部电磁场影响细胞内线粒体的机制,研究人员从细胞膜机械力学角度进行了深入探索。
原子力显微镜结果显示,动脉粥样硬化环境下内皮细胞形态异常,表面粗糙度和细胞刚度增加,细胞膜张力显著升高。而PEMFs处理能有效逆转这些病理性的机械特性改变。
值得注意的是,研究人员发现机械敏感性离子通道TRPV4在这一过程中扮演关键角色。动脉粥样硬化条件下,TRPV4表达上调且对激动剂敏感性增加;而PEMFs能下调TRPV4的表达和功能。
核心机制二:从细胞膜到线粒体的信号传导
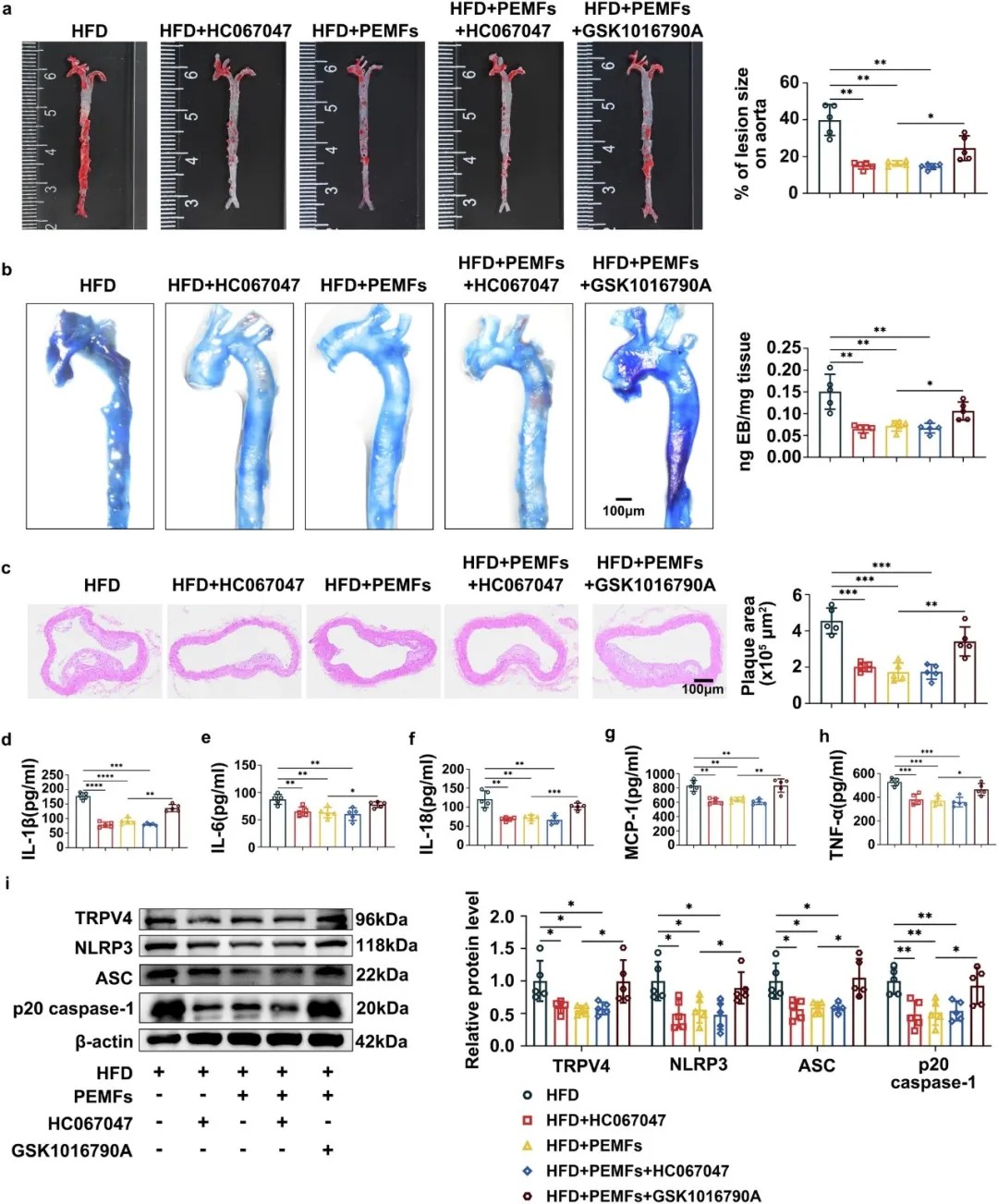
TRPV4的激活会加重动脉粥样硬化的发生,反之,抑制TRPV4则能产生与PEMFs相似的有益效果
研究人员进一步揭示了从细胞膜到线粒体的信号传导通路。研究表明,TRPV4活化会导致线粒体功能障碍,包括膜电位下降、活性氧产生增加、钙离子失衡和呼吸功能受损。脉冲电磁场通过调节细胞膜张力和TRPV4通道,有效改善线粒体功能,抑制NLRP3炎症小体活化,最终减少内皮细胞焦亡。
PEMFs首先通过调节内皮细胞膜张力,下调机械敏感TRPV4通道,进而修复线粒体功能障碍,从而抑制NLRP3炎症小体活化及其下游的GSDMD依赖性细胞焦亡。
这一机制不仅揭示了电磁场对动脉粥样硬化的治疗作用,也为理解机械生物学在血管疾病中的作用提供了新视角。
研究意义和未来展望
动脉粥样硬化是冠心病、脑梗死等缺血性心脑血管病的共同病理基础。据统计,中国心血管病现患人数高达3.3亿,平均每11秒就有一人因心血管病死亡。
随着脉冲电磁场等创新疗法的不断成熟,动脉粥样硬化治疗正迎来一些新的变化——从药物干预到物理调控,从局部治疗到全身调节,从单一靶点到多维度干预的转变,这些正在重塑心血管疾病的治疗格局。
原文链接:
https://www.nature.com/articles/s41392-025-02479-2(转化医学网360zhyx.com)
【关于投稿】
转化医学网(360zhyx.com)是转化医学核心门户,旨在推动基础研究、临床诊疗和产业的发展,核心内容涵盖组学、检验、免疫、肿瘤、心血管、糖尿病等。如您有最新的研究内容发表,欢迎联系我们进行免费报道(公众号菜单栏-在线客服联系),我们的理念:内容创造价值,转化铸就未来!
转化医学网(360zhyx.com)发布的文章旨在介绍前沿医学研究进展,不能作为治疗方案使用;如需获得健康指导,请至正规医院就诊。
责任声明:本稿件如有错误之处,敬请联系转化医学网客服进行修改事宜!
微信号:zhuanhuayixue
 腾讯登录
腾讯登录






还没有人评论,赶快抢个沙发