同济大学/苏州大学/复旦大学联合突破:肺癌靶向治疗发现关键分子调控新机制
| 导读 | PRC1是一种预后标志物,其在肺癌中具有低 DNA 甲基化的特点。 |
7月15日,同济大学/苏州大学/复旦大学研究团队合作共同在期刊《Journal of Experimental & Clinical Cancer Research》上发表了研究论文,题为“CCNY-mediated phosphorylation and TET2-BACH1-driven DNA demethylation activate PRC1 to augment NSCLC progression”,本研究发现PRC1 在非小细胞肺癌细胞中高表达。无论是沉默 PRC1 还是促进 PRC1 磷酸化的 CCNY,均会显著降低体外细胞生长,损害纺锤体形成,促进 G2/M 期细胞周期停滞,增加多核细胞,并削弱细胞的致瘤活性。此外,TET2 被发现通过与 BACH1 相互作用诱导 PRC1 的 DNA 去甲基化并激活其转录。抑制 TET2、BACH1 或 PLK1-PRC1 相互作用会削弱非小细胞肺癌细胞在体内的致瘤潜力。组织微阵列分析显示肿瘤组织中 CCNY、TET2 和磷酸化 PRC1 的水平升高。生物信息学分析表明,这些分子与非小细胞肺癌患者的不良预后相关。综上,本研究证明了 PRC1 在非小细胞肺癌(NSCLC)中具有关键的致癌作用。CCNY 调节 PRC1 的磷酸化,而 TET2-BACH1 级联反应调节 PRC1 的去甲基化和转录,它们可能成为 NSCLC 治疗的有前景的靶点。

https://jeccr.biomedcentral.com/articles/10.1186/s13046-025-03472-x#Sec29
背景知识
01
根据 2025 年的癌症统计数据,在美国,肺癌是第二常见的癌症,但却是癌症死亡的首要原因,其致死率几乎是排名第二的结直肠癌的 2.5 倍。非小细胞肺癌(NSCLC)约占所有肺癌诊断病例的 85%。可是,只有 20% 至 25% 的患者在早期被诊断出来,此时手术治疗仍有可能治愈。大多数患者在晚期才被确诊,错失了可能治愈的手术机会。在这种情况下,化疗、放疗、免疫治疗和分子靶向治疗等替代治疗策略,无论是单独使用还是联合使用,都是必要的,但其效果往往有限。令人担忧的是,即使在早期被诊断出来并接受了最佳治疗的患者,仍可能面临疾病复发和死亡的风险。因此,开发靶向更多致病基因的新型治疗药物的需求日益迫切。
用瑞贝治疗可降低 PRC1 磷酸化水平并抑制非小细胞肺癌细胞的生长
02
瑞贝已被确认为一种抗肿瘤药物,也是 CDK16 的拮抗剂,其作用机制在于破坏 CCNY 与 CDK16 的相互作用。为了评估瑞贝在非小细胞肺癌(NSCLC)中的治疗潜力,研究人员用不同剂量的瑞贝处理了 NSCLC 细胞系。PRC1 表达较高的 H1299 和 H1975 细胞对瑞贝治疗表现出更强的耐药性,这体现在这些细胞系中瑞贝的 IC50 值升高。此外,瑞贝处理导致 H1299 和 H1975 细胞中 PRC1 磷酸化水平呈剂量依赖性降低。体内实验也观察到了类似的结果。在由 H1299 细胞形成的裸鼠皮下异种移植瘤模型中,瘤内注射瑞贝显著抑制了肿瘤生长,降低了 KI67 和磷酸化 PRC1 的染色强度,并增强了 C-Cas3 的染色强度。
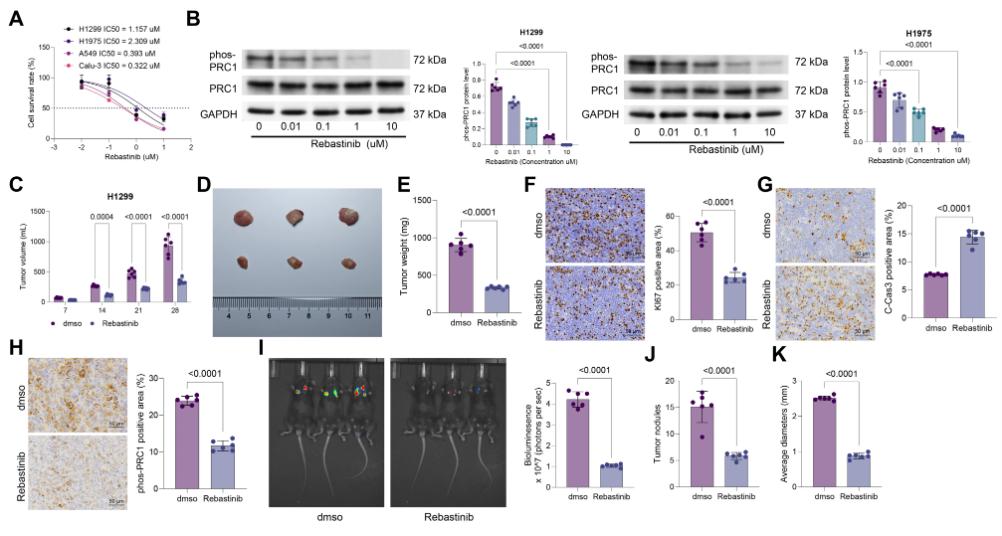
用瑞贝治疗可降低 PRC1 磷酸化水平并抑制非小细胞肺癌细胞的生长
为了更好地模拟肿瘤生长和免疫微环境,研究人员将荧光素酶转染到小鼠的 Lewis 肺癌细胞(3LL)中,并将其注射到免疫功能正常的 C57 小鼠的肺部。7 天后,通过尾静脉注射给予小鼠瑞贝(Reb),直至第 28 天。瑞贝的给药显著降低了小鼠的生物发光强度,表明肿瘤生长速度减缓。在终点时,瑞贝治疗组小鼠肺部肿瘤病灶的数量和大小均显著减少。
结论
03
总之,本研究证明了 PRC1 在非小细胞肺癌(NSCLC)中发挥着关键的致癌作用,通过驱动细胞分裂和肿瘤生长。研究强调了 TET2/BACH1 信号级联和 CCNY 是 NSCLC 中 PRC1 过度激活的关键调节因子。TET2 和 BACH1 促进 PRC1 的 DNA 去甲基化和基因转录,而 CCNY 则增强 PRC1 的磷酸化。这些发现为 NSCLC 进展的分子机制提供了新的见解,并为靶向治疗干预开辟了新的途径。(转化医学网360zhyx.com)
参考资料:
https://jeccr.biomedcentral.com/articles/10.1186/s13046-025-03472-x#Sec29
【关于投稿】
转化医学网(360zhyx.com)是转化医学核心门户,旨在推动基础研究、临床诊疗和产业的发展,核心内容涵盖组学、检验、免疫、肿瘤、心血管、糖尿病等。如您有最新的研究内容发表,欢迎联系我们进行免费报道(公众号菜单栏-在线客服联系),我们的理念:内容创造价值,转化铸就未来!
转化医学网(360zhyx.com)发布的文章旨在介绍前沿医学研究进展,不能作为治疗方案使用;如需获得健康指导,请至正规医院就诊。
责任声明:本稿件如有错误之处,敬请联系转化医学网客服进行修改事宜!
微信号:zhuanhuayixue
 腾讯登录
腾讯登录









还没有人评论,赶快抢个沙发