谭蔚泓院士创新突破:细菌搭载适配子-药物偶联物,开辟胰腺癌协同治疗新纪元
| 导读 | 在这项研究中,团队提出了一种协同疗法方法,该方法通过将ApDC与VNP20009结合,将细菌的渗透能力与ApDC的靶向和毒性作用相结合。 |
2024年10月14日,上海交通大学医学院附属仁济医院谭蔚泓院士团队在期刊《Signal Transduction and Targeted Therap》上发表了题为“Aptamer-drug conjugates-loaded bacteria for pancreatic cancer synergistic therapy”的研究论文。研究结果表明,与游离药物组相比,该方法将ApDC的血清稳定性延长至48小时,并导致肿瘤部位的药物浓度增加。此外,适配体与癌细胞的靶向结合,使肿瘤部位的细菌定植增加了两倍,导致肿瘤细胞死亡和T细胞浸润增加。该策略利用了细菌和ApDC,因此,为胰腺癌治疗提供了一种有效的协同策略。

https://www.nature.com/articles/s41392-024-01973-3
关于胰腺癌
01
胰腺癌独特的微环境,对其治疗提出了额外的挑战。大约70%的胰腺癌患者表现出“致密”的肿瘤微环境,其特征是高浓度的致密结缔组织和细胞外基质。这不仅会阻碍有效的药物输送,还可能削弱化疗和其他治疗方式的有效性。
近年来,药物递送方法取得了重大进展,特别是通过战略性地使用核酸适配体。这一进展导致了适配子-药物偶联物(ApDC)的开发,这是一种创新结构,巧妙地将适配子的靶向精度与药物有效载荷的治疗效果相结合。其中一种有效载荷是单甲基 Auristatin E(MMAE),这是一种微管蛋白抑制剂,可破坏微管动力学,导致细胞周期停滞在G2/M期和随后的细胞凋亡。MMAE在构建ApDC(适配子-药物偶联物)中的应用,已在靶向癌症治疗中显示出前景。
为了克服胰腺癌治疗中的重大挑战,团队提出了一种新的协同疗法,利用细菌和适配体-药物偶联物(ApDC)的互惠互利。团队将ApDC共价连接到VNP20009表面,确保治疗剂更有效地到达肿瘤并保持稳定,从而优化药物输送、增强治疗效果,并激活靶向免疫反应。这种双功能方法为胰腺癌的治疗,提供了一个有前途的新方向。
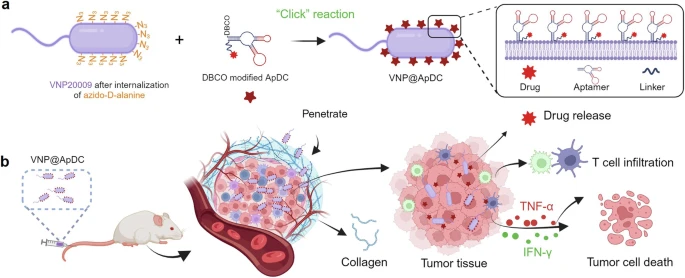
功能化细菌的构建和对抗胰腺肿瘤的机制。
VNP@ApDC穿透诱导的肿瘤微环境改善
02
团队观察到注射VNP@Sgc8c-MMAE后,肿瘤中枢T细胞富集。与对照组相比,VNP@Sgc8c-MMAE组的CD4 T细胞和CD8 T细胞数量是对照组的3-4 倍,与In Vivo靶向结果一致。
VNP@Sgc8c-MMAE不仅通过增加细胞毒性和辅助性T细胞群来增强抗肿瘤免疫力,而且还可能通过修饰肿瘤基质以减轻免疫细胞浸润的障碍,突出了其作为强大免疫治疗策略的潜力。
这些发现与细菌定植和ApDC渗透的结果一致,证实了细菌-ApDC复合物在这些模型中的协同作用。
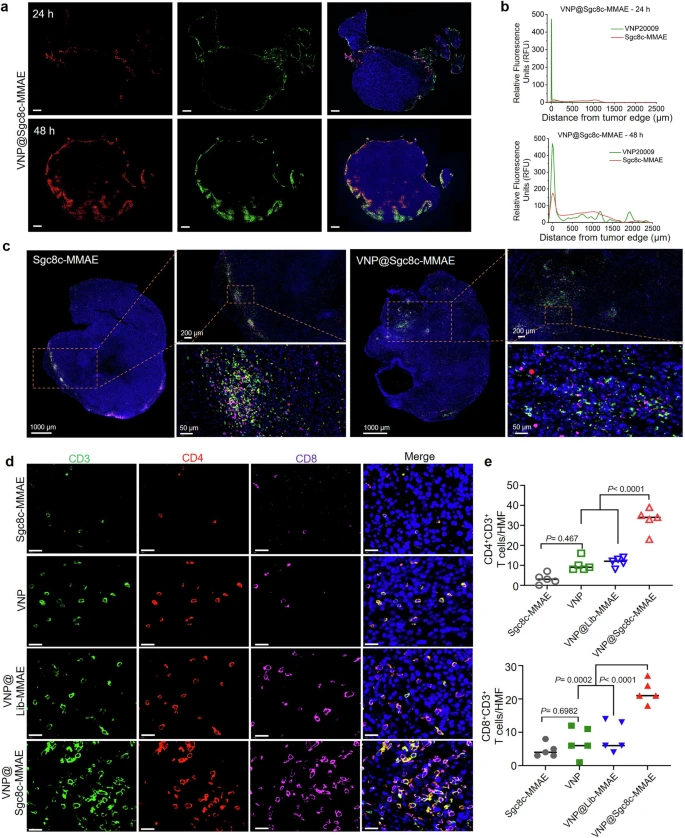
胰腺癌组织中,免疫反应和药物递送的多方面分析。
VNP@ApDC的体内协同治疗疗效
03
与对照组相比,用VNP@Sgc8c-MMAE处理的肿瘤组织中,CD45免疫细胞的浸润显著增加,表明细菌载体促进了强大的免疫反应。CD4 T细胞分析显示,VNP@Sgc8c-MMAE处理组浸润增强,CD4 Tregs显著减少,表明肿瘤微环境中免疫抑制细胞群减少。在用VNP@Sgc8c-MMAE治疗的肿瘤中,成熟树突状细胞(CD11cMHCII)显著增加,表明抗原呈递能力增强。VNP@Sgc8c-MMAE组中M1型与M2型巨噬细胞的比例增加,M1巨噬细胞更普遍,M2巨噬细胞较少,表明向促炎巨噬细胞表型的转变。
CD8 T细胞表现出较高的GzmB、T-bet、IFN-γ和TNF-α表达,表明细胞毒活性增强,Th1免疫反应更强。这些发现表明,VNP@Sgc8c-MMAE有效增强免疫细胞浸润和功能性抗肿瘤免疫,通过多种机制促进免疫激活,以发挥抗肿瘤功能。

VNP@Sgc8c-MMAE激活抗肿瘤免疫。
总结
04
1. 转移性肿瘤的潜在疗效:推测VNP@Sgc8c-MMAE在转移性肿瘤中也可能有效,需要进一步研究来验证疗效和安全性。
2. 给药途径的探索:探索口服给药和粪便移植等替代给药途径。
3. 优化和联合疗法:未来的研究将侧重于优化菌株、改进适配子设计、探索给药途径和联合疗法。
4. 治疗策略的前景:该研究提出的治疗策略可能对胰腺癌治疗产生重大影响,克服当前治疗中的挑战。
参考资料:
1. Bazeed, A. Y., Day, C. M. & Garg, S. Pancreatic cancer: challenges and opportunities in locoregional therapies. Cancers 14, 4257 (2022).
2. Springfeld, C. et al. Neoadjuvant therapy for pancreatic cancer. Nat. Rev. Clin. Oncol. 20, 318–337 (2023).
 腾讯登录
腾讯登录









还没有人评论,赶快抢个沙发