【Cell子刊】南京医科大学团队:肿瘤内微生物群是肾透明细胞癌有潜力的预后生物标志物
| 导读 | 这项研究旨在使用来自The Cancer Genome Atlas的RNA-Seq数据,来表征肾透明细胞癌的微生物景观和特征。 |
2024年9月22日, 南京医科大学第一附属医院Sun Lejia团队在期刊《Heliyon》上发表了题为“Tumor microbiota of renal cell carcinoma affects clinical prognosis by influencing the tumor immune microenvironment”的研究论文。基于微生物组的亚型揭示了肿瘤微生物组、临床预后和肿瘤微环境之间的相关性,表明肿瘤内微生物群是肾透明细胞癌有潜力的预后生物标志物。

https://www.cell.com/heliyon/fulltext/S2405-8440(24)14341-1
研究背景
01
迄今为止,癌症仍然是一个主要的全球健康问题,肾细胞癌(RCC)在所有癌症类型中排名第10。大约30%的RCC患者在晚期被诊断出来,5年生存率仅为10%。由于对常规放疗和化疗缺乏敏感性,转移性肾透明细胞癌(KIRC)是最常见的RCC 亚型,患者接受免疫治疗和靶向治疗作为一线治疗。最近的研究表明,微生物群在包括RCC在内的多种癌症的进展和治疗反应中,起着重要作用。
尽管瘤内微生物组已经在各种癌症中得到表征,但与RCC特异性相关的微生物组,仍未得到充分研究。尿路感染已被确定为RCC发展的可改变危险因素。2022年的一项研究,揭示了细菌载量与PU.1巨噬细胞之间存在负相关关系,为了解细菌如何影响RCC相关免疫细胞的表型提供了见解。
在这项研究中,KIRC转录组测序数据和患者临床数据来自癌症基因组图谱(TCGA)数据库。随后,团队在长期总生存期(OS)与短期总生存期(OS)患者之间鉴定出差异丰富的微生物,并构建基于Cox回归的风险评分特征。团队进行了进一步的分析,包括差异基因表达和基因集富集,以阐明这些风险相关微生物影响肿瘤免疫反应和疾病预后的潜在免疫原性机制。
研究进展
02
已鉴定的预后相关微生物与免疫相关基因具有显著相关性
通过特别关注免疫相关基因,团队确定了30个感兴趣的基因。其中,24个基因在高危人群中上调,主要与抗菌功能、炎症和自然免疫有关。示例包括PI3、LBP、IFNG和趋化因子相关基因CXCL5、SAA1和SAA2,这些基因可能在驱动炎症反应和肿瘤发展中发挥关键作用。相反,在高危组中,有6个基因下调,主要与适应性免疫有关。值得注意的例子是免疫球蛋白家族基因,如IGKV1-16、IGKV1D-17和IGKV2D-24,它们可能参与针对肿瘤的适应性免疫反应。
大多数微生物相关基因与鉴定的免疫相关基因呈负相关,并参与抗菌反应、炎症诱导、先天免疫和肿瘤促进。相反,与免疫相关基因呈正相关的微生物相关基因,主要表现出与抗体结合、适应性免疫诱导和肿瘤抑制相关的功能。这表明与免疫相关基因呈负相关的微生物,可能通过促进抗菌反应、炎症和自然免疫,导致患者预后变差;而与此类基因呈正相关的微生物,可能会增强适应性免疫,从而获得更好的患者预后。
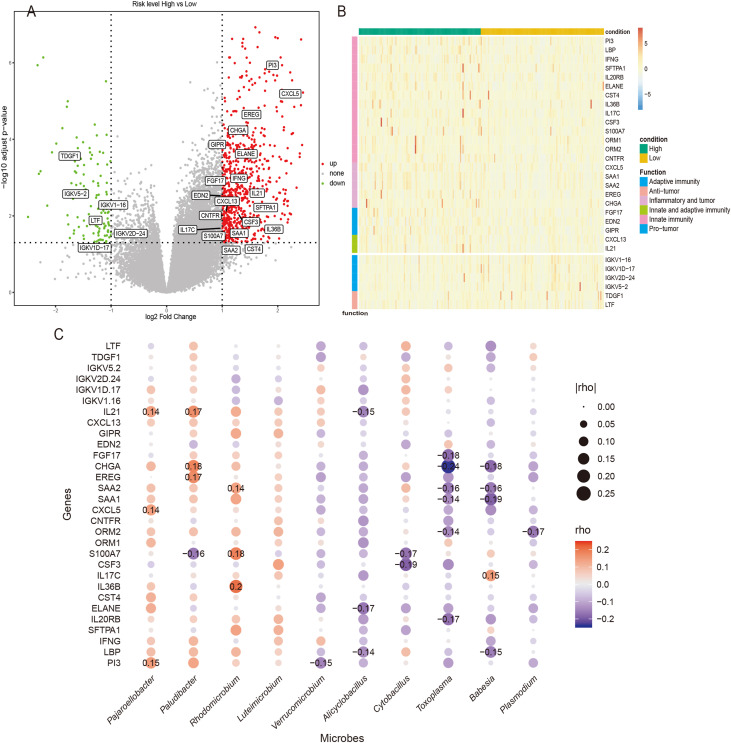
差异丰度微生物与免疫功能基因相关
基于微生物的风险评分可以将患者分为两个不同的组,其特征是免疫细胞功能不同
上调的基因富含与急性反应、炎症反应、抗菌免疫和表皮细胞分化相关的功能,这些功能与肿瘤生长有关,而下调的基因与免疫球蛋白复合物和离子转运过程有关。上调的基因通路是那些参与表皮生长、核分裂、趋化因子、抗菌反应和急性炎症的基因通路,而下调的基因通路参与抗体结合、离子转运和适应性免疫反应。
不良预后相关微生物与单核细胞、巨噬细胞和肥大细胞活性有关,它们在诱导先天性炎症反应中起关键作用。相反,阳性预后相关微生物与B细胞和T细胞相关,B细胞和T细胞是适应性免疫反应的关键参与者。
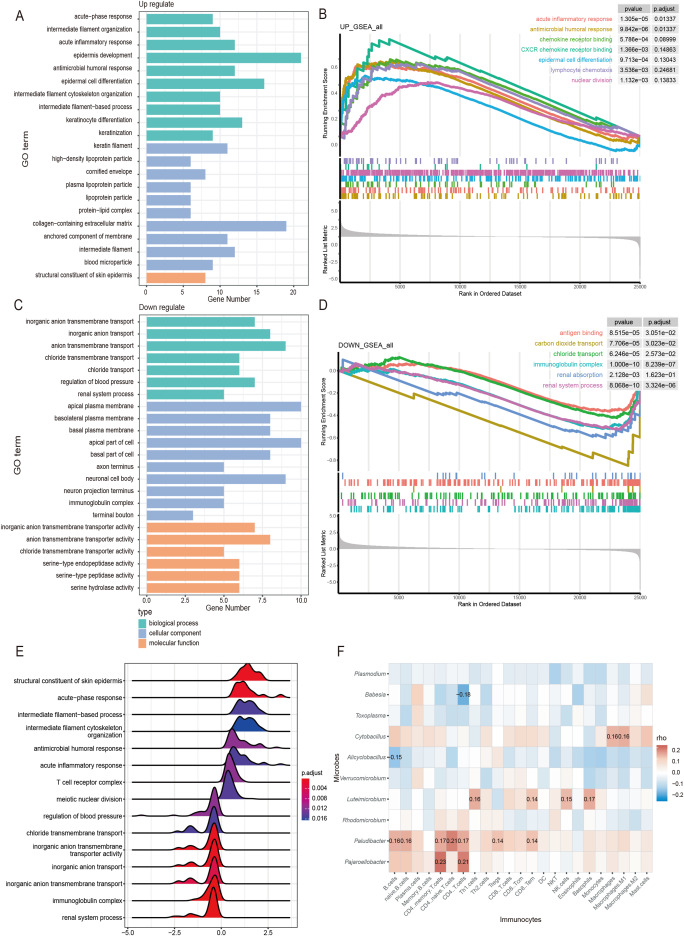
生存风险评分区分具有不同免疫相关特征的高危和低危患者
研究结论
03
这项研究提出了几个关键的见解。首先,与邻近非肿瘤组织的比较分析表明,肿瘤微生物群的α和β多样性降低,微生物组成不同。此外,团队确定了10个在总生存期长和短患者之间显著不同的微生物属,并用于制作基于微生物组的预后风险特征。这种特征有助于识别2种不同的微生物组驱动的亚型,这些亚型与不同的临床结果和免疫微环境相关:4种高危微生物与促肿瘤急性炎症有关,而6种低风险微生物激活过继免疫以阻止肿瘤进展。
总之,微生物群、预后和肿瘤免疫之间的关联,突出了利用肿瘤内微生物群作为预后生物标志物的潜力。未来的关键方面,包括阐明肿瘤内微生物群与肿瘤微环境相互作用的基本机制,并确定关键微生物作为潜在的治疗靶点。此外,需要真实世界的临床研究,来证实这些微生物在预测患者预后和优化免疫治疗反应方面的实际效用。
参考资料:
1.Xue, C. ∙ Chu, Q. ∙ Zheng, Q. ...
Current understanding of the intratumoral microbiome in various tumors
Cell Rep Med. 2023; 4, 100884
2.Siegel, R.L. ∙ Miller, K.D. ∙ Jemal, A.
Cancer statistics
CA Cancer J Clin. 2019; 69:7-34 2019
 腾讯登录
腾讯登录









还没有人评论,赶快抢个沙发