迈杰医学支持PARP抑制剂尼拉帕利临床研究数据亮相ESGO
| 导读 | 迈杰医学MEDx HRDetectCDx panel适用于检测中国卵巢癌患者的HRD。 |
在2024年3月7日-10日欧洲妇科肿瘤学会(ESGO)年会上,迈杰医学与中国医学医科院肿瘤医院妇科吴令英教授合作发表了题为”MEDx HRDetectCDx Predicts The Response Of Newly Diagnosed Advanced Ovarian Cancer Patients In China To First-Line Maintenance Treatment With Niraparib”的ePoster。数据显示,迈杰医学HRD检测产品:MEDx HRDetectCDx panel在分析性能上与Myriad myChoice CDx展现出高度一致性。 同时,在国内22家中心参与的真实世界前瞻性研究中,证实了MEDx HRDetectCDx与尼拉帕利在初诊晚期卵巢癌患者一线维持治疗中疗效的相关性。研究还显示SLX4基因在中国人群中突变频率与BRCA1接近且与预后相关,后续基础功能的深入开展将进一步验证SLX4基因的重要性。这些发现为精确治疗决策和探索HRD的分子机制提供了新的视角。
背 景
同源重组缺陷(Homologous Recombination Deficiency, HRD)是DNA修复途径缺陷的结果,会造成基因组和染色体的不稳定。HRD阳性常见于卵巢癌患者中,是卵巢癌聚腺苷二磷酸核糖聚合酶抑制剂(PARP inhibitor, PARPi)治疗相关的重要生物标志物之一。
在初诊晚期卵巢癌患者中,HRD检测对于患者使用PARPi一线(1L)维持治疗疗效的预测价值已通过随机对照试验得到证实。然而,关于HRD的预测价值在真实世界的研究中一直很有限。迈杰医学开发了专为中国人群设计的MEDx HRDetectCDx panel,用于检测HRD。通过与金标准Myriad Mychoice CDx比较对其分析性能进行了评价, 并在中国的一项前瞻性、多中心真实世界RENI-1研究(NCT04986371)中验证了该Panel对PARPi一线维持治疗疗效预测价值。其他同源重组修复(Homologous Recombination Repair, HRR)基因突变及其与疗效和预后的相关性也进行了探讨。
方 法
MEDx HRDetectCDx 测试通过捕获法靶向测序约 42,000 个特定于中国人群的全基因组单核苷酸多态性(SNP),覆盖度约为 ±200x,并对 85 个基因的编码外显子进行了约 ±400x 的覆盖度测序。通过分析LOH、TAI和LST,计算HRD评分。分值≥43(阈值)时判定HRD为阳性。并通过与Myriad myChoice CDx比较来评估HRDetectCDx的分析性能。
在前瞻性RENI-1真实世界研究中评估了HRD评分对尼拉帕利疗效的预测性。该研究招募了来自中国22个中心的卵巢癌患者,这些患者在2021年至2022年间接受尼拉帕利作为1L维持治疗。PFS数据截止日期为2023年10月18日。与疗效相关的分子特性也进行了探索性研究。
结 果
1.MEDx-HRDetectsCDx与Myriad test具有高度一致性
HRDetectCDx panel和myChoice CDx 之间的阳性一致率为89.5%,阴性一致率是93.3%,总体一致率是91.2%(表1)。
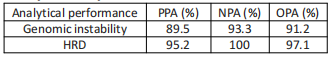
表1:Analytical performance comparison of the MEDx HRDetectCDx and Myriad assays
2.患者特征和HRD评分分布
227名符合条件的患者入选,122名患者接受了HRDetectCDx测试,其中92名可评估HRD状态。20名患者(16.4%)携带BRCA 突变(BRCA mutation, BRCAm),53名患者(43.4%)HRD阳性(表2)。
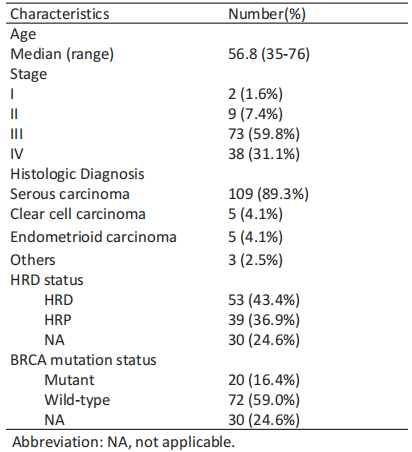
表2:Clinical characteristics of patients (n=122)
16.4%(20/122)的患者中发现了胚系与体系 BRCA1/2突变,包括BRCA1的13个突变和BRCA2的7个突变。其中,13名患者显示BRCA1/2突变,且HRD评分大于43(图1)。


图1:HRD scores and BRCA mutation distributions A. HRD (GIS) score distribution. B-C. Distribution of mutations detected in the BRCA1 and BRCA2 genes, with sticks indicating the locations of these mutations.
3.BRCA突变和HRD状况与无进展生存期(Progress Free Survival, PFS)的关系
HRD组及同源重组修复正常组(homologous recombination proficient, HRP)的PFS分别为未达到(not reached, NR)及14.4个月(HR 0.51;95%CI 0.27–0.97)。在HRD组中,BRCAm患者的PFS为NR,BRCAwt/HRD患者的PFS为18.1个月(HR 0.46;95% CI 0.15-1.39)(图2)。

图2:PFS analysis in patients with different BRCA and HRD statuses PFS analysis of patients in the BRCA mutation subgroup vs. wild-type subgroup (A), HRD subgroup vs. HRP subgroup (B), and BRCAm subgroup vs. BRCAwt/HRD subgroup vs. HRP subgroup (C).
4.HRR基因突变与PFS和疾病进展的关系
突变频率较高的基因包BRCA1(14%)、PALB2(9%)、BRCA2(8%)、ARID1A(7%)、PTEN(5%)、BRIP1(4%)和ATRX、FANCL和SLX4(每个基因的突变频率为3%)。特别是当可能致病和不确定意义的变异(variant of uncertain significance, VUS)基因突变被包括在内时,SLX4基因的突变频率高达16%,超过了BRCA1基因的突变频率(15%)(图3)。

图3:Gene mutation landscape of the HRDetectCDx panel
PFS分析显示,与野生型SLX4患者相比,SLX4基因中可能致病或VUS突变的患者预后更差(图4A-C)。SLX4基因中的大多数可能致病和VUS突变分布在其功能尚未确定的区域(图4D)。


图4:PFS analysis of patients in subgroups with different SLX4 statuses and SLX4 mutation distributions PFS analysis in the SLX4 mutation subgroup (pathogenic and VUS) vs. wild-type subgroup within the HRD cohort (A), the HRP cohort (B), and the whole cohort (C). D, Distribution of detected SLX4 mutations.
结 论
迈杰医学 MEDx HRDetectCDx Panel适用于检测中国卵巢癌患者的HRD状态,其预测无进展生存期的能力也在真实世界研究中得到了确认,有效预测了具有不同 BRCA和HRD状态的卵巢癌患者的预后。SLX4基因中可能致病或VUS的变异频率相对较高,这些突变与使用尼拉帕利一线维持治疗的卵巢癌患者预后较差相关。这些发现将促使进一步研究,以便为制定个性化治疗方案和深入了解HRD的分子机理提供新的认识。
参考文献
[1] Ning Li et al. Treatment with Niraparib maintenance therapy in patients with newly diagnosed advanced ovarian cancer a phase 3 randomized clinical trial. JAMA Oncol 2023; 9(9): 1230-1237.
[2] González-Martín A et al. Niraparib in Patients with Newly Diagnosed Advanced Ovarian Cancer. N Engl J Med. 2019; 381(25): 2391-2402.
[3]Loverix L et al. PARP inhibitor predictive value of the Leuven HRD test compared with Myriad MyChoice CDx PLUS HRD on 468 ovarian cancer patients from the PAOLA-1/ENGOTov25 trial. Eur J Cancer. 2023; 188: 131-139.
[4]Mosele F et al. Trastuzumab deruxtecan in metastatic breast cancer with variable HER2 expression: the phase 2 DAISY trial. Nat Med. 2023; 29(8): 2110-2120.
致谢
感谢再鼎医药(上海)有限公司对本研究的支持。

迈杰转化医学研究(苏州)有限公司(以下简称为:迈杰医学)于2013年成立,前身为QIAGEN转化医学研究中心。作为伴随诊断整体解决方案领导者,拥有综合转化医学技术支持药物临床转化、伴随诊断产品(CDx)开发和用药指导检测三大业务,基于基因组学、蛋白组学、细胞组学,病理组学以及大数据与AI等综合技术平台,一流的产品开发团队与完善的研发流程,以及完善的质量体系(涵盖CAP、CNAS ISO 17025、ISO13485、GMP、GSP等), 迈杰医学围绕靶向治疗,免疫治疗及细胞/基因治疗,赋能药物临床转化研究并开发对应的伴随诊断产品,支持药物上市后的精准用药。迈杰医学已与全球300+创新药企及技术公司展开合作,已开发验证了数百个生物标记物及方法学,支持上百个药物临床试验。截至目前共有20+款产品获得药监批准,涵盖实体肿瘤和血液肿瘤,其中包括国内首个获批的JAK2-V617F突变检测试剂盒及用于免疫治疗的PDL-1检测试剂盒;以及8款CE认证产品。同时,迈杰医学有40多款在研 CDx/IVD产品管线其中有10个正在临床试验中。基于独创的一体化商业模式,迈杰医学已迅速发展成为中国伴随诊断整体解决方案创新企业,解决创新药物的研发痛点及患者的用药痛点,助力精准医疗。
 腾讯登录
腾讯登录







还没有人评论,赶快抢个沙发