再取进展!浙江大学徐骁等团队合作发现肝细胞癌转移调控新机制
| 导读 | 最近的研究表明,环状RNA(circRNA)介导的RNA结合蛋白(RBP)翻译后修饰在肝细胞癌(HCC)的转移中起着关键作用。然而,尚不清楚其潜在作用机制和临床治疗意义。 |
2月15日,浙江大学徐骁及Chen Ronggao共同在期刊《Advanced Science》上发表了题为“Integrated Multiomics Reveals Silencing of has_circ_0006646 Promotes TRIM21-Mediated NCL Ubiquitination to Inhibit Hepatocellular Carcinoma Metastasis”的研究论文,该研究使用多组学方法描绘circRNA和RBP的调控网络。Has_circ_0006646(circ0006646)是一种未报道的HCC circRNA,与预后不良相关,circ0006646沉默能够明显抑制体内转移。总体而言,该研究描述了circRNA介导的NCL泛素化降解在HCC转移中的综合多组学景观,并提供了一个新的治疗靶点。

https://onlinelibrary.wiley.com/doi/10.1002/advs.202306915
研究背景
01
肝细胞癌(HCC)占大多数原发性肝癌(75 - 85%),是第六大最常诊断的癌症,并已被公认为全球癌症相关死亡的第三大原因。尽管在过去的70年里,化疗、靶向药物、免疫治疗以及手术切除和肝移植(LT)等全身疗法发展迅速,但HCC的5年生存率仍然不容乐观。
转移和复发,或治疗抵抗的后果共同决定了致命的HCC结果。转移作为肿瘤细胞在全身的扩散和增殖,被证实是直接影响实体肿瘤患者5年生存率的主要因素,其范围为5 ~ 30%。微血管浸润(MVI)被认为是转移的起始阶段,它的存在会影响手术的有效性。因此,作为转移的初始步骤,破译MVI发生的分子机制尤为关键。
研究进展
02
为了验证circ0006646对转移能力的影响,研究人员首先测量了circ0006646在HCC细胞系和人正常肝细胞系(THLE-2)中的表达水平。与正常细胞系(THLE-2)相比,在HCC细胞系中观察到circ0006646的表达显著增加。研究人员设计了两个sirna覆盖circ0006646的后接位点。转染两种sirna后,circ0006646的表达被沉默,而PTK2的表达未被沉默,这意味着sirna精确地靶向circ0006646而不是其亲本基因。
此外,上皮-间充质转化(epithelial-to-mesenchymal transition, EMT)是上皮细胞向间充质表型的转化,是转移过程中最经典的变化之一。在本研究中,当circ0006646被沉默时,被认为是EMT标志物的E cadherin和vimentin的表达水平分别升高和降低。这些变化随后通过免疫组织化学(IHC)染色和免疫荧光(IF)测定证实。综上所述,circ0006646沉默抑制HCC的侵袭和迁移。
另外,研究人员还构建了HCC PDX模型。通过侵袭实验,研究人员发现circ0006646沉默也能抑制原发性HCC细胞的转移能力。此外,NCL、p53、E cadherin的蛋白水平变化与HCC细胞系的结果一致。在应用PDX模型证实circ0006646是HCC患者的潜在治疗靶点后,研究人员模拟临床全身治疗,将sh-circ0006646或shNC慢病毒(两次注射,间隔一周)注射到小鼠尾静脉,在小鼠脾脏注射荧光素酶标记的HCCLM3细胞。注射sh-circ0006646慢病毒可降低体内HCC细胞的转移能力,通过降低荧光强度、减少转移和缩小肿瘤面积来测量。总之,circ0006646是一个具有临床转化价值的治疗靶点。
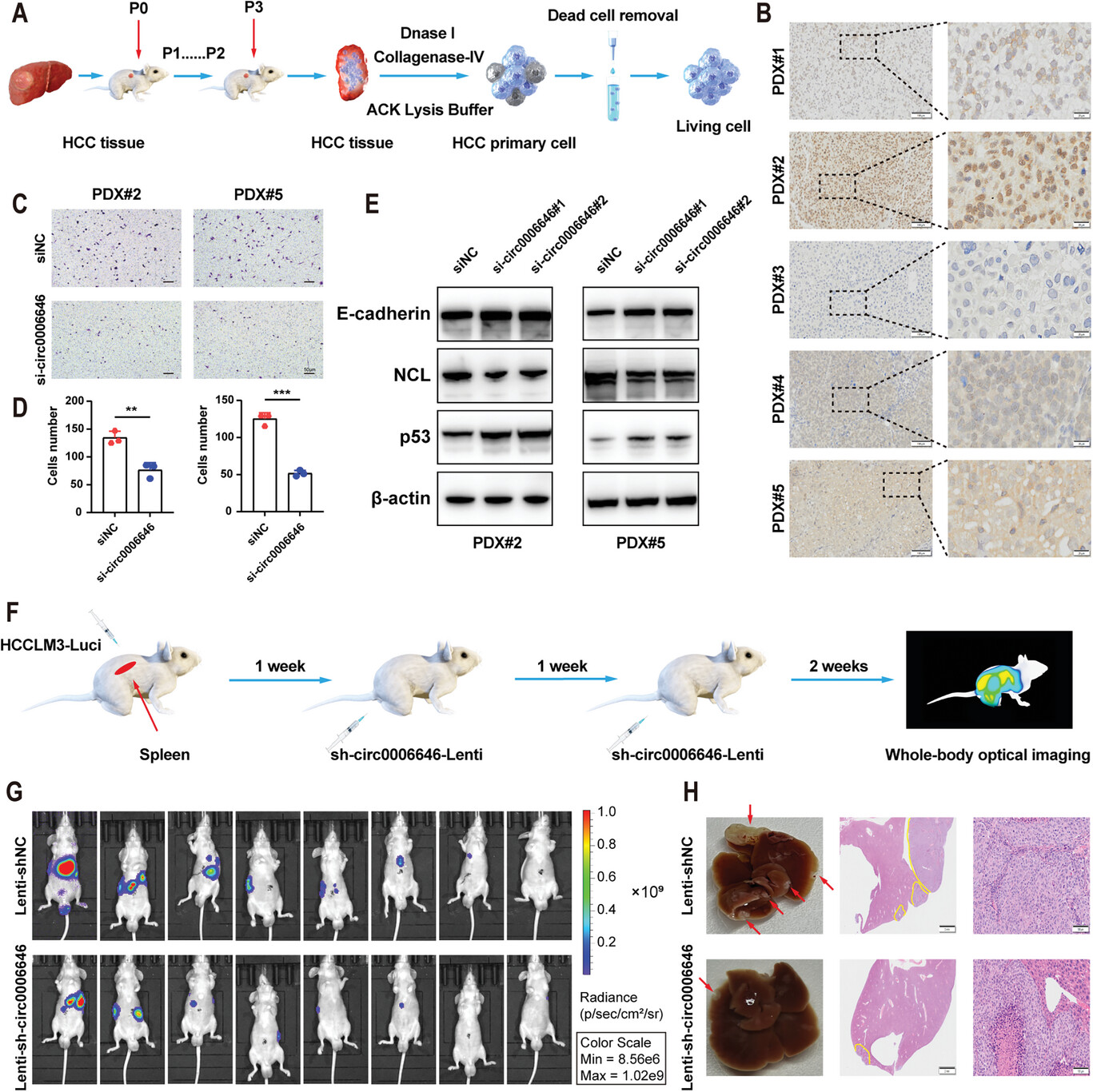
Circ0006646可能是治疗肝癌转移的潜在靶点
研究结论
03
综上所述,本研究描述了circrna介导的NCL泛素化降解在HCC转移中的综合多组学景观。Circ0006646是一种在肝细胞癌中表达上调的新RNA,可通过抑制K48泛素化稳定表达NCL促进肝细胞癌转移。P53通路在这一介导EMT发生的生物学过程中发挥了重要作用。(转化医学网360zhyx.com)
参考资料:
https://onlinelibrary.wiley.com/doi/10.1002/advs.202306915
注:本文旨在介绍医学研究进展,不能作为治疗方案参考。如需获得健康指导,请至正规医院就诊。
 腾讯登录
腾讯登录









还没有人评论,赶快抢个沙发