双重疗效!苏州大学最新研究:揭秘促进结直肠癌的有氧糖酵解和癌症进展的分子机制
| 导读 | HES1/IGF2BP2/GLUT1轴介导的有氧糖酵解的治疗干预可能是阻止CRC进展和转移的新策略。 |
11月13日,苏州大学陈卫昌、石通国等在期刊《Cell Death Discovery》上发表题为“HES1 promotes aerobic glycolysis and cancer progression of colorectal cancer via IGF2BP2-mediated GLUT1 m6A modification”的研究论文,研究证实,HES1在结直肠癌(CRC)患者中过表达,并与恶性行为有关。此外,HES1敲低通过以IGF2BP2依赖性方式降低m6A修饰的GLUT1 mRNA的稳定性来抑制CRC细胞的增殖、转移和有氧糖酵解。因此,HES1/IGF2BP2/GLUT1轴介导的有氧糖酵解的治疗干预可能是阻止CRC进展和转移的新策略。

https://www.nature.com/articles/s41420-023-01707-4#Abs1
研究背景
01
结直肠癌(CRC)是一种常见的消化道恶性肿瘤,严重威胁着人类的生命和健康。根据癌症统计分析,中国将有超过59,000例新发结直肠癌病例。CRC的晚期诊断和高转移率是导致死亡的主要原因。尽管多学科治疗和靶向免疫治疗等治疗取得了进展,但CRC患者的5年总生存率仍然很低。因此,深入研究CRC进展的分子机制有望改善CRC患者的预后。
代谢重编程是癌细胞的一个重要标志。有氧糖酵解是一种现象,即使在常氧环境中,肿瘤细胞也喜欢通过消耗大量葡萄糖来满足其能量需求,同时产生乳酸。糖酵解增强主要是由于肿瘤细胞中糖酵解相关基因的表达或活性增加。例如,葡萄糖转运蛋白1(GLUT1),顾名思义,将葡萄糖转运到细胞质中,启动糖酵解。研究表明,GLUT1在各种类型的肿瘤组织中高表达,并且与不良的临床结局有关。大量证据表明,异常的糖酵解水平会促进癌细胞的增殖和转移,但调节有氧糖酵解的分子机制尚未阐明。
作为转录因子,毛茸茸的分裂同源物-1(HES1)是螺旋-环-螺旋结构蛋白家族的重要成员之一,在细胞分化、增殖等生理过程中起着关键作用。在病理学上,HES1在胰腺癌、结直肠癌和非小细胞肺癌等多种癌症中高表达,这些癌症与不良结局相关。Li等人指出,在三阴性乳腺癌中,HES1通过转录激活Slug表达调节乳腺癌干细胞(BCSC)自我更新、BCSC群体和癌细胞增殖。此外,HES1过表达通过促进上皮-间充质转化(EMT)和诱导ABC转运蛋白基因(包括ABCC1、ABCC2和P-gp1)的表达,增强了CRC对5-氟尿嘧啶的化疗耐药性。上述研究结果表明,HES1对肿瘤进展具有重要作用。然而,HES1在CRC中的作用和潜在的分子机制仍不明确。
研究进展
02
我们使用 GEO 和 TCGA 数据集研究了 CRC 患者组织样本中 HES1 的 mRNA 表达。结果显示,HES1在CRC肿瘤组织中高表达(图1A)。随后,我们通过 IHC 测定检查了我们队列中 CRC 患者标本中 HES1 的蛋白表达。如图1B、C所示,与相应的正常癌旁组织相比,肿瘤组织中HES1的蛋白水平显著升高。此外,还研究了结直肠癌患者HES1表达与临床病理特征的关系。晚期(III期和IV期)结直肠癌患者的HES1水平远高于早期(I.期和II.期)患者。此外,与无淋巴结转移的患者相比,有淋巴结转移的CRC患者的HES1水平更高。重要的是,HES1高表达的CRC患者的预后较差(图1D)。此外,我们观察到大多数CRC细胞系(HCT8、HCT116和HT29)中的HES1表达明显高于结肠上皮细胞系NCM-460中的表达(图1E,F)。基于这些结果,HES1 在 CRC 患者和 CRC 细胞系中的表达均增加,并且 HES1 表达的增加与 CRC 的进展有关。
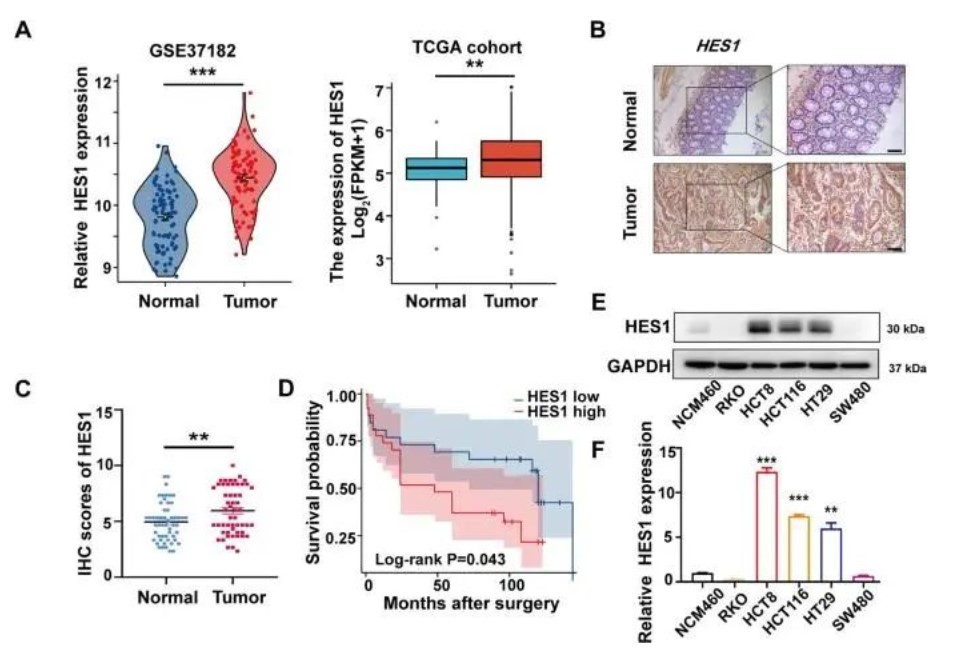
HES1 在 CRC 组织中高表达,与 CRC 患者的不良预后呈正相关。
研究结果
03
本研究,我们发现HES1在CRC组织中的表达明显高于邻近正常组织。此外,HES1 高表达与 CRC 患者的生存率低相关。HES1敲低在体外和体内均显著抑制细胞生长和转移。此外,HES1 的沉默抑制了 CRC 细胞的有氧糖酵解。机制研究表明,HES1敲低降低了结直肠癌细胞中需氧糖酵解的关键基因GLUT1的表达。GLUT1过表达消除了HES1敲低对细胞需氧糖酵解、增殖、迁移和侵袭的影响。ChIP-PCR和双荧光素酶报告基因检测结果显示,HES1直接结合IGF2BP2启动子,促进IGF2BP2表达。此外,我们的数据表明,IGF2BP2识别并结合了GLUT1 mRNA中的m6A位点,并增强了其稳定性。
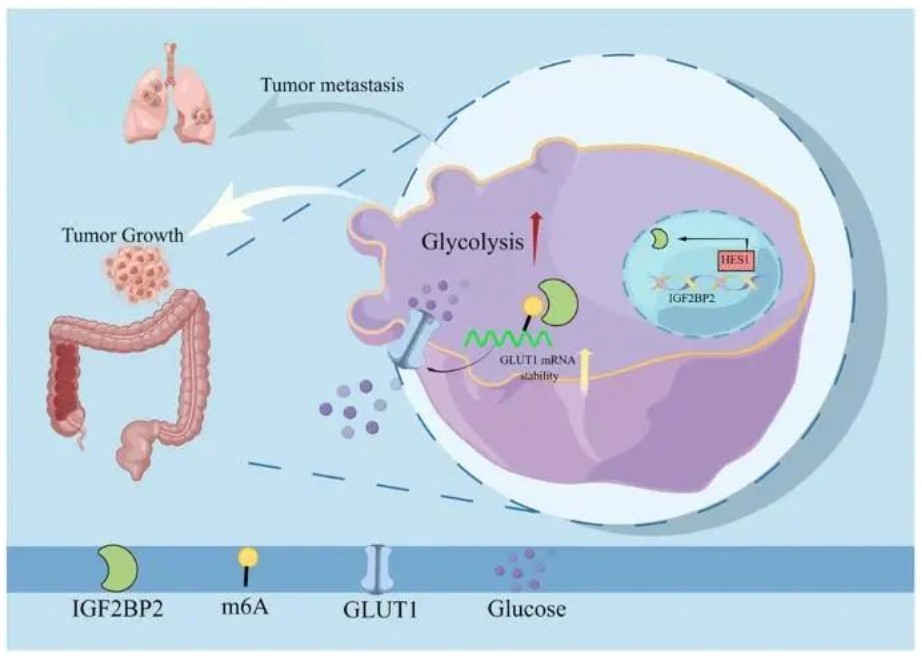
图形摘要
综上所述,HES1通过IGF2BP2依赖性方式增强m6A修饰的GLUT1 mRNA的稳定性,对CRC有氧糖酵解和进展具有显著的促进作用,可能成为治疗人类CRC的可行治疗靶点。(转化医学网360zhyx.com)
参考资料:
https://www.nature.com/articles/s41420-023-01707-4#Abs1
注:本文旨在介绍医学研究进展,不能作为治疗方案参考。如需获得健康指导,请至正规医院就诊。
 腾讯登录
腾讯登录









还没有人评论,赶快抢个沙发