【Adv. Sci.】山西大学合作湖南大学揭示通过新型纳米组装达到高肿瘤生长抑制的新机制
| 导读 | 导读:单原子纳米酶(SAzymes)具有高催化活性,具有打破肿瘤微环境(TME)中活性氧代谢平衡的潜力。TME中含有多种内源性还原性物质,如谷胱甘肽(GSH)。 |
9月11日,山西大学/湖南大学研究人员在国际权威期刊《Advanced Science》上发表了题为“Drug-Primed Self-Assembly of Platinum-Single-Atom Nanozyme to Regulate Cellular Redox Homeostasis Against Cancer”的研究论文,该研究中,研究人员构建了一种新型纳米组装物(CDs@Pt SAs/NCs@DOX),其Pt载量为34.8%,表现出突出的双重酶活性,模拟过氧化物酶(POD)和谷胱甘肽氧化酶(GSHOx)。其独特的GSHOx-like活性能够以相对较低的Km (1.04 mm)和较高的Vmax (7.46 × 10−6 m s−1)高效清除GSH,从而避免单一氧(1O2)的消耗。CDs@Pt SAs/NCs@DOX同时展示了低温光热疗法和TME或激光控制的拆卸和药物释放,可以有效调节细胞氧化还原稳态,实现高抑制肿瘤生长。这些结果为制备具有多种活性和可变大小纳米组装体的Pt szymes提供了有前景的策略,为szymes及其纳米组装体在生物医学领域的广泛应用提供了可能。

https://onlinelibrary.wiley.com/doi/full/10.1002/advs.202302703
研究背景
01
纳米酶是一种具有酶样活性的纳米材料,在制备成本、稳定性、酶活性和物理化学性质方面比大多数天然酶具有许多优点。研究人员首次报道的单原子催化剂(SAC),由于其明确的电子和几何结构,可以模拟天然酶的高度进化的催化中心,是一种很有前途的传统酶的替代品。受SACs的启发,单原子纳米酶(SAzymes或SAEs)引起了研究人员的广泛关注,并已成功地应用于癌症治疗、污染物催化降解、生物催化和抗菌试验等领域。在肿瘤治疗领域,SAzymes可以产生多种活性氧(ROS),如单氧(1O2)、超氧自由基(O2−)、羟基自由基(·OH.)、过氧化物(O22−)等。然而,谷胱甘肽(GSH),一种ROS清除剂,在肿瘤微环境(TME)中过度表达(高达10 mm),阻碍了ROS增强癌症治疗的效果。因此,有效控制和消耗TME中的谷胱甘肽对提高癌症治疗效率至关重要。谷胱甘肽氧化酶(GSHOx)在谷胱甘肽转化为谷胱甘肽二硫(GSSG)中起重要作用,有助于调节细胞氧化还原稳态; 然而,关于这一现象的报道很少。
在所有纳米材料中,碳点(CDs)具有丰富的悬空键(─OH、─C = O和─NH2)和高的表面体积比,这有利于铆接和暴露活性金属位点。此外,CDs具有良好的生物相容性和较低的细胞毒性,因此它们经常被用作构建SAzymes的载体,并在生物医学领域得到了应用。然而,CD的超小尺寸(<10 nm)使它们能够快速清除肾脏而不是肿瘤部位。因此,需要一种细致的策略来提高CDs作为Pt SAzymes载体的增强渗透性和滞留性(EPR)效果,以实现肿瘤递送。
研究过程及发现
02
考虑到DOX的自聚集行为,本研究首次将其作为牵引剂,驱动CDs@Pt SAs/NCs的自组装形成球形纳米组装体(CDs@Pt SAs/NCs@DOX),增强EPR效果并引入CT。另外,研究人员综合研究了CDs@Pt SAs/NCs的酶活性。由于CDs@Pt SAs/NCs在500 ~ 900 nm范围内具有较强的吸收光谱,研究人员进一步研究了CDs@Pt SAs/NCs作为光热转换器的可行性。研究人员采用经典的甲基噻唑四氮唑(MTT)对人正常肝细胞(LO2)、人宫颈癌细胞(HeLa)和小鼠乳腺癌细胞(4T1)进行体外细胞毒性实验。此外,研究人员进一步研究了HeLa细胞对不同浓度CDs@Pt SAs/NC和CDs@Pt SAs/NCs@DOX的摄取能力。随后,研究人员在健康小鼠中广泛评估了CDs@Pt SAs/NCs@DOX的生物相容性。结果发现,治疗后的小鼠血液学参数在标准范围内,而在治疗期间,老鼠的体重表现出合理的波动,显示出色的生物安全和生物相容性的CD@862/NCS@dox。
本文详细研究了CD@TP/NCS和CD@pt/NCS@DOX的药代动力学行为。还研究了4T1含肿瘤白蛋白/丙型小鼠CD的生物分布。本文进一步研究4T1多细胞球体的内化行为和组织渗透。体外实验结果表明,CD@TPS/NCS@DOX具有巨大的体内肿瘤治疗潜力。研究结果还证实了CDS@TPS/NCS@DOX在肿瘤的三联治疗中的巨大潜力。
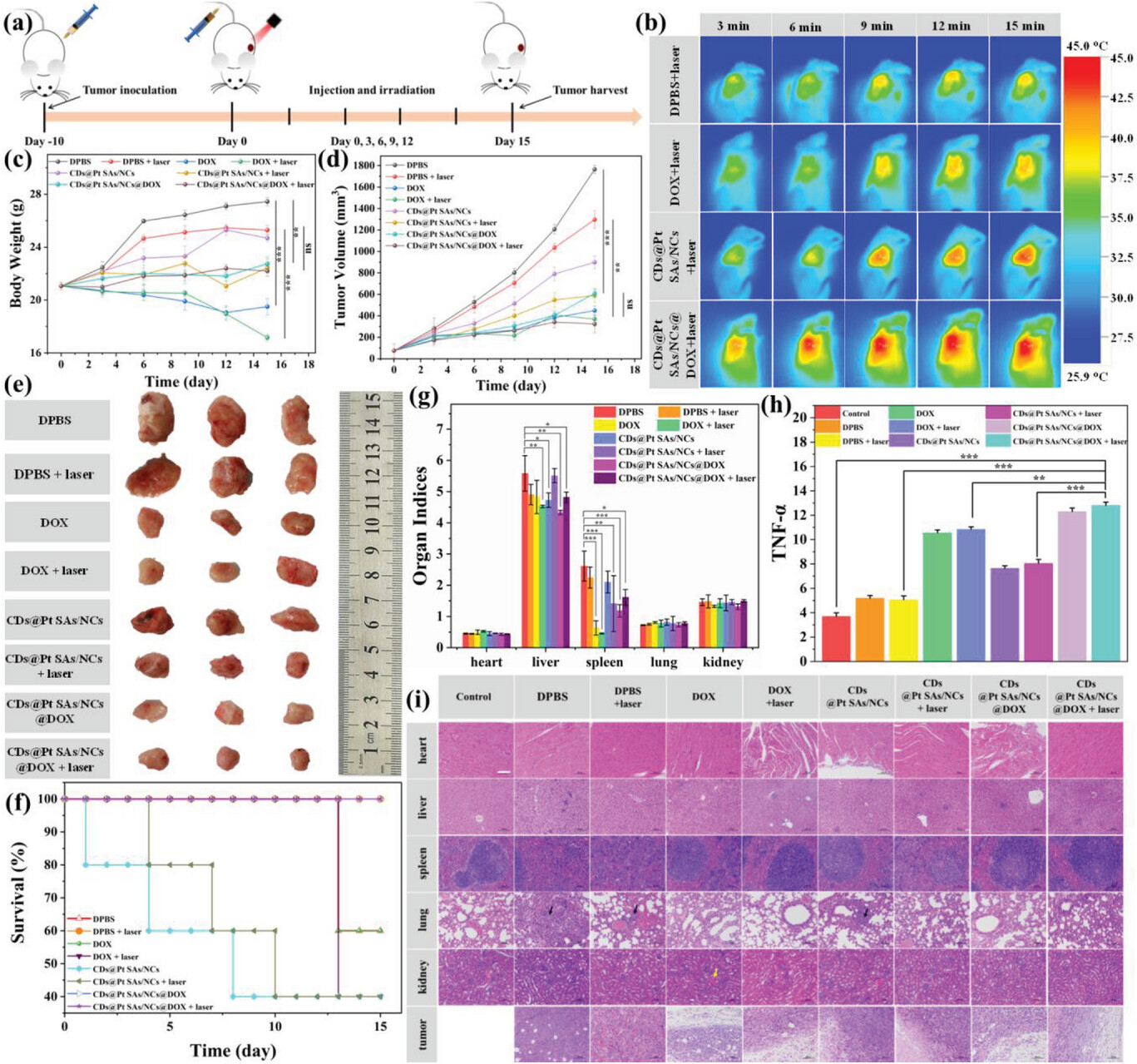
体内肿瘤抑制研究
研究结论
03
研究人员首次开发了一种以DOX为先导的基于CDS的Pt SAs/NCs超稳定纳米组件(CDs@Pt SAs/NCs@DOX),用于调节细胞氧化还原稳态,并结合纳米酶催化治疗、低温PTT和CT治疗恶性肿瘤。与其他已报道的用于肿瘤治疗的纳米系统相比,本纳米组件具有以下优势:1)CDs@Pt SAs/NCs@DOX可以通过TME中发生的生化反应产生1O2并消耗GSH,从而放大肿瘤中的氧化应激反应。2) dox驱动CDs@Pt SAs/NCs@DOX的形成提高了其在肿瘤中的富集效率,延长了其在血液中的清除时间。3) CDs@Pt SAs/NCs@DOX协同作用于肿瘤部位,保证了生物安全性,提高了肿瘤治疗效率。综上所述,研究人员利用CDs作为载体,利用DOX的驱动行为自组装Pt SAzymes,构建具有仿生酶活性的CDs@Pt SAs/NCs@DOX,拓展了CDs和SAzymes在生物纳米医学中的应用。(转化医学网360zhyx.com)
参考资料:
https://onlinelibrary.wiley.com/doi/full/10.1002/advs.202302703
注:本文旨在介绍医学研究进展,不能作为治疗方案参考。如需获得健康指导,请至正规医院就诊。
 腾讯登录
腾讯登录









还没有人评论,赶快抢个沙发