《Cell Reports》浙江大学研究团队发现推动肝脏肿瘤发生新机制
| 导读 | Mettl3是执行m6A机制的一个关键组成部分,已被发现在一些恶性肿瘤包括肝癌中过量表达。虽然发现Mettl3在肝细胞癌(HCC)进展中起到促肿瘤的作用,并与预后恶化相关,但鉴于肝脏微环境在HCC启动中的复杂作用,其在肝癌发生中的功能仍未确定。 |
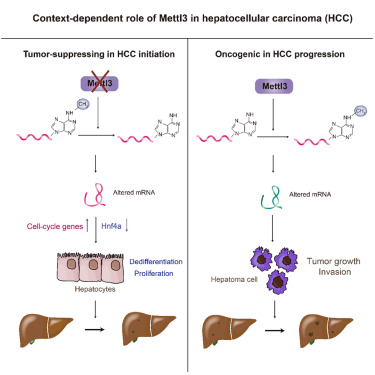
6月27日,来自浙江大学的梁廷波团队在《Cell Reports》上发表了名为“Loss of Mettl3 enhances liver tumorigenesis by inducing hepatocyte dedifferentiation and hyperproliferation”的研究文章,研究结果确定了Mettl3在肝脏肿瘤发生中的肿瘤抑制作用,表明其在HCC的启动和进展中可能具有相反的阶段性功能。

https://www.cell.com/cell-reports/fulltext/S2211-1247(23)00715-5
研究背景
肝细胞癌(HCC)占原发性肝脏恶性肿瘤的大多数,是第六大最常见的癌症。肝细胞随着潜在的持续炎症和纤维化而积累基因组和分子改变,最终引起全面的肿瘤性病变。
N6-甲基腺苷(m6A)是一种丰富的RNA内部修饰,通过影响RNA的命运在正常生理和疾病中发挥重要作用。通过调节前mRNA剪接、mRNA衰变、稳定性和致癌和抑癌转录物的翻译,m6A修饰影响肿瘤细胞的增殖、生存、迁移、侵袭、进展、转移和对抗癌疗法的敏感性。
m6A对癌症的影响要么是促肿瘤,要么是抗肿瘤,这取决于某种甲基化调节因子,对于不同的肿瘤类型和生物学背景也是不同的。Mettl3是执行m6A机制的一个关键组成部分,已被发现在一些恶性肿瘤包括肝癌中过量表达。虽然发现Mettl3在HCC进展中起到促肿瘤的作用,并与预后恶化相关,但鉴于肝脏微环境在HCC启动中的复杂作用,其在肝癌发生中的功能仍未确定。特别是,最近使用Mettl3基因敲除小鼠的研究结果显示,Mettl3的缺失与肝细胞平衡的改变、肝损伤、炎症和非酒精性脂肪肝有关。为此,我们产生了肝细胞特异性Mettl3缺失的小鼠,并试图研究Mettl3在多种临床相关HCC小鼠模型中的影响。
研究过程
Mettl3已被证明在HCC中发挥致癌功能。我们发现Mettl3的表达在人类HCC组织中过度表达,下调Mettl3对肝癌细胞有抗肿瘤作用,这与以往的研究一致。然而,通过使用不同的功能缺失的遗传策略,结果一致表明Mettl3在多种小鼠HCC模型中对肝脏肿瘤的发生有保护作用。这些结果清楚地表明,Mettl3在HCC发展的早期阶段具有抑制肿瘤的作用,而在已建立的HCC癌细胞中则具有促进肿瘤的作用。这一矛盾的发现得到了临床数据的进一步支持,即健康的肝脏组织比HCC副肿瘤组织的Mettl3表达水平更高。考虑到M6A机制的高度动态功能输出,Mettl3在肝癌中的贡献可能取决于阶段和环境。
在本研究中,使用肝细胞特异性Alb-Cre对Mettl3进行消融,破坏了肝细胞的平衡并诱发了肝损伤。这些发现与最近的几项研究一致。但Xu等人发现了一个更严重的表型,Mettl3(Flox/Flox); Alb-Cre小鼠在出生后7周内由于肝细胞逐渐死亡而死亡。我们和其他人的报告表明,Mettl3基因敲除的小鼠肝脏损伤不大,肝脏/体重比与年龄匹配的野生型对照组相当,而且年轻的小鼠没有出生后的死亡。肝脏的代谢特征和调节肝细胞分化的基因被明显下调。然而,不能排除独立于m6A甲基化的其他分子机制介导了Mettl3的功能影响。Li等人发现,Mettl3在肝脏中的耗竭通过增加其启动子区域的染色质可及性上调了人类白细胞分化抗原36(Cd36)和趋化因子配体2 (CCL2)的表达,从而推动了非酒精性脂肪性肝炎(NASH)的进展。值得注意的是,使用TBG-Cre敲除成年小鼠的Mettl3与明显的肝脏损伤无关,这与其他使用诱导性Alb-CreER模型的研究一致。
Mettl3的缺失加速了肿瘤的发生,这是多因素造成的。首先,高度增殖的肝细胞可能有助于增强肿瘤的发生。虽然过度增殖可能是对肝脏损伤的补偿,但Alb-Cre和TBG-Cre模型的MeRIP-seq分析显示,调节细胞周期的基因是Mettl3介导的m6A修饰的目标。在HCC模型中,脱分化也使肝细胞容易发生肿瘤性转化。特别是,肝细胞核因子4α(Hnf4α)被确定为Mettl3的一个关键下游因子,这与另一项研究相一致。最后,由Mettl3缺失引起的肝脏状况让人联想到非酒精性脂肪肝(NAFLD)。多条证据表明,Mettl3通过m6A修饰脂肪酸合成酶和过氧化物酶体增殖剂-激活剂α来调节脂肪酸代谢。Li等人通过在高脂肪饮食和蛋氨酸/胆碱缺乏饮食模型中使用条件性敲除小鼠,表明Mettl3是NASH发病机制的一个关键负调控因素。伴随着肝脏损伤和脂肪肝疾病的炎症、免疫细胞浸润和纤维化也可能与肿瘤的加速发生有非自主性的联系。Mettl3也可能在NASH以外的其他癌前病变中发挥作用。例如,Mettl3可与乙肝病毒蛋白相互作用,通过调节PTEN mRNA促进HCC的转化,表明对HBV相关的肿瘤发生有致癌功能。这些发现表明,鉴于不同的病因,Mettl3在肝癌发生中的作用更为复杂。
研究意义
研究发现Mettl3的缺失在推动肝癌发生中发挥了意想不到的强大作用,这与Mettl3在HCC进展中的致癌功能形成鲜明对比。Mettl3已被发现与许多肝脏疾病有关,包括肝脏发育、免疫学和病毒性肝炎,以及脂质代谢和非酒精性脂肪肝。考虑到HCC有不同的风险因素和发病机制,这些矛盾的结果可能与Mettl3的不同功能有关。因此,研究结果强调了在评估Mettl3对肝癌发生的影响时,实验条件、肿瘤模型和背景的重要性,在实施针对HCC的Mettl3的治疗策略时,可能出现相反的治疗结果。(转化医学网360zhyx.com)
参考资料:
https://www.cell.com/cell-reports/fulltext/S2211-1247(23)00715-5
注:本文旨在介绍医学研究进展,不能作为治疗方案参考。如需获得健康指导,请至正规医院就诊。
 腾讯登录
腾讯登录









还没有人评论,赶快抢个沙发