肿瘤界“扛把子”!中山大学黎孟枫团队研究发现液体活检在癌症转移中的调控新机制
| 导读 | TGF-β信号传导的异常激活在癌症转移和进展中起着关键作用。然而,TGF-β途径失调的分子机制仍有待了解。 |
4月18日,中山大学黎孟枫团队在《Cell Discovery》(IF=38)在线发表题为“PHF14 enhances DNA methylation of SMAD7 gene to promote TGF-β-driven lung adenocarcinoma metastasis”的研究论文,该研究表明趋化因子CCL17是治疗心血管衰老的新靶点。该研究发现SMAD7,一个直接下游的转录靶点,也是TGF-β信号的关键拮抗剂,在肺腺癌(LAD)中由于DNA高甲基化而被转录抑制。进一步发现PHF14结合DNMT3B并作为DNA CpG基序读取器,将DNMT3B募集到SMAD7基因位点,导致DNA甲基化和SMAD7转录抑制。

https://www.nature.com/articles/s41421-023-00528-0
研究背景
肺腺癌(LAD)是非小细胞肺癌(NSCLC)的主要组织学亚型,是全球最常见的恶性癌症类型之一。由于在 LAD 发展的早期阶段症状通常难以察觉,超过 50% 的 LAD 患者在初始诊断时发现肺内或远处转移,导致 LAD 患者的总体 20 年生存率约为 5%,转移性 LAD 患者的 5 年生存率低于 5%。因此,确定调节LAD转移的机制,旨在为转移性LAD提供潜在的诊断和预后生物标志物以及治疗靶点,是改善疾病临床结果的关键。
先前的研究表明,TGF-β信号传导有力地驱动SMAD特异性转录程序,并且TGF-β信号在癌细胞中的生物学不同作用的协调可能部分依赖于与SMAD相互作用的分子,从而调节SMAD的功能,从而改变TGF-β靶基因的表达谱。然而,各种SMAD的功能如何通过其相互作用分子改变,从而重定向TGF-β信号传导的生物学效应,仍然不完全清楚。
研究进展
为了深入了解 DNMT3B 介导的 LAD 中 SMAD7 位点异常 DNA 甲基化的机制,我们进一步研究了以前未鉴定的因子是否可能调节 DNMT3B 介导的 SMAD7 DNA 甲基化和 LAD 中的转录抑制。采用免疫沉淀-质谱(IP-MS)测定法筛选A3细胞中DNMT549B的未知结合伴侣。在DNMT3B排名靠前的推定结合蛋白中,一种植物同源域(PHD)指蛋白PHF14被鉴定为表观遗传抑制因子,与DNMT3B相互作用,并且使用LAD细胞和293FT细胞通过内源性和外源性共IP进一步验证了相互作用。值得注意的是,TGF-β处理适度增强了DNMT3B和PHF14之间的相互作用。
此外,LAD细胞中过表达PHF14通过促进SMAD7 DNA甲基化增强了TGF-β诱导的SMAD结合元件(SBE)荧光素酶活性和抑制SMAD7表达,而在未TGF-β处理的细胞中,SMAD7 DNA甲基化水平中等增强,SMAD7 mRNA水平和TGF-β信号活性不受异位过表达PHF14的显著影响。相反,敲除LAD细胞中的PHF14通过耗尽的SMAD7 DNA甲基化提高SMAD7表达水平来损害TGF-β诱导的SBE-荧光素酶活性。这些结果表明,PHF14是DNMT3B新发现的结合伴侣,可能通过促进LAD中DNMT3B介导的SMAD7 DNA高甲基化和转录抑制来促进TGF-β信号激活。
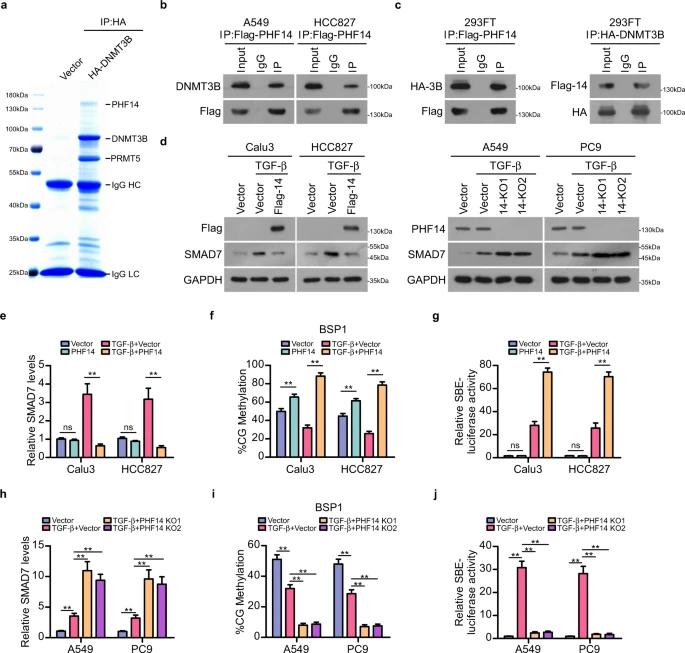
PHF14被确定为DNMT3B的新型结合伴侣
研究意义
综上所述,本研究结果为TGF-β信号异常激活及其对LAD转移的诱导提供了思路,揭示了参与SMAD14表观遗传抑制的新型PHF3/DNMT7B复合物,表明PHF14在决定TGF-β的生物学效应中起着关键作用。这些结果也表明PHF14和SMAD7在LAD的诊断和预后评估中具有显着意义。
此外,值得注意的是,我们目前的研究还揭示了使用液体活检的可行性,液体活检是一种有前途的临床肿瘤学无创诊断方法,开发实用的SMAD7 ctDNA甲基化测试,作为LAD进展和预后的临床有用标志物。
此外,值得未来努力进一步评估抑制DNA甲基化和消除PHF14,DNMT3B和DNA之间的相互作用是否可以成为靶向TGF β驱动的LAD进展和转移的潜在策略。(转化医学网360zhyx.com)
参考资料:
https://www.nature.com/articles/s41421-023-00528-0
注:本文旨在介绍医学研究进展,不能作为治疗方案参考。如需获得健康指导,请至正规医院就诊。
 腾讯登录
腾讯登录









还没有人评论,赶快抢个沙发