【研究】细胞器提取技术再上一个新的台阶!
| 导读 | 提取完好的溶酶体将有助于研究和治疗溶酶体缺陷症。 |
我们细胞的正常运转离不开细胞器与许多复杂程序的精确配合。动物细胞中有一个必不可少的细胞器——溶酶体,它的作用是分解和重复利用蛋白质,脂类与核苷酸这些大分子。除了细胞消化和废料处理,溶酶体还参与氨基酸的信号传递以促进蛋白质合成及其他工序。
考虑到大部分疾病都是由于溶酶体功能缺陷造成的,科学家花费数十年的时间专注研究这个细胞器也就不足为奇。但是只有为数不多的技术可以用来提取细胞中的溶酶体。最常见的方法称为“密度梯度离心法”,它可以慢慢破坏细胞膜,并为细胞里的物质提供离心力,再通过密度的不同来分离细胞组分。可惜的是,有些细胞器与溶酶体的密度相同,所以得到的样品纯度不高。此外,此工序耗时太久,许多溶酶体蛋白早已流失或降解。
“免疫沉淀法”是一种更为先进的技术,它可以修复溶酶体的膜蛋白,让包覆着特定抗体的磁珠可以抓取到它们。虽然这种方法可以得到纯度高的样本,但提取出的溶酶体中,蛋白质组分有所改变,所以后续的蛋白分析也相应的不够准确。因此,我们必须寻找新的方法来提取细胞中的溶酶体。
幸运的是,北陆先端科学技术大学院大学(JAIST)的Shinya Maenosono教授带领的研究团队接受了这一挑战,并且研发出了一项新颖的技术来快速提取高纯度完好的溶酶体。该研究发表于《ACS Nano》期刊上,题为“Quick and Mild Isolation of Intact Lysosomes Using Magnetic–Plasmonic Hybrid Nanoparticles”。(研究人员还包括来自JAIST的松村和明教授、平冢佑一教授,和日本东北大学的田口智彦教授)
https://pubs.acs.org/doi/10.1021/acsnano.1c08474
这种技术是运用银和铁钴合金制成的磁化等离子体混合纳米粒子(MPNPs),它的表面覆盖着名为氨基葡聚糖(aDxt)的化合物。细胞通过“内吞作用”自动吸收“aDxt包覆的MPNPs,它会在溶酶体中达到峰值。一旦溶酶体中积蓄了足够多的MPNPs,细胞就会慢慢被“瓦解”,然后用电磁体取出溶酶体。
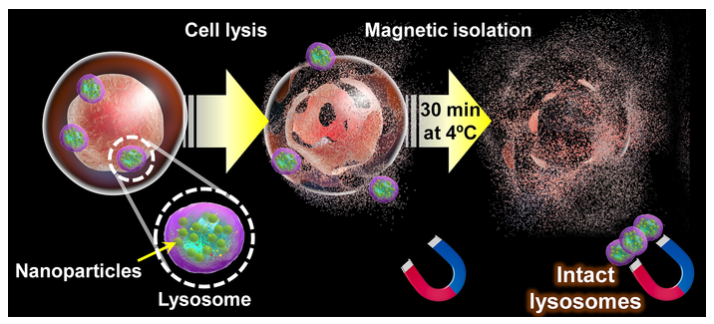
(一旦细胞中的溶酶体通过内吞作用途径积蓄电磁纳米粒子,细胞膜就会破裂。在30分钟之内用电磁体“筛选”里面的物质。这一工序结束之后,就可以用电磁体吸取完好的溶酶体,以研究其结构,代谢及蛋白组分。)
https://www.eurekalert.org/multimedia/813478
该技术能否成功最关键的部分在于让MPNPs只能进入溶酶体。这时等离子成像就能派上用场了。在光线的作用下,光学显微镜可以很容易显现等离子纳米粒子。通过免疫染色对内吞途径中不同类型的细胞器进行不同的染色,并检查MPNPs与它们的重叠情况,研究人员明确了最多MPNPs可以抵达溶酶体的确切时间,同时,也可以确保分离程序中产生的溶酶体是纯度较高的。
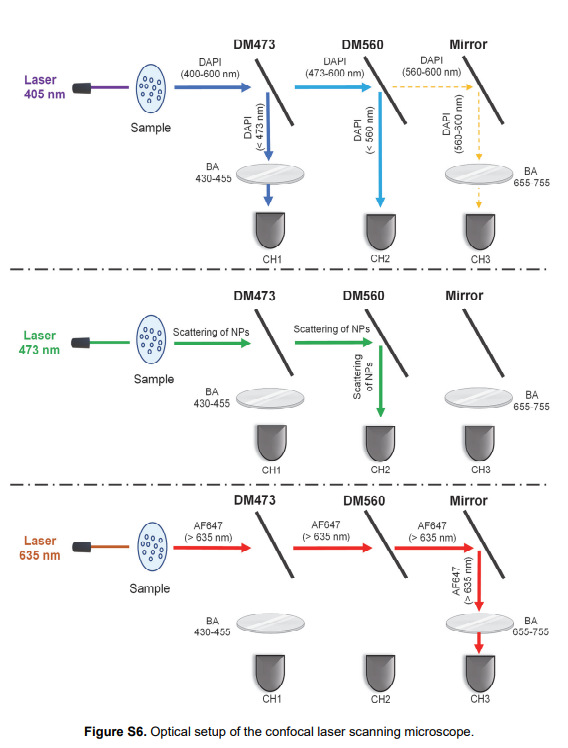
随后,该团队分析了溶酶体蛋白组分中温度对其的影响和电磁分离时间。研究结果表明,甚至是在温度低至4°C的情况下,蛋白质流失也是非常迅速的。所幸,他们的方法可以足够快速的提取完好的溶酶体,正如Maenosono教授强调的那样:“我们已经发现,细胞破碎之后最快提取溶酶体的时间为30分钟,离心分离技术最少需要几个小时,这已经是很大幅度的提升了。”
总体来说,这项新技术将帮助研究人员探索溶酶体那些不稳定的代谢产物以及它们在受到刺激时的变化情况。也就是说,这为我们探究溶酶体功能紊乱的病症提供了新的方向。就这一方面而言,Maenosono教授认为:“鉴于溶酶体与许多细胞代谢物有着紧密的联系,更好的了解溶酶体功能以明确其在不同细胞状态下的调节方式是极为必要的。因此,我们的技术未来将有助于更好的研究和治疗溶酶体缺陷症。”此外,通过改进这项新技术也可以用于提取除了溶酶体以外的其他细胞器。这项研究有希望让我们对细胞内的物质有一个更高水平的了解。(转化医学网360zhyx.com)
参考链接:https://www.eurekalert.org/news-releases/939401
 腾讯登录
腾讯登录









还没有人评论,赶快抢个沙发