【Cell子刊】为什么减肥总败给肚腩?腹部脂肪才是脂肪中的“战斗机”
| 导读 | 减肥就是一场没有终点的旅程:意志力与脂肪时刻都在PK,此消彼长。为了对抗肥胖引起的代谢紊乱,许多饮食干预法也脱颖而出,其中最流行的当属间歇性禁食。 |

众所周知,肥胖是2型糖尿病、心脏病和癌症等许多重大疾病的主要风险因素。对于大多数人来说,减肥就是一场没有终点的旅程:意志力与脂肪时刻都在PK,此消彼长。为了对抗肥胖引起的代谢紊乱,许多饮食干预法也脱颖而出,其中最流行的当属间歇性禁食。近几年来,间歇性禁食成了瘦身界的新宠,这种方法不仅可以减肥、增强精力,甚至还可以延寿。
然而,对于一些人来说,再好的效果,最终也会被大肚腩打败。这是为什么?
北京时间3月3日,发表在《Cell Reports》上的一项最新研究中,来自悉尼大学的研究团队发现了其中的“端倪”,他们利用了蛋白质组学技术发现,腹部脂肪(内脏脂肪)会在体内积聚成一个“大肚腩”,随着时间的推移,这些脂肪可以自行改变储存模式,并适应空腹状态,从而对减肥产生更强的抵抗力。原来,腹部脂肪才是脂肪中的“战斗机”。

此前已有研究表明,在人类和啮齿类动物中,即使在体重没有减轻的情况下,间歇性禁食也被证明能降低空腹胰岛素水平,改善葡萄糖耐量,并降低血胆固醇。
间歇性禁食法主要分为两种,即限时进食和隔日禁食(每隔一日不进食)。隔日禁食是一种更简单且容易实施的策略,已在人体试验中被确定更具耐受性。
在这项新研究中,研究人员使用先前建立的隔日禁食小鼠模型,检查它们体内不同地方的脂肪组织类型以了解其功能。
脂肪组织在调节急性禁食反应中发挥着核心作用。在禁食期间,血糖水平降低,循环中胰岛素水平降低,胰高血糖素升高并通过肝脏作用维持血糖水平。随着一系列刺激后,包括瘦素在内的其他激素的释放会导致交感神经系统释放儿茶酚胺、去甲肾上腺素,或肾上腺素。这些分子通过肾上腺素能受体信号诱导脂肪分解,并触发白色脂肪组织释放非酯化脂肪酸(游离脂肪酸),以在禁食期间为其他组织提供能量。
研究人员发现,除了上述复杂的作用外,不同的脂肪类型在禁食期间的变化存在很大差异,其中包括内脏脂肪(腹部脂肪)和皮下脂肪。此前的研究表明,在人类和啮齿类动物中,大量的内脏脂肪与胰岛素抵抗、心血管疾病和癌症等高发病率呈正相关。相比之下,作为最大脂肪库的皮下脂肪,它的增加与代谢疾病风险降低有关。
研究通讯作者、悉尼大学生命与环境科学学院Mark Larance博士:“虽然大多数人认为所有的脂肪组织都是一样的,但事实上,位置不同,脂肪组织也有很大的不同。我们的数据显示,在间歇性禁食期间,内脏和皮下脂肪都会发生剧烈变化。”
为什么内脏脂肪会抵抗减肥?
在禁食期间,脂肪组织通过释放游离脂肪酸向身体其他部位提供能量。与对照组小鼠相比较,隔日禁食的小鼠总食物摄入量出现轻微但不显著的减少,体重没有变化。如果隔日禁食持续时间延长,结果显示总食物摄入量的小幅减少,并导致总体重下降,这与其他研究的结果一致。然而,研究人员发现,隔日禁食将小鼠内脏脂肪和皮下脂肪的线粒体蛋白含量提高到相似的程度,却仅诱导了皮下脂肪中的解偶联蛋白1(UCP1)的表达。出乎意料的是,研究人员观察到,隔日禁食大大降低了内脏脂肪存储的脂解途径,相反,却增加了内脏脂肪和皮下脂肪中的脂肪酸合成途径。这些数据表明,在多次禁食期间,内脏脂肪可以显著且独特地改变脂质储存。
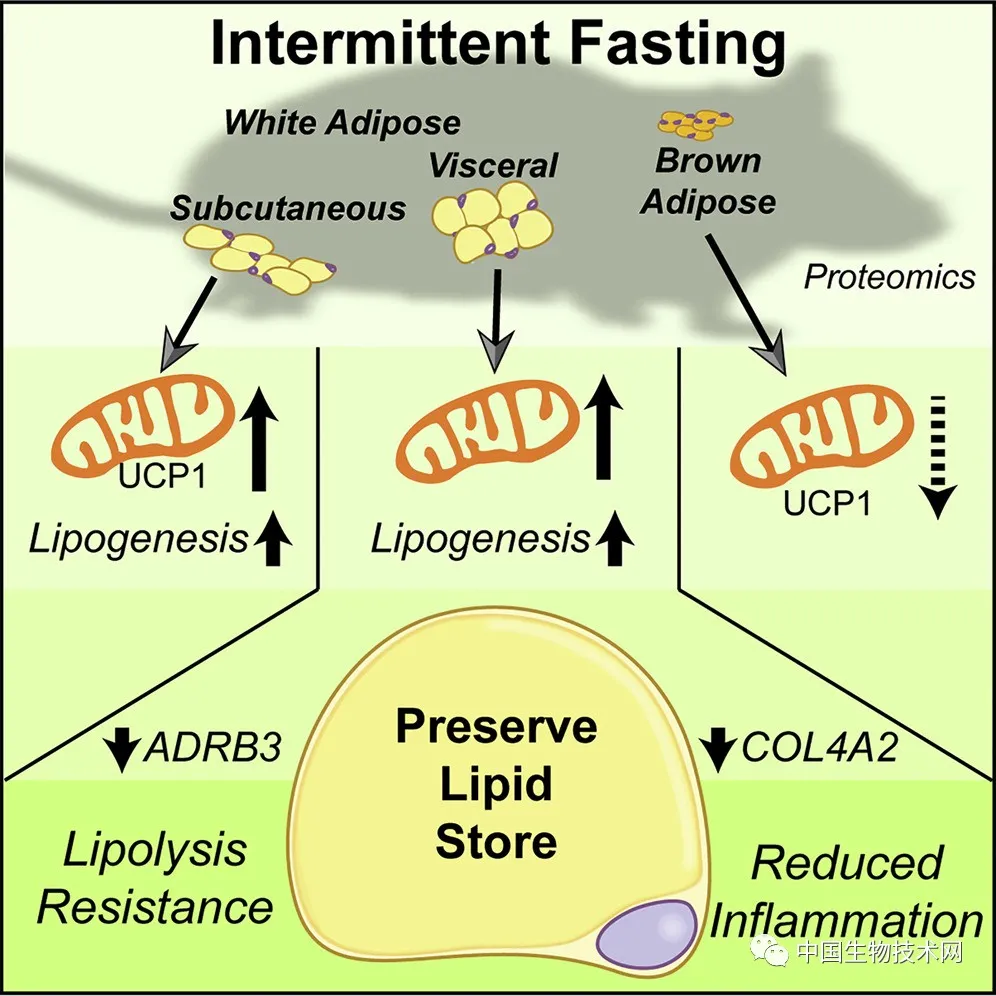
简而言之,在禁食期间,内脏脂肪对脂肪酸的释放产生了抵抗力,并连同皮下脂肪增加了它们的脂肪储存能力,以便在下一个禁食期之前迅速重建脂肪储存。
研究人员认为,很有可能是反复禁食的经历触发了内脏脂肪存储的信号途径。
Larance说:“这表明内脏脂肪能适应反复禁食的空腹状态,并保护其能量储存。这种适应可能是内脏脂肪在长时间节食后抵抗体重减轻的原因。”
研究人员表示,未来对小鼠和人类的研究可能会揭示这种抗性发生的机制,以及哪种饮食类型和其他干预措施可以最有效地解决腹部脂肪的问题。
研究人员利用蛋白质组学技术,检测了8500多种位于脂肪沉积物中的蛋白质,并建立了小鼠脂肪组织间歇性禁食期间蛋白质组学分析的可视化网站。
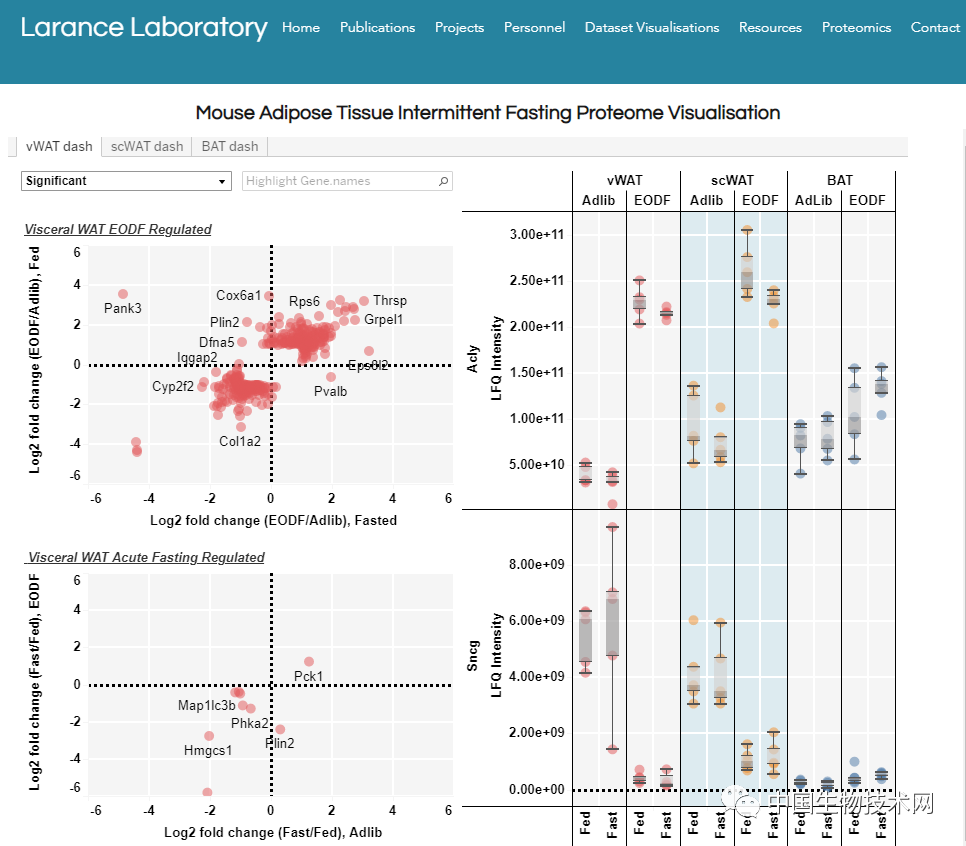
蛋白质组学是一个相对较新的研究领域。该研究结果提供了丰富的数据来源,有助于更全面描绘脂肪组织的内部运作机制。通过蛋白质组学,研究团队对间歇性禁食引起的主要细胞变化有了了解,并在进一步分析后强调了内脏脂肪的有效储存机制。
该结果为未来的研究奠定了基础,剖析导致内脏脂肪在禁食期间抵抗能量释放的分子,并帮助确定哪种饮食策略能最有利于代谢健康将是该团队下一步的工作。
论文链接:
https://doi.org/10.1016/j.celrep.2021.108804
 腾讯登录
腾讯登录









还没有人评论,赶快抢个沙发