还记得18年诞生的两名基因编辑婴儿吗?

此前,霍金曾预言:“过不了多久,富人将能够编辑子女的DNA,提高其记忆力和疾病免疫力......,没得到改造的人类可能无法竞争,逐渐绝迹,或者变得不重要,人类会展开自我设计的竞争。”
而后,中国科学家贺建奎宣布将基因编辑技术用于人类受精卵并植入母亲子宫,一对名为露露和娜娜的基因编辑婴儿在中国健康诞生。而这对双胞胎,因利用CRISPER技术修改过体内一个基因CCR5,出生后即能天然抵抗艾滋病。
且不论道德方面,这样的技术确实可以为人类的遗传性疾病打开一扇窗。那么,这类难治性疾病是否可以抛除CRISPER技术,采用新的基因编辑工具进行治疗呢?
作为全球基因编辑领域的顶尖学者,麻省理工学院和哈佛大学布罗德研究所的化学生物学家刘如谦(David R. Liu)表示,目前至少有6000-10000种已知的遗传疾病与基因突变相关,为了真正解决致病原因,需要开发出纠正或改善基因突变的方法。基因编辑剪刀,CRISPER可以通过剪切DNA破坏致病基因。但很多情况下,研究人员并不想破坏致病基因,因此刘如谦开发了“单碱基编辑法”。尽管如此,但该技术仍有很大的发展空间。于是,“先导编辑”出世,相当于一种“分子文字处理器”,能够在DNA分子中寻找一条链,并直接用另一条链来取代它。
继前两大基因编辑技术突破后,刘如谦团队在Nature上发表题为“A bacterial cytidine deaminase toxin enables CRISPR-free mitochondrial base editing”的研究论文。研究团队发现,一种细菌毒素,DddA,可以将胞嘧啶(C)转化为尿嘧啶(U)。DddA可直接作用于双链DNA,无需依靠Cas9酶来进行破坏,这是以前从未见过的。该研究使用首个不依赖CRISPER碱基编辑器——DdCBE,实现了对线粒体基因组的精准编辑,这是前所未有的研究和治疗线粒体遗传病的工具。

18年,刘如谦收到了一封电子邮件,来自华盛顿大学微生物学家Joseph Mougous,他的团队发现了一种奇怪的酶。而刘在碱基编辑中也利用了类似的酶,只是它们只作用于单链DNA。在过去,刘必须依靠Cas9酶来破坏DNA并创建一个未缠绕的单链DNA区域,以使其酶起作用。由于它依赖于指导Cas9的RNA链,因此该技术无法到达线粒体基因组。而Mougous发现的新酶DddA,可以直接到达线粒体基因组。
研究人员首先分析?了预测的细菌脱氨酶,其中包含的序列暗示它们是细胞间蛋白质的递送系统,如VI型分泌系统(T6SS)的底物。他们发现,DddA?可能作用于先前未描述的脱氨酶底物。
在进一步的实验中,他们发现在?大肠杆菌中表达?亚致死水平的?DddA??大大增加了突变频率。?他们对经历了连续接触DddA和克隆瓶颈的5个大肠杆菌?谱系进行全基因组测序,在存在DddA的情况下对物种对照菌株进行了相似的治疗。他们观察到,接触有活性的DddA的菌株的SNP?总量??,大约是产生无活性酶的菌株的50倍。
但是,研究人员观察到,??完整的DddA??与可编程DNA结合蛋白融合的表达?,对人HEK293T细胞是有毒的。为了避免这种毒性,他们将蛋白质分成两半,旨在邻近的目标DNA上组装时才重建脱氨活性。他们的实验也共同证明了分裂的DddA可融合成转录激活子样效应子(TALE)阵列,介导人类核DNA中C-G到T-A的转化。
于是,第一个在mtDNA中进行精确基因组编辑的工具——DdCBE横空出世。为了探究mtDNA编辑的普遍性,他们设计并改造了7对TALE阵列,以靶向5个线粒体基因:MT-ND1,??MT-ND2,MT-ND4,MT-ND5,和MT-ATP8。
治疗后3-6天后,?研究人员观察到,?HEK293T细胞中DdCBE线粒体碱基编辑效率在4.6%-49%间变化,具体取决于间隔区域中的拆分类型、拆分方向和目标胞嘧啶位置。他们没有在间隔区域外检测到插入缺失或碱基编辑。
研究人员还证实了?HEK293T细胞中mtDNA?编辑的持久性?超过18??天,并指出??mtDNA??编辑不会降低细胞活力,不会产生大的??mtDNA??缺失,也不会干扰??mtDNA的?拷贝数。
为了分析DdCBE??在人线粒体基因组中的脱靶活性?,他们用组成性表达优化的DdCBE?或相应的死DdCBE?对照的质粒转染HEK293T细胞,?以区分?DdCBE?诱导的单核苷酸突变体?与背景异质性。?研究人员发现,每个DdCBE对线粒体全基因组范围的脱靶?C-G到T-A编辑的平均频率与未处理和无DdCBE的对照组相似,除了靶向MT-ND5的DdCBE,其平均脱靶编辑频率高出1.6倍。具有标准N端结构域的DdCBEs??通常表现出比脱靶编辑高150?860倍的脱靶编辑,而脱靶编辑效率和脱靶活性之间没有很强的相关性。
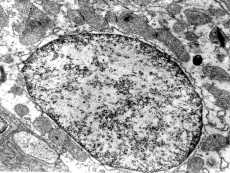
线粒体包围的鱼鳃上氯细胞细胞核的电镜图像
南加州大学医学遗传学家Joseph Hacia表示,新的DNA编辑器颇具创新性和开拓性。它很可能会在小鼠中起作用,他希望它能对治疗产生深远的影响。
哥伦比亚大学研究线粒体疾病研究专家,平野道雄(Michio Hirano),并未参与这项工作,他说这是一个“非常聪明”的策略,是“解决线粒体领域的圣杯”。
除了试图创建人类线粒体疾病的细胞和小鼠模型外,研究人员还将寻找其他可以修饰双链DNA的细菌脱氨酶。他们还希望提高编辑效率并减少脱靶编辑,以便最终可以在人类中测试mtDNA基础编辑。刘表示,要走到那条路很长。他希望,有了他们的蓝图,该领域的精力和资源将采用这些工具,并继续对其进行改进。
参考:
【1】Mok, B.Y., de Moraes, M.H., Zeng, J.?et al.?A bacterial cytidine deaminase toxin enables CRISPR-free mitochondrial base editing.?Nature?(2020).
【2】https://health.qq.com/a/20181221/007071.ht
【3】
【4】https://mp.weixin.qq.com/s/_5FaBK_n-RviuSsdiul6AQ
【5】
【6】https://www.genomeweb.com/gene-silencinggene-editing/bacterial-toxin-leads-crispr-free-mitochondrial-dna-base-editing#.XwgQC6EzbIW



 腾讯登录
腾讯登录









还没有人评论,赶快抢个沙发