首个PD-L1单抗在中国获批!III期肺癌治疗迎来重磅利器
| 导读 | 12月9日,国家药品监督管理局官网显示阿斯利康PD-L1单抗Imfinzi(durvalumab,度伐利尤单抗注射液,中文商品名:英飞凡,简称I药)的上市申请(JXSS1800040/41)获得批准 |
首个PD-L1单抗在中国获批!III期肺癌治疗迎来重磅利器12月9日,国家药品监督管理局官网显示阿斯利康PD-L1单抗Imfinzi(durvalumab,度伐利尤单抗注射液,中文商品名:英飞凡,简称I药)的上市申请(JXSS1800040/41)获得批准在灵魂砍价4.36之后,阿斯利康迎来新一轮刷屏。12月9日,国家药品监督管理局官网显示阿斯利康PD-L1单抗Imfinzi(durvalumab, 度伐利尤单抗注射液,中文商品名:英飞凡,简称I药)的上市申请(JXSS1800040/41)获得批准。这是继奥希替尼获批NSCLC一线、奥拉帕利获批卵巢癌一线之后,阿斯利康今年在中国收获的又一项重磅新药上市批准,进一步壮大了阿斯利康的中国肿瘤业务。
Imfinzi用于治疗同步放化疗后未进展的不可切除III期非小细胞肺癌,是国内第6家上市的免疫检查点制剂,不过前面5家都是PD-1单抗,I药是第1个在中国上市的PD-L1单抗。PD-L1单抗和PD-L1单抗有什么区别吗?
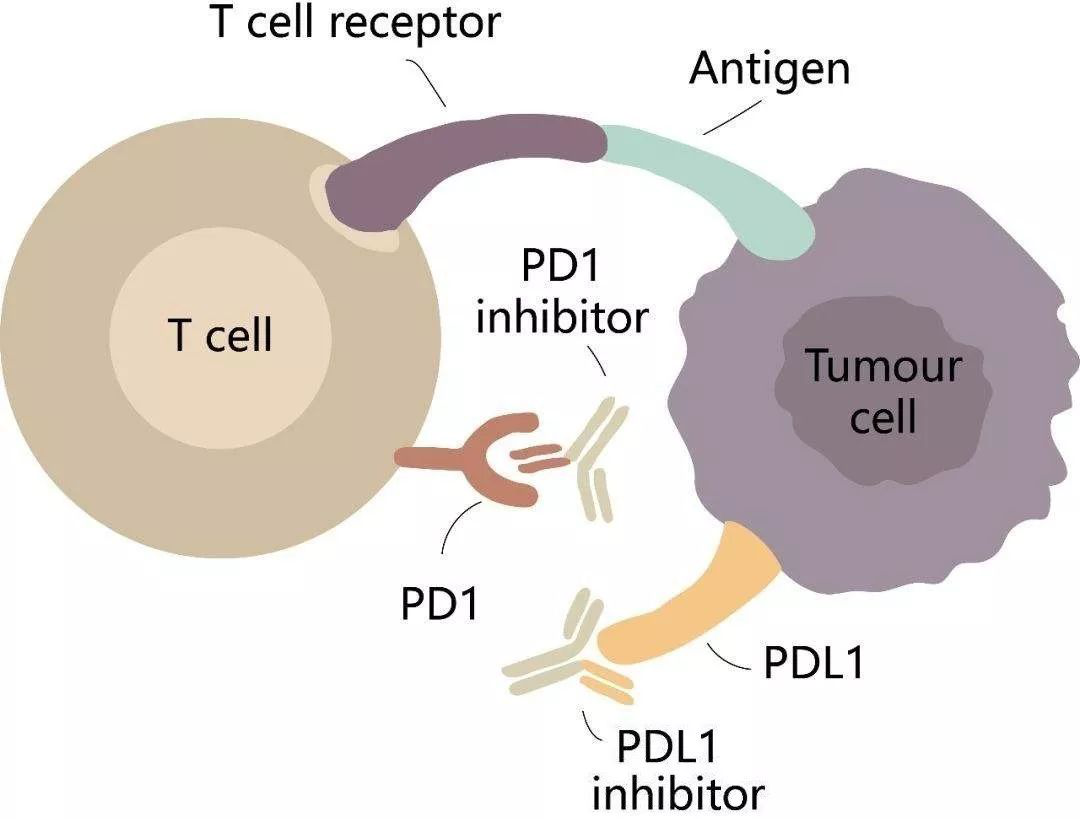
如上图所示,PD-L1和PD-1是配体和受体的关系,二者识别结合后会给肿瘤细胞提供一条逃脱免疫系统杀伤的“生路”。具体来说,肿瘤细胞表面可以表达PD-L1,T细胞表面则表达PD-1,当PD-L1与PD-1结合后,则让T细胞活性受到抑制而失去原有的杀伤作用,肿瘤便得以生长。因此,阻断PD-L1/PD-1的结合,便可恢复T细胞对肿瘤细胞的杀伤力。无论是PD-1抗体,还是PD-L1抗体,都是在这一思路下开发的。?那么,PD-L1抗体和PD-1抗体的抗肿瘤疗效是否有差异呢?理论上讲,抗PD-1单抗阻断PD-1与PD-L1结合同时阻断PD-1与PD-L2的交互作用,可潜在增加自身免疫性的风险;抗PD-L1单抗保留PD-L2与PD-1交互作用,潜在降低对免疫稳态的影响。?从临床试验数据看,在一些瘤种中PD-1和PD-L1抗体两者的疗效差不多。一致认为,PD-1目前约30%的有效率,因此也就为PD-L1抗体留下了市场空间。正因为如此,对每一种癌症,甚至每一个患者,PD-1或PD-L1抗体也将不是一种绝对选择,可能根据瘤种、疾病进展状态、患者情况、药物耐受、响应率等多方面因素共同考虑,选择用药,甚至有时PD-1和PD-L1抗体也是一种相辅相成的关系。回到今天新闻的主角,我们再进一步介绍一下I药。
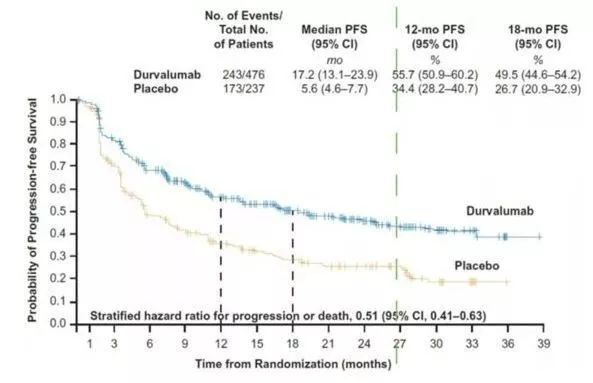
III期肺癌:Imfinzi的应许之地Imfinzi此次获批的III期非小细胞肺癌其实是肺癌领域非常细分的一个市场。但是恰恰正是因为一开始就锚定了这个细分市场,I药才得以在激烈的市场竞争中占据了自己的一席之地。?从病情严重程度上,肺癌可以分为I期、II期、III期、IV期。I期和II期肺癌都处于病情的早期阶段癌细胞没有扩散,手术切除肺部肿瘤块+化放疗等就是非常有效的治疗方案,临床上以治愈为目标。I期肺癌的5年生存率可以达到70%-90%,II期肺癌的5年生存率可以达到50%-70%。而到了IV期肺癌阶段,癌细胞出现向胸腔之外的远端扩散,比如转移至远端淋巴结、肝脏、骨骼或脑,已经无法手术,临床上治愈可能性较低,通常以延长生存期改善生活质量为目标。IV期肺癌的5年生存率只有5%左右。?III期肺癌,癌细胞虽然出现扩散但仍局限在胸腔内,会扩散转移至胸腔其他部位的淋巴结或胸腔内的其他主要器官,因此III期肺癌也被称为局部晚期肺癌。虽然III期肺癌很难通过手术清除所有癌细胞,但是相比IV期肺癌仍有较大希望治愈。过去很长时间内,III期肺癌的标准治疗是同步放化疗,但效果不如人意。基于1999-2010年的美国NSCLC生存数据,IIIA~IIIC期患者的5年生存率分别约为36%,26%和13%。?Imfinzi用于III期肺癌在临床数据上显示出了巨大的优势。在代号为PACIFIC的III期多中心随机、双盲、安慰剂对照的试验中,III期肺癌患者采用同步放化疗之后,给予一年的Imfinzi巩固治疗,可以将标准治疗的中位PFS从5.6个月显著延长至17.2个月,将18个月无进展生存率从26.7%提高到49.5%,把III期患者发生远端转移的时间从16.2个月延长到到28.3个月,将疾病进展推迟将近1年的时间,同时,死亡风险也降低了32%!?
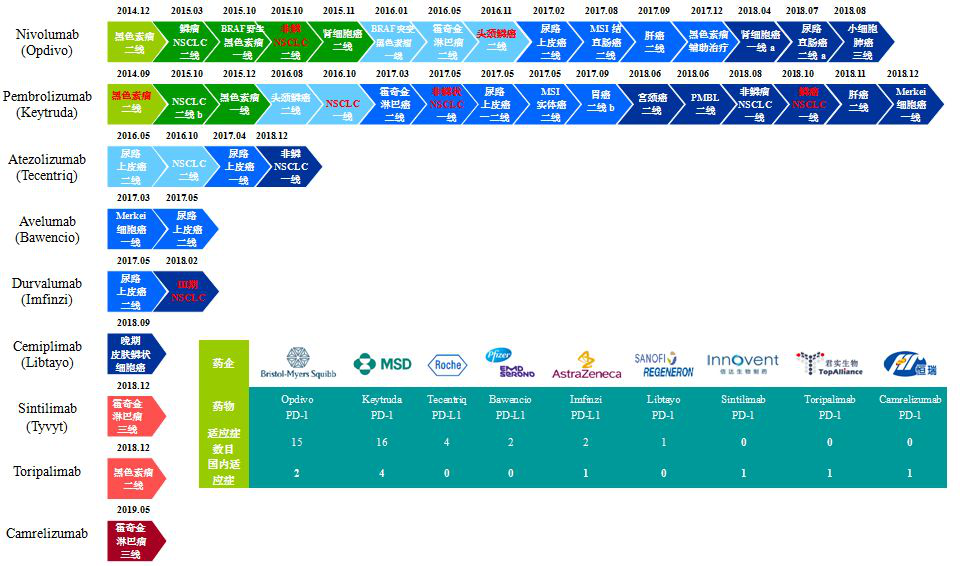
全球后发,中国先至:I药成PD-1/PD-L1赛道黑马从全球市场的出场顺序上看,Imfinzi在PD-1/PD-L1市场并没有占据先发优势,不仅比PD-1抗体O药、K药的上市时间晚了近3年,比同类PD-L1抗体T药的上市时间也晚了一年,但是在中国市场上,I药并没有比O药、K药落后太多,上市时间还跑到了T药的前面。?在市场业绩上,Imfinzi在2019年前三个季度的销售收入合计已达10.45亿美元,较2018年同期的3.71亿美元增长了180%,而季度收入走势上又有逼近Tecentriq的趋势,可见其虽是后发,但市场表现并不逊色,堪称是PD-1/PD-L1赛道黑马。?
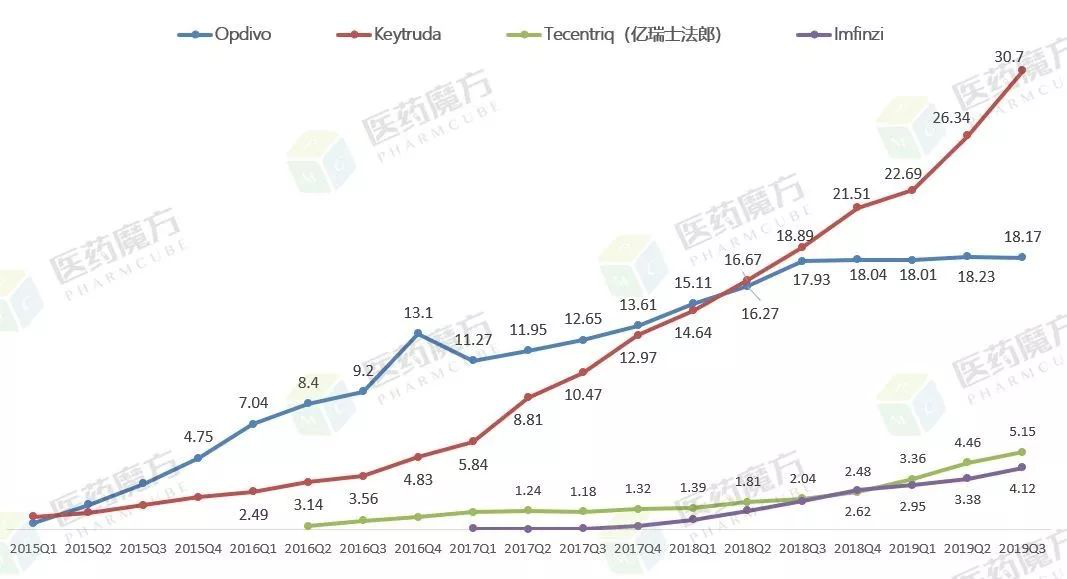
与全球率先推出尿路上皮癌适应症不同,Imfinzi在中国市场是将III期肺癌定为了首发适应症,这不失为一个明智选择。K药在中国上市的12个月内销售额突破20亿元,信迪利单抗和特瑞普利单抗凭借较小的适应症标签也能在一个季度斩获大约3.3亿的销售额,体现了市场对于PD-1/PD-L1药物的强劲需求。如今Imfinzi获批成为国内唯一一个专门针对III期肺癌的PD-1/PD-L1抗体,不仅具有适应症上的差异化,还可以借阿斯利康在中国肺癌领域的协同优势快速做大市场。?
当然,Imfinzi占有优势或者正在建立优势的细分适应症并不局限在III期NSCLC。就在11月30日,FDA还授予了Imfinzi一线治疗小细胞肺癌上市申请优先审评资格。目前为止,O药和K药虽然也获批治疗小细胞肺癌,但是均为三线用药,意味着PD-L1对这一领域患者的扩展走在了PD-1的前列。小细胞肺癌占全部肺癌患者的15%,也算是非常大的一个市场了,Imfinzi虽然比T药会晚一年左右拿下这个适应症,但是这两个PD-L1的较量一时间还难以分出胜负。?(转化医学网360zhyx.com)
 腾讯登录
腾讯登录







还没有人评论,赶快抢个沙发