通过机器学习预测癌症抗原能否引起免疫反应——新算法助力个性化癌症疫苗研究
| 导读 | 近日,北卡罗莱纳大学的研究人员设计并验证了一个新的机器学习算法模型,该模型可以预测特定肿瘤特异性抗原产生免疫反应的能力,有助于克服研制个性化癌症疫苗的重大障碍。 |

近日,北卡罗莱纳大学的研究人员设计并验证了一个新的机器学习算法模型,该模型可以预测特定肿瘤特异性抗原产生免疫反应的能力,有助于克服研制个性化癌症疫苗的重大障碍。

抗原是免疫系统区分正常细胞和癌细胞的标志,而肿瘤新生抗原(Neoantigen)的发现对癌症的诊断、过继性免疫治疗、肿瘤疫苗、个性化治疗起着极其重要的作用。随着高通量测序技术的发展以及国际大型肿瘤基因组研究项目(如COSMIC、TCGA)的开展,获得了大量肿瘤突变数据,为基于机器学习算法的抗原发现提供基础。
通过对癌症患者的基因组测序,往往可测出数万个突变,经过机器学习预测后可得到的新生抗原有数十个,但进入临床阶段后有免疫反应的寥寥无几甚至没有。如果算法能够预测出能产生免疫反应的新生抗原,就可以大大降低成本和缩短研究时间。

肿瘤疫苗制备流程图
当前的肿瘤新生抗原预测算法主要通过对表位/MHC亲和力预测选择潜在的抗原表位,这些算法最大的问题是都不能准确的预测抗原表位免疫原性,也就无法准确预测这些抗原能否触发人体免疫系统对抗癌症。
针对这个问题,研究人员设计并验证了一种新的机器学习算法,以预测特定肿瘤特异性抗原(tumor-specific antigen,TSA)产生免疫反应的能力。并发表在近日的《Cancer Immunology Research》上。
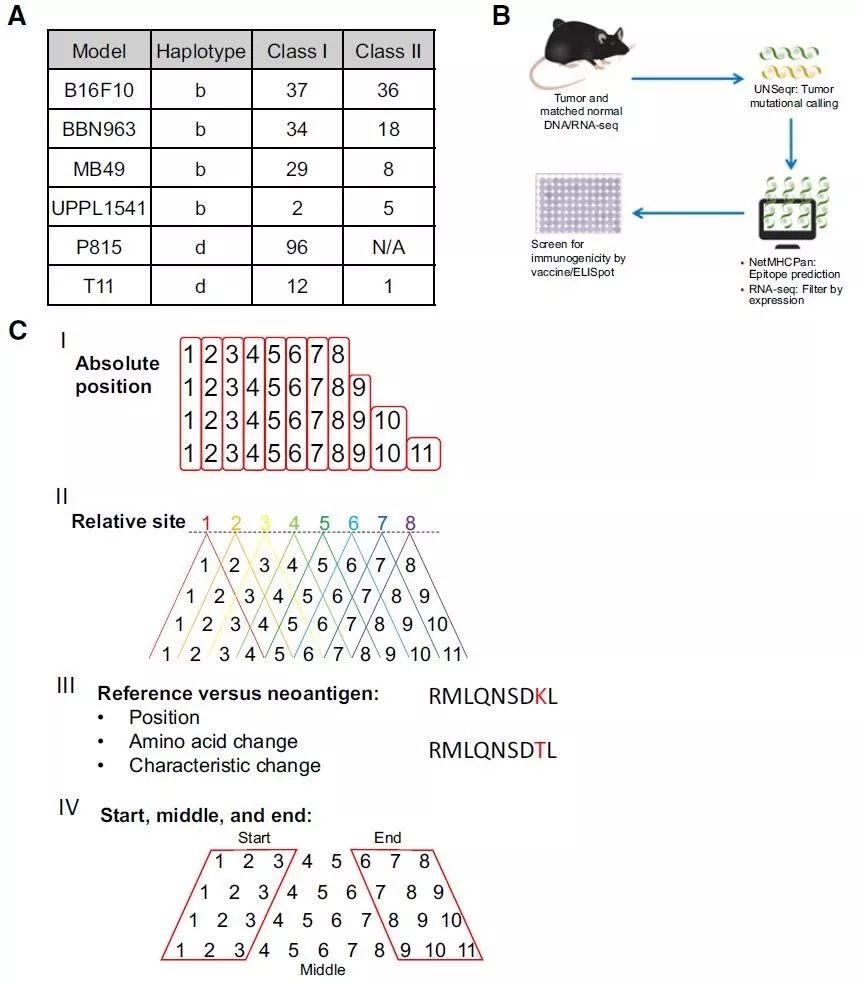
肿瘤抗原预测和抗原内在性质鉴定示意图。A,研究采用的各个肿瘤模型中MHC-I和MHC-II类新生抗原/mHA数量。B,新生抗原/mHA预测以及ELISpot验证流程。C,抗原性质鉴定,包括氨基酸序列以及:(I)绝对位置,(II) 相关位点,(III)突变位置 ,(IV)每个多肽的起始、中间和末端。
随后,研究人员将这个算法在两个小鼠肿瘤模型进行了验证,并证实该算法可以预测具有潜在治疗价值的抗原。
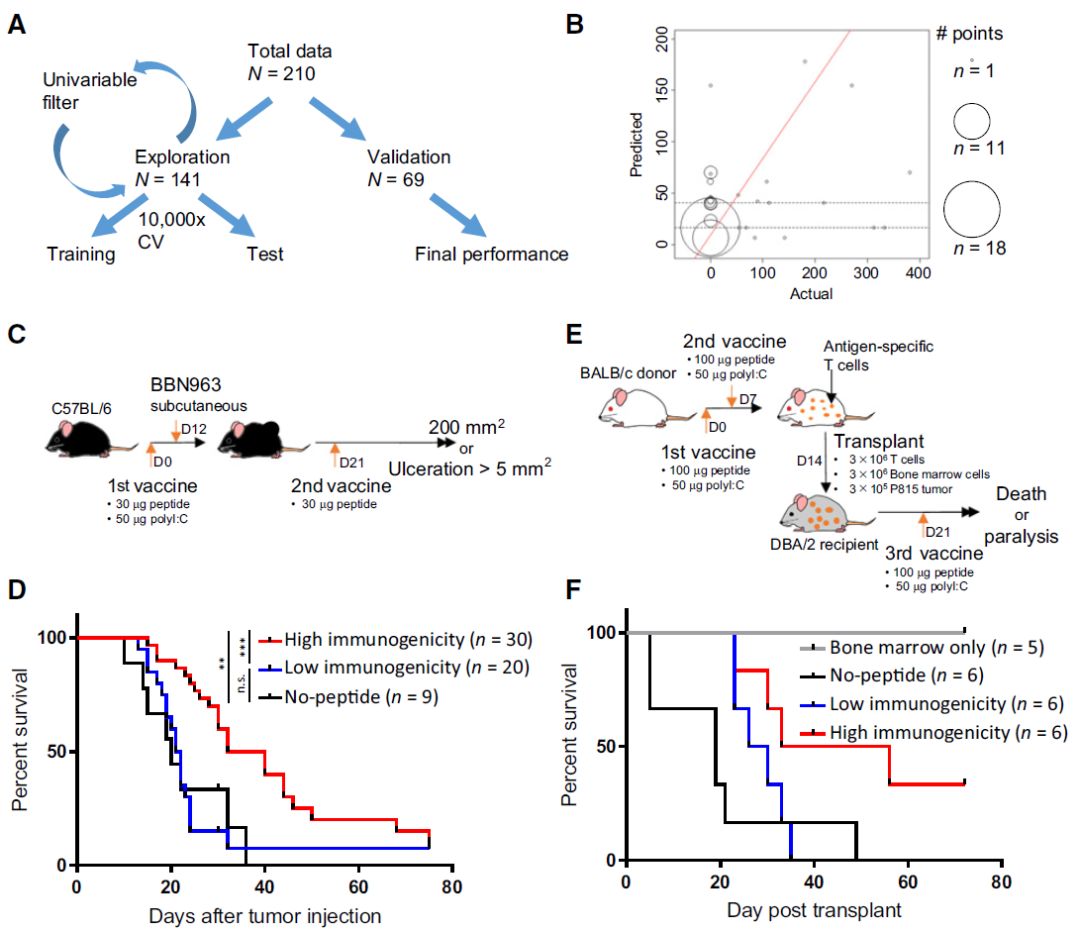
梯度推进模型(gradient boosting model, GBM)方法预测的肿瘤新生抗原/mHA免疫原性的验证。A,GBM模型的交叉验证方法示意图。B,最终的GBM在验证数据集中的表现,X轴表示实际的免疫原性评分,Y轴表示预测的免疫原性评分,圆圈大小表示抗原数量,红线为最佳拟合线。C和E为肿瘤疫苗的体内验证流程图,C为小鼠膀胱癌模型(BBN963),E为P815肥大细胞瘤小鼠模型。D和F为两种小鼠模型Kaplan–Meier生存曲线。
在小鼠模型中成功验证后,研究人员推测人类肿瘤新生抗原的免疫原性也有相似的规则。并通过TCGA数据库中结肠癌和肺腺癌相关数据集进行了验证,证明了该算法可发现肿瘤新生抗原与免疫原性的联系。
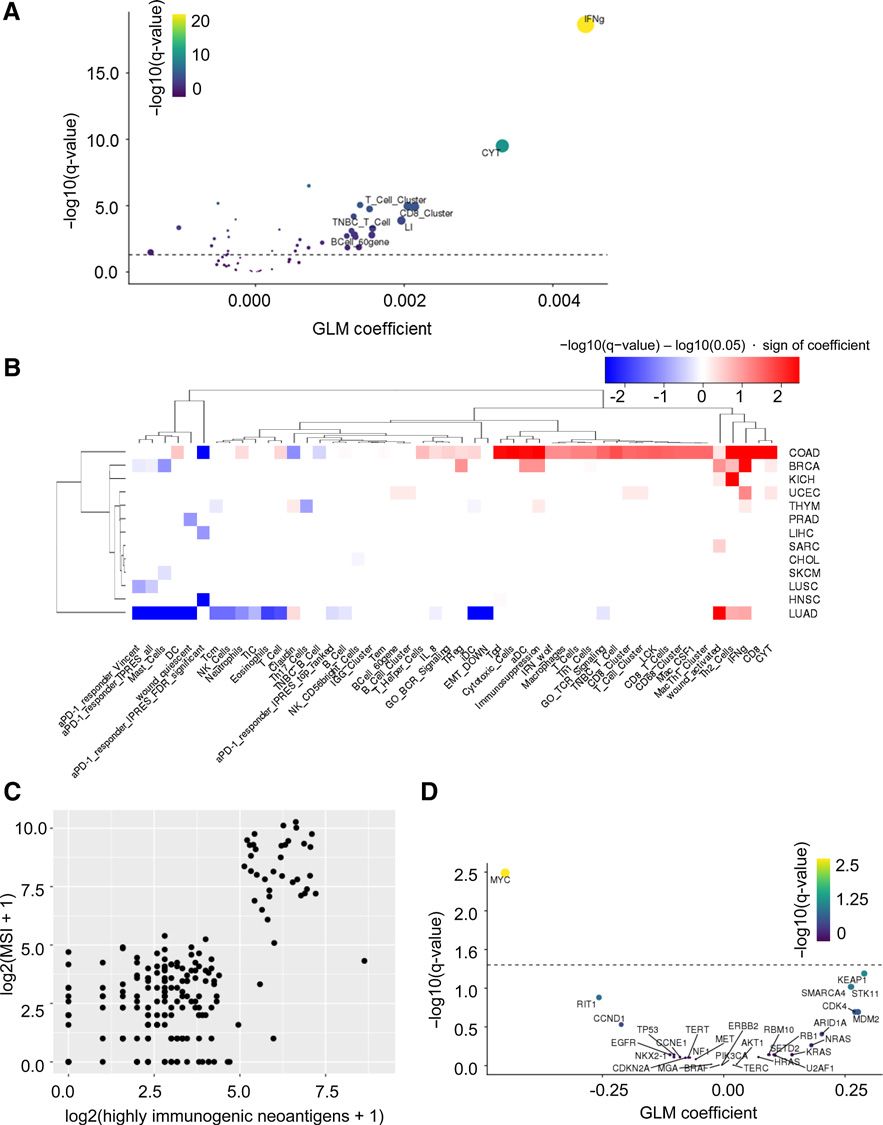
在TCGA人类数据库中预测的肿瘤新生抗原关联分析。A,TCGA泛癌数据集中HINs和IGS的数量关系,X轴为GLM系数,Y轴为-log10(q值)。B,每个TCGA数据集的HINs和IGS数量关系的GLM回归热图。C,TCGA结肠癌数据集的HINs(X轴)和MSI值(Y轴)的关系,D,IGS平均表达水平的GLM系数与-log10(q值)的火山图。
注:HINs(highly immunogenic neoantigens, 高免疫原性新生抗原),MSI (microsatellite instability, 微卫星不稳定性),IGS(Immune gene signatures,免疫活性基因表达谱)
随着肿瘤疫苗在肿瘤临床治疗上重要性的逐渐提升,该方法提高了预测抗原表位免疫原性的精确性,有助于更好的筛选肿瘤特异性抗原,缩短肿瘤疫苗临床应用的周期。
参考文献:
Machine-Learning Prediction of Tumor Antigen Immunogenicity in the Selection of Therapeutic Epitopes. Cancer Immunology Research(2019).
DOI: 10.1158/2326-6066.CIR-19-0155

 腾讯登录
腾讯登录









还没有人评论,赶快抢个沙发