帕金森免疫成因机制终破解!肠道感染是关键!
| 导读 | 被誉为人类的"第二基因组"的肠道菌群,近年来已经成为最火爆的研究领域之一。已有研究表明,肠道细菌可以加速阿尔茨海默病的发展。近日,肠道细菌重出江湖,再显神威,研究人员首次发现,小鼠肠道革兰氏阴性菌感染可诱发帕金森病的发生发展。 |
众所周知,帕金森氏病(Parkinson氏病)是伴有运动障碍的神经退行性疾病,已被证实其与黑质内核团多巴胺能神经元缺失有关,但其具体发病机制仍是未解之谜,而大量研究表明大约10%的PD病例是由于编码PINK1和Parkin等蛋白质的基因突变所致。Parkin最早在青少年Parkinson氏病的研究中被发现,现有模型认为,PINK1可磷酸化激活Parkin和泛素分子,使应激后损伤的线粒体发生泛素化修饰,经线粒体自噬途径(Mitophagy)完成降解清除。
尽管目前已证实PINK1和Parkin突变可引起Parkinson氏病,但Pink1−/−和Prkn−/−的小鼠模型却几乎未见有Parkinson氏病样运动障碍发生,研究人员猜测,小鼠模型的无菌环境是该现象的主要原因,接下来,他们给实验小鼠喂了大量的细菌,神奇的一幕发生了:小鼠们发病了。
以往的流行病学证据和基础研究表明,自身免疫反应极有可能是帕金森病的背后成因,而以上小发现给研究人员以灵感:或许肠道细菌的感染恰好是帕金森的免疫扳机触发点,通过诱导线粒体抗原呈递过程(mitochondrial antigen presentation,MitAP)引起CD8+T细胞发生线粒体特应的活化。
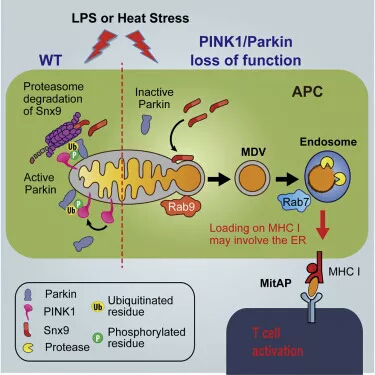
PINK1/Parkin的缺失导致MitAP
为证实这一推测,研究人员在Raw 264.7细胞内表达了糖蛋白gB(glycoprotein B)以指示抗原呈递,并感染了多种细菌,果然,只有革兰阴性菌可引起MitAP。随后,研究者分离了感染小鼠的脾细胞,发现Pink1敲除小鼠的抗原提呈细胞里出现了MitAP,产生了针对线粒体的杀伤性T细胞。
既往已有体外证据发现LPS可诱导多巴胺能神经元表达MHC-I分子,使其易感于CD8+T细胞的免疫作用。本研究人员在体外共培养中发现,与Pink1−/−小鼠神经元共培养可诱导杂交瘤细胞发生MitAP,并在共培养5天后发现40%多巴胺能神经元死亡。这些结果提示,在Pink1−/−小鼠感染模型中,发生了MitAP的CD8+T细胞在脑中浸润增加,进而引起多巴胺能神经元死亡。
机制搞清楚了,所以小鼠们到底有怎样的表现呢?
在吃了革兰阴性菌之后,小鼠感染不严重,20天左右就完全好了;但是在感染4个月以后,Pink1敲除小鼠开始“不会走路”了。它们明显全身都不太灵活,头抬不起来,特别是后腿的不灵活,有趣的是,给予左旋多巴后,小鼠又生龙活虎了--帕金森,没跑了。
本研究的关键之处在于将肠道感染模型引入到Parkinson氏病动物模型的研究中,从而解释了既往Pink1−/−小鼠因缺少炎症性干预未能呈现Parkinson氏病症状的原因。
神经退行性疾病的发生并非是单一因素促成,而是遗传、神经病理、感染免疫乃至更多因素共同参与的病理过程。我们还有很多工作要做,我们,仍然,任重道远。
参考文献:
https://www.nature.com/articles/s41586-019-1405-y
 腾讯登录
腾讯登录









还没有人评论,赶快抢个沙发