《Cancers》:两种抗癌药可改变肿瘤基因的表达!
| 导读 | 一项新的研究中发现,同时用两种抗癌药物治疗乳腺肿瘤可以通过两条不同的基因通阻止肿瘤细胞产生内分泌抵抗。 |
作者:Michael 编辑:Carrie
伊利诺伊大学Zeynep Madak-Erdogan教授及其研究团队在一项新的研究中发现,同时用两种抗癌药物治疗乳腺肿瘤可以通过两条不同的基因通阻止肿瘤细胞产生内分泌抵抗。
ERα(+)乳腺癌肿瘤患者中大多数病人的死亡是由于其肿瘤细胞对内分泌治疗产生了抗性进而导致肿瘤转移的发生。因此,我们迫切需要新的治疗方法来抵抗ERα(+)乳腺癌肿瘤产生内分泌抵抗,重新使其对现有内分泌治疗敏感。
伊利诺伊大学Zeynep Madak-Erdogan教授及其研究团队在一项新的研究中发现,同时用两种抗癌药物治疗乳腺肿瘤可以通过两条不同的基因通阻止肿瘤细胞产生内分泌抵抗。此研究阐明了联合靶向ERα和核转运蛋白XPO1可防止肿瘤细胞产生内分泌抗性的有效机制。该研究发表于最新的《Cancers》杂志。

虽然内分泌治疗目前是激素反应性乳腺癌治疗的最有效形式,但是一些患者要么不响应,要么随着时间的推移会对药物产生耐药性。这种情况称为内分泌抵抗,这会导致肿瘤细胞发生转移,最终导致患者死于激素反应性乳腺癌。
根据研究小组的先前研究,研究人员认为激素受体Erα和核转运基因XPO1两种共同作用可引起内分泌抵抗。同时,药物selinexor可以阻止XPO1蛋白的功能,4-OHT可以抑制雌激素受体对激素的反应,联合使用这两种药物可能比单独使用更为有效。

两种药物对基因表达的影响
(来源:Combined Targeting of Estrogen Receptor Alpha and XPO1 Prevent Akt Activation, Remodel Metabolic Pathways and Induce Autophagy to Overcome Tamoxifen Resistance)
在2016年发表于Molecular Endocrinology的一项研究中,Madak-Erdogan的研究小组发现,表达较高水平的XPO1和其他核转运基因的女性患者更可能产生内分泌抗性。
在目前的研究中,该团队使用4-OHT或selinexor以及两种药物联合使用来治疗内分泌抗性肿瘤细胞,进而明确这些治疗方案中的每一种药物是如何影响肿瘤的存活和功能的。他们发现,这种药物组合在降低肿瘤细胞活力方面比单独使用药物更有效。当他们在乳腺癌小鼠模型中测试这三种治疗方法时,他们发现4-OHT和selinexor的组合比单独使用一种药物能够更快和更完全地消灭肿瘤细胞。
在分析人类内分泌抗性乳腺肿瘤的遗传活动时,他们发现该药物组合增加了100多个基因的表达,并降低了其他132种不受这两种药物影响基因的表达。该药物组合似乎通过降低与内分泌抗性和转移相关基因的活性来维持肿瘤的清除工作,这其中包括调节控制细胞存活、增殖和迁移的Akt调节的信号通路基因的表达。
在内分泌抗性肿瘤中,XPO1通过调节Akt的活性帮助细胞发生突变,其通过重新调节乳腺癌细胞的代谢,为它们提供新的生存或转移条件。通过降低某些基因的表达,4-OHT和selinexor组合可以阻止肿瘤细胞激活这些信号通路,当针对肿瘤单独使用这两种药物的其中一种药物时,这种信号通路仍可被激活。
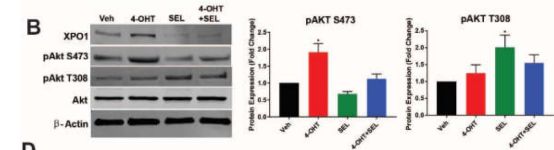
XPO1抑制剂对Akt通路的抑制
(来源:Combined Targeting of Estrogen Receptor Alpha and XPO1 Prevent Akt Activation, Remodel Metabolic Pathways and Induce Autophagy to Overcome Tamoxifen Resistance)
因此,这项研究证实联合阻断激素受体Erα和核转运基因XPO1,可通过抑制Akt调节的基因表达,进而避免肿瘤细胞出现内分泌抗性,这为激素敏感型乳腺癌的治疗提供了关键的信息。
参考文献
Yosef Landesman ,Zeynep Madak-Erdogan. Combined Targeting of Estrogen Receptor Alpha and XPO1 Prevent Akt Activation, Remodel Metabolic Pathways and Induce Autophagy to Overcome Tamoxifen Resistance
推荐内容

肿瘤组织原来是这样“招兵买马”的!
盘点|乳腺癌最新研究进展
到底是谁诱发了侵袭性乳腺癌?
(转化医学网360zhyx.com)
 腾讯登录
腾讯登录









还没有人评论,赶快抢个沙发