信达 PD-1 获批上市!国产第 2 家
| 导读 | 刚刚,Insight数据库显示信达PD-1(信迪利单抗注射液)CFDA办理状态变更为「在审批」。知情人士向Insight数据库透露,信迪利单抗已获CFDA批准上市。君实、信达首家之争2017年12月13日,信达生物的信迪单抗提交上市申请,用于治疗霍奇金淋巴瘤。后信迪利单抗首次上市申请被主动撤回。 |
刚刚,Insight 数据库显示信达 PD-1(信迪利单抗注射液)CFDA 办理状态变更为「在审批」。知情人士向 Insight 数据库透露,信迪利单抗已获 CFDA 批准上市。
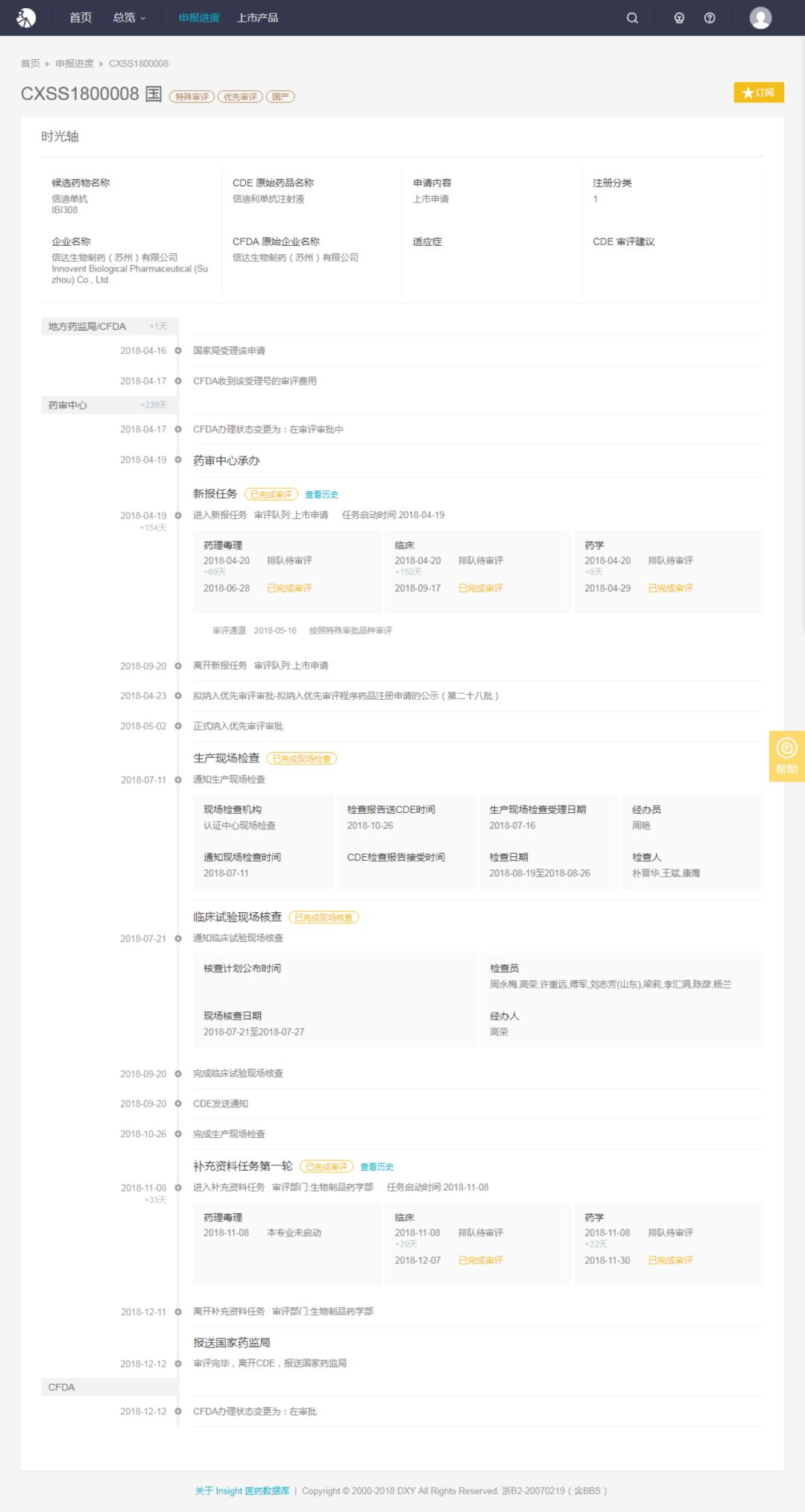
君实、信达首家之争
2017 年 12 月 13 日,信达生物的信迪单抗提交上市申请,用于治疗霍奇金淋巴瘤。后信迪利单抗首次上市申请被主动撤回。
2018 年 3 月 9 日,君实生物宣布特瑞普利单抗的新药上市申请获 CDE 正式受理,适应症为黑色素瘤。特瑞普利单抗是国产第 2 家提交上市申请的 PD-1/PD-L1 类药物。
2018 年 4 月 19 日,信达生物重新提交的 PD-1 单抗信迪利单抗注射液的上市申请 (CXSS1800008) 正式获得药品审评中心承办受理。
此后信达一直略慢一步,直至获批上市。
PD-1产品定价困局
目前我国已获批上市的 3 款 PD-1 分别是默沙东的 K 药、BMS 的 O 药和君实的特瑞普利单抗。
Opdivo 在 2017/11/2 申报上市,用于二线治疗非小细胞肺癌,6 月获批上市, Keytruda 在 2018/2/11 提交了上市申请,7 月获批上市,特瑞普利单抗在 2018/3/9 提交了上市申请,12 月 21 日获批上市。
其中,K 药在我国获批适应症为黑色素瘤。O 药在我国获批的适应症为 EGFR 阴性和 ALK 阴性、既往接受过含铂方案化疗后疾病进展或不可耐受的局部晚期或转移性非小细胞肺癌 (NSCLC) 成人患者。君实生物的特瑞普利单抗申报上市的适应症与已获批的 K 药相同。
信达与恒瑞的 PD-1 申报上市适应症相同,上市后不免要进行市场角逐。
王雅媛港股圈认为国产PD-1的市场大概如此:长期看药效,中期看销售,短期看速度。激烈的竞争将压制各家公司的利润率到一个低水平,只有疗效出现明显优势的公司,才能得到溢价。
首发的两家进口PD-1的价格。加上赠药,Keyturda是19万一年。Opdivo没有赠药,大概是36万一年(赠药仍未确定),但这两个价格都是全球最低,与香港比,都要便宜一半。
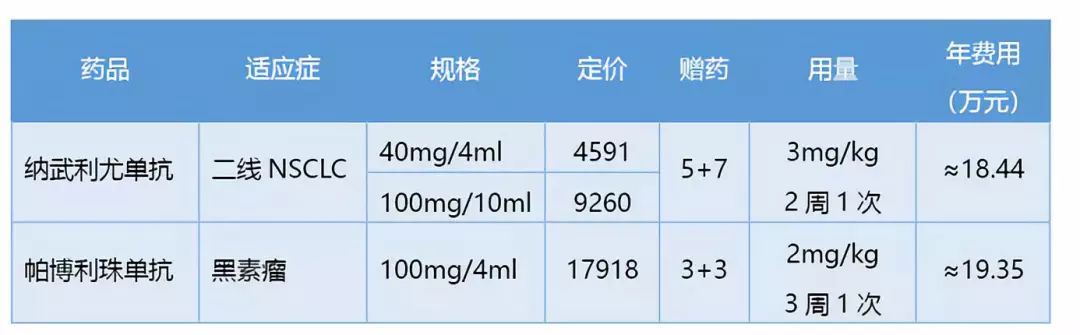
这个低定价完全是竞争造成的,进口的两家也明白,中国还有十几家pd-1在研,个个成本都低,有不少疗效也不差,就凭首发身份定个高价无疑于自断财路。
目前国产第一梯队的四家PD-1从定位上看,价格不会差太远,四家各有优势,也各有劣势,不好评判谁优谁劣,但临床设计都没有证明自己是me-better就对了。
国产PD-1的定价,哪怕销售能力再强,卖高价也不算一个好策略,到时因为价格太贵,医保不报销,那就是自寻短见了。
(转化医学网360zhyx.com)
 腾讯登录
腾讯登录







还没有人评论,赶快抢个沙发