这种基因突变导致1/4的人罹患癌症,并且还助力癌症生长!
| 导读 | 之前的相关研究表明,Ras基因是原癌基因,它发生突变以后就变成有致癌活性的癌基因。随着研究的继续深入,近日科学家发现,Ras基因的突变还可以抑制免疫系统的抗癌反应。 |
癌症的发生与原癌基因的突变有关。研究表明,原癌基因例如Ras基因发生突变,会导致25%的人类癌症的发生。
近日弗兰西斯克里克研究所的Matthew Coelho博士做了相关实验后发现,Ras基因发生突变还可以抑制免疫系统的抗癌反应。相关研究成果以题为《Oncogenic RAS Signaling Promotes Tumor Immunoresistance by Stabilizing PD-L1 mRNA》发表在了《Immunity》杂志上。

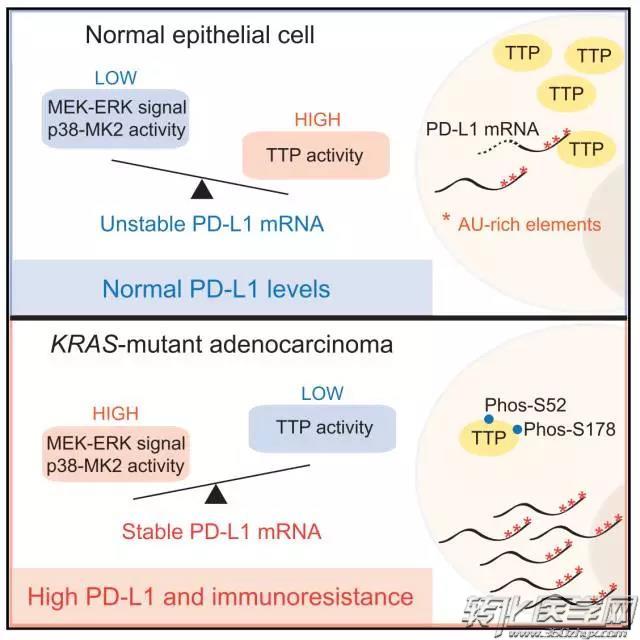
研究人员认为,具有致癌效应的Ras信号通路可以上调PD-L1的表达。相应的机制包括通过相关蛋白质的调节(TTP)来增加PD-L1 mRNA的稳定性。
1.PD-L1作用机理
PD-L1,即程序性死亡配体1(programmed death-ligand 1),通常在体内只会少量表达,它们的作用是防止免疫系统攻击健康的细胞。但肿瘤细胞也可以通过一个名为检查抑制剂的蛋白来表达PD-L1,以此来避免遭受免疫系统的“骚扰”。
2.PD-L1调控机理
虽然癌症免疫疗法最近以PD-L1为研究目标,试图通过它来揭示癌细胞,但科学家对于PD-L1仍然知之甚少。
例如,我们对PD-L1的调控机制仍不清楚。如果科学家能更好的理解这些机制,他们也许可以开发出新药,或是可以更好的支持现有的癌症免疫疗法。现阶段,现有的癌症免疫疗法理论上有好的结果但实际上治疗效果仍旧不佳。
“通过调节PD-L1mRNA的3’端非翻译区的相关基因,TTP可以实现对PD-L1表达的负调控,”Matthew Coelho 认为:“Ras的MEK信号下游通路会导致磷酸化,并且该信号通路也可以通过激酶MK2来抑制TTP。”
3.研究为用药开辟新航路
科学家还做了其它研究,例如对具有RAS突变的肿瘤小鼠给予相应的化合物来对抗PD-L1表达的Ras信号所带来的影响。实验结果显示,小鼠体内的肿瘤遭受到了免疫系统的攻击,体内肿瘤的生长速度明显减缓。
Matthew Coelho 在文中写道:“在人体内,PD-L1 mRNA的降解可以导致TTP表达的恢复,其结果是可以增强人体的抗肿瘤免疫能力。我们的研究证明了RAS可以驱动细胞内皮PD-L1的表达,从而可以改变RAS突变所致的癌症患者体内的免疫耐受表型。”
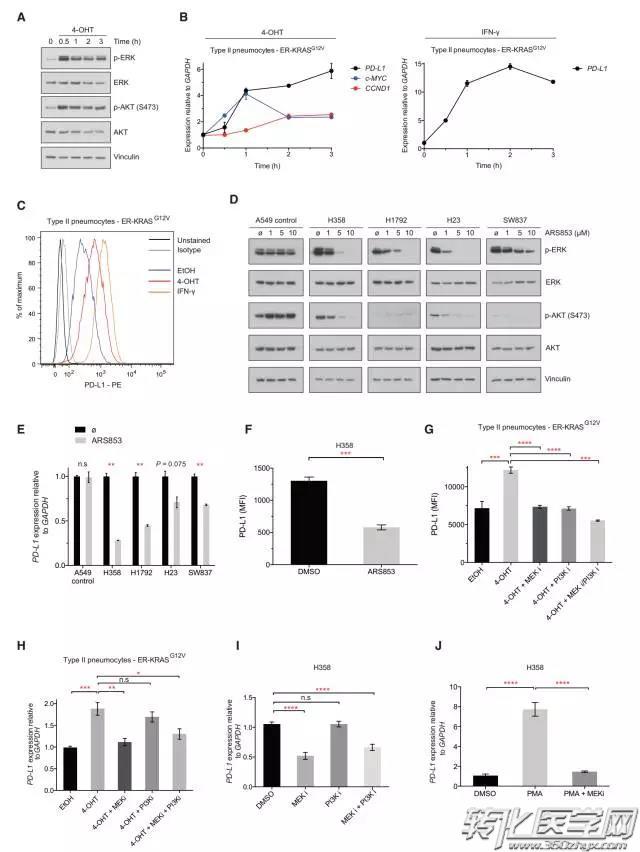
研究人员通过揭示Ras和PD-L1水平之间的因果联系和背后的机制,为使用不同药物联合治疗癌症提供了新的可能。
“了解不同的突变如何‘保护’癌细胞免受免疫系统的影响,将有助于我们为病人提供更精确有效的治疗方法。” Matthew Coelho博士说,“目前PD-L1蛋白的抗体正在进行初步的临床试验,对五个肺癌患者进行了相应的治疗,就目前来看,试验结果令人期待。现阶段,医生可以通过检测PD-L1的水平来帮助确定哪些患者对PD-L1蛋白抗体的反应最好,然后可以接受相应的治疗。”
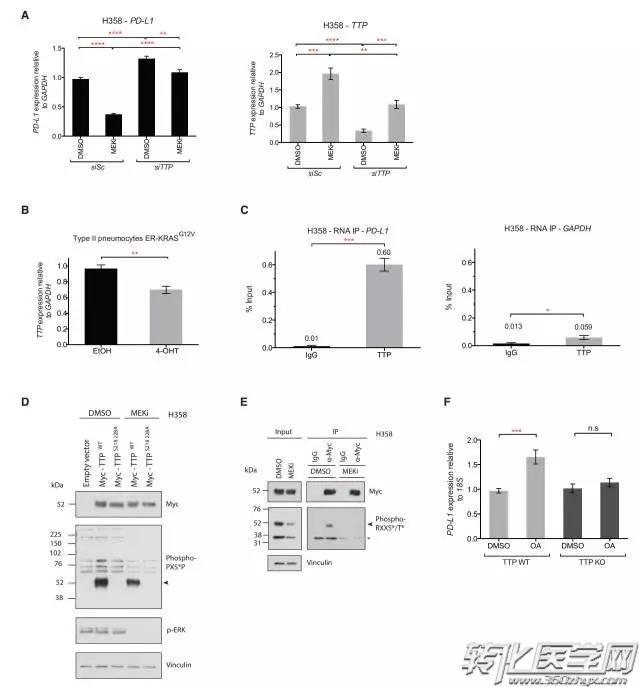
要使针对PD-L1的癌症免疫疗法起作用,首先,我们需要降低癌症患者癌细胞PD-L1的免疫抑制作用。其次,让癌细胞产生相应的抗原。
免疫系统只能识别并攻击产生“抗原”的癌细胞,这些抗原是免疫细胞能与之结合的分子,所以抗原对于免疫系统而言,至关重要。但是目前临床难以对癌细胞表面的抗原进行测定,所以现阶段PD-L1是决定这种免疫治疗是否会起作用的关键。因此,弄清是什么导致了癌症细胞中PD-L1的生成是非常重要的。
“我们的研究弄清了Ras基因突变在整个癌症的不同阶段所起到的作用。” 弗兰西斯克里克研究所的组长Julian Downward博士总结道, “我们已经知道,他们导致了大约四分之一的人类癌症,致使癌细胞生长、繁殖和扩散。Ras基因的突变也有助于‘保护’癌细胞免受免疫系统的影响,最终使得癌症更难治疗。了解这背后的机制将有助于我们在将来开发更好的治疗方法,例如,用能破坏癌症防御能力的药物来提高免疫治疗的效果。”
参考资料:Oncogenic RAS Signaling Promotes Tumor Immunoresistance by Stabilizing PD-L1 mRNA. Matthew A. Coelho, Sophie de Carne´ Tre´ cesson, Sareena Rana, Davide Zecchin, Christopher Moore, Miriam Molina-Arcas, Philip East, Bradley Spencer-Dene, Emma Nye, Karin Barnouin, Ambrosius P. Snijders, Wi S. Lai, Perry J. Blackshear, and Julian Downward. https://doi.org/10.1016/j.immuni.2017.11.016
(转化医学网360zhyx.com)
 腾讯登录
腾讯登录









还没有人评论,赶快抢个沙发