去噪存真|为何“看不见”的蛋白更有价值
| 导读 | Olink致力于将目光聚集于关键的生物学事件,减少数据噪音的干扰,加速从蛋白质组学精准识别出真正具有临床价值的标志物 |
编者按
在精准医疗的探索中,蛋白组学正以前所未有的深度,重塑我们对多种疾病机制的认知。与基因组相比,蛋白质作为生命活动的直接执行者,更能反映机体在“后天”环境中的动态变化,揭示那些基因组层面难以捕捉的病理机制。
近年来,随着高深度质谱、邻位延伸技术(PEA)等突破性方法的涌现,蛋白质组学已实现对数以千计蛋白的高通量检测。然而,技术能力的提升也带来了新的挑战:研究人员开始面临“如何在数千种蛋白质中,精准识别出真正具有临床价值的标志物”这一关键问题。尽管新技术能够产生海量数据,但若缺乏有效的聚焦方向,宝贵的生物学信号仍可能淹没在数据噪音的海洋中,难以转化为临床可用的可靠标志物。
今天,借助Olink Explore HT平台近期对6,800例样本的系统性分析结果,我们将和大家一同探讨:高通量蛋白质组学如何从“追求数量”转向“聚焦价值”。并直面一个核心问题:当技术已能覆盖近万种蛋白时,我们究竟需要多少数据,才能穿透噪音,触达真实的生物学真相?
打破误区
每份血样都应检出所有蛋白?
对6,800份泛人群血浆样本(包含随机选择的健康和疾病人群样本)的Olink Explore HT分析数据,绘制出了一幅清晰的蛋白质分布图谱。其核心规律在于:蛋白质的检出并非简单的“全或无”,而是存在“常见性观测蛋白”与“条件性存在蛋白”的不同类别。
常见性观测蛋白(Commonly observed proteins):在大多数情况下为大部份个体所共有。
条件性观测蛋白(Conditionally observed proteins):针对特定个体在特定的时间被观察到.
样本类型与蛋白“可见性”的关系
组织与血浆的惊人差异
一个更有趣的发现是,蛋白质的表达分布具有高度的组织特异性和功能依赖性。同一蛋白在不同样本类型中的"可见度"可能截然不同。这或许解释了为何许多组织中的明星标志物,到了血液中却难以检测。我们对同一组人群的部分细胞和组织样本进行了对比分析,并观察到了几组鲜明的案例。
血液中“常见”,组织中“罕见”
某些蛋白质在血液中为常见性观测蛋白,但在细胞和组织中则为条件性观测蛋白。例如,SERPINC1(凝血调节蛋白,由肝脏分泌)、GC(维生素D运输蛋白,由肝脏分泌)以及GUCA2A(食欲调节蛋白,由结肠与回肠分泌)在血浆样本中普遍可被检测(检出率99.9%),反映出其在循环系统中的稳定存在。然而,由于这些蛋白的组织来源具有特异性,SERPINC1 和 GC 仅由肝脏表达,而 GUCA2A 仅由结肠和回肠表达。当对164份不同细胞和组织的裂解液样本进行检测,这些蛋白质仅在其来源组织中被检测到(数据见下图)。这也表明了,采用Olink Explore平台所获得的检测结果符合样本的生物学特性。
与分泌至血液中广泛分布的蛋白质相反,另一类蛋白因其细胞内定位特性,在血液中难以检测,却在特定组织或细胞中高表达。例如,转录因子TP53主要定位于细胞核内,而雌激素受体ESR1作为膜结合蛋白,特异性表达于子宫内膜、乳腺等激素应答组织。这两类蛋白在血液中的检出率极低,但在相应的组织或细胞裂解物中可被稳定检测。这一分布差异不仅反映了蛋白质功能与其亚细胞定位、组织表达模式之间的紧密关联,也为生物标志物研究提供了重要启示:在试验设计时,应依据目标蛋白的生物学特性,合理选择不同类型的样本,以提高标志物检出的有效性和准确性。
条件性观测蛋白的临床潜力
在蛋白质组学研究中,低检出率蛋白可能被视为“无关信号”而忽略。然而,基于Olink技术的一系列研究表明,这类条件性观测蛋白恰恰具备重要的生物标志物潜力。符合“稀缺价值”理论:若某一蛋白在健康人群中难以捕捉,却在特定疾病队列中高频出现,则其很可能标志着关键病理过程,具备显著的标志物价值。
癌症早诊有效“工具”
CEACAM5(癌胚抗原相关细胞粘附分子5)在6,800份泛人群血浆样本中检出率仅为1.3%,但在特定的结直肠癌研究队列中,检出率显著提升至78.4%。这一跨越不同人群的显著差异,不仅印证了CEACAM5在区分结直肠癌患者与健康个体方面的鉴别能力,也凸显了其作为潜在诊断标志物的早期应用价值。
 疾病分层精准“利器”
疾病分层精准“利器”
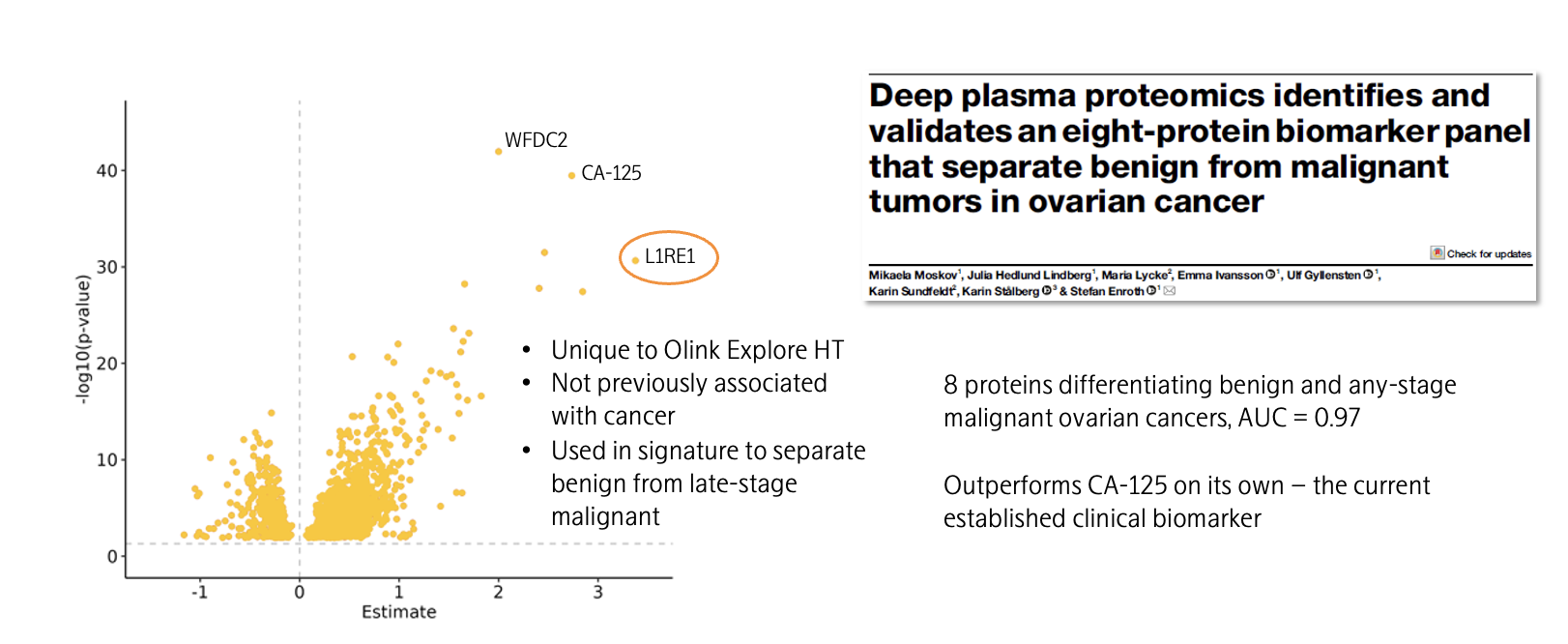
L1RE1(LINE-1反转录转座子元件ORF1蛋白)在广泛人群血浆样本中的检出率仅为8.5%,但在III-IV期恶性卵巢癌患者中的检出率为77.7%(在良性肿瘤队列中为9.6%)。瑞典乌普萨拉大学免疫学、遗传学和病理学系Ulf Gyllensten教授团队利用Olink Explore HT技术,在未经治疗的卵巢癌队列中验证了L1RE1等蛋白在区分良恶性卵巢癌方面的能力。该研究首次提出L1RE1可作为鉴别晚期卵巢癌与良性肿瘤的潜在生物标志物,此前L1RE1尚未被报道与癌症相关。
 以真实的生物学视角,加速标志物发现
以真实的生物学视角,加速标志物发现
Olink Explore平台检测结果的可靠性及其所带来的深刻生物学洞察,已获得全球学术界与大型队列研究的广泛验证,包括截止到2025年10月份已发表的3,200余篇同行评议论文,以及UK Biobank制药蛋白组学(UKB-PPP)和再生元遗传学中心等多项权威项目的认可。
此外,发表于《Science Advances》与《Nature》等顶刊的重要研究均已表明,尽管Olink在蛋白检测数量上并非最高,其数据却能揭示更多具有生物学意义的表型关联。这源于Olink研发端对于蛋白标志物库的“精挑细选”与“严格验证”:通过精准聚焦与系统验证,确保所选蛋白覆盖关键生物学通路,同时具备高度的准确性与临床应用潜力。
Olink希望通过Explore平台,不仅提供一种前沿的高通量蛋白组学技术,更推动一种研究范式的转变。我们理解到,蛋白质组学的价值边界不在于检测蛋白的数量,而在于能否从海量数据中识别真正驱动生物学过程的关键信号。
正如KTH皇家理工学院转化蛋白质组学教授、HUPO(人类血浆蛋白质组项目)主席Jochen Schwenk教授所言:
 基于“常见性观测蛋白”与“条件性观测蛋白”的分类框架,研究人员能够:
基于“常见性观测蛋白”与“条件性观测蛋白”的分类框架,研究人员能够:
建立起更可靠的基础参考范围;
优先关注到在特定疾病队列中显著高发的“条件性蛋白质”;
构建更具特异性和临床相关性的生物标志物模型。
最终将目光聚焦于关键的生物学事件,减少数据噪音的干扰,加速从蛋白质组学数据到可临床应用的标志物转化,为精准医疗开辟更为清晰、可靠的研究路径。
参考文献:
1. John E Blume, Michael Wilhelmsen, Ryan W Benz, et.al, Discovery and Validation of Plasma-Protein Biomarker Panels for the Detection of Colorectal Cancer and Advanced Adenoma in a Danish Collection of Samples from Patients Referred for Diagnostic Colonoscopy, The Journal of Applied Laboratory Medicine, Volume 1, Issue 2, 1 September 2016, Pages 181–193, https://doi.org/10.1373/jalm.2016.020271
2. Moskov, M., Hedlund Lindberg, J., Lycke, M. et al. Deep plasma proteomics identifies and validates an eight-protein biomarker panel that separate benign from malignant tumors in ovarian cancer. Commun Med 5, 230 (2025). https://doi.org/10.1038/s43856-025-00945-0
3. Katz DH, Robbins JM, Deng S, et al. Proteomic profiling platforms head to head: Leveraging genetics and clinical traits to compare aptamer- and antibody-based methods. Sci Adv. 2022 Aug 19;8(33):eabm5164. doi: 10.1126/sciadv.abm5164. Epub 2022 Aug 19. PMID: 35984888; PMCID: PMC9390994.
4. Eldjarn, G.H., Ferkingstad, E., Lund, S.H. et al. Large-scale plasma proteomics comparisons through genetics and disease associations. Nature 622, 348–358 (2023). https://doi.org/10.1038/s41586-023-06563-x
具体来说,我们基于专利PEA技术,秉承严谨和透明的科学精神,开发并充分验证了一系列开创性的Olink Panel。
这些Panel可赋能科学家,通过在1-6µl体液中精确检测5-5400+种生物标志物,更加充分地理解实时生物学。从而,借助多组学发现pQTL等创新药物靶点;筛选更好的疾病预测和预后标志物;理解药物作用的MoA, Safety, PK, PD, Dose;拓展已上市药物的适应症;开发伴随诊断;加速药物研发进程,降低药物研发成本;同时促进从临床科研到临床应用的转化;提高肿瘤等疾病早筛方法的灵敏度和特异性,并最终达致精准医学。
Olink现已覆盖100%主要信号通路,实现生物学意义上的超灵敏无偏靶向蛋白组学(兼容各种样本类型,对传统方法无法胜任的血浆血清等体液样本尤其适用)。
官网:https://www.olink.com
电话:+86 21 5077 8771
邮箱:China@olink.com
地址:上海市浦东新区沪南路2157弄2号1011
在精准医疗的探索中,蛋白组学正以前所未有的深度,重塑我们对多种疾病机制的认知。与基因组相比,蛋白质作为生命活动的直接执行者,更能反映机体在“后天”环境中的动态变化,揭示那些基因组层面难以捕捉的病理机制。
近年来,随着高深度质谱、邻位延伸技术(PEA)等突破性方法的涌现,蛋白质组学已实现对数以千计蛋白的高通量检测。然而,技术能力的提升也带来了新的挑战:研究人员开始面临“如何在数千种蛋白质中,精准识别出真正具有临床价值的标志物”这一关键问题。尽管新技术能够产生海量数据,但若缺乏有效的聚焦方向,宝贵的生物学信号仍可能淹没在数据噪音的海洋中,难以转化为临床可用的可靠标志物。
今天,借助Olink Explore HT平台近期对6,800例样本的系统性分析结果,我们将和大家一同探讨:高通量蛋白质组学如何从“追求数量”转向“聚焦价值”。并直面一个核心问题:当技术已能覆盖近万种蛋白时,我们究竟需要多少数据,才能穿透噪音,触达真实的生物学真相?
打破误区
每份血样都应检出所有蛋白?
对6,800份泛人群血浆样本(包含随机选择的健康和疾病人群样本)的Olink Explore HT分析数据,绘制出了一幅清晰的蛋白质分布图谱。其核心规律在于:蛋白质的检出并非简单的“全或无”,而是存在“常见性观测蛋白”与“条件性存在蛋白”的不同类别。
常见性观测蛋白(Commonly observed proteins):在大多数情况下为大部份个体所共有。
条件性观测蛋白(Conditionally observed proteins):针对特定个体在特定的时间被观察到.

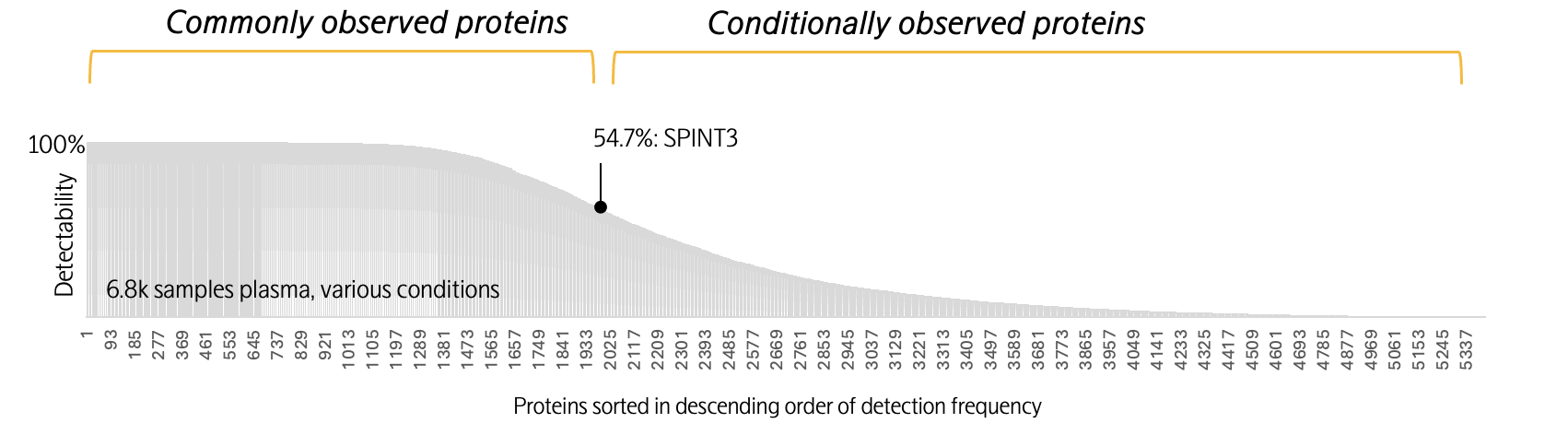
Olink Explore HT在6800份多维样本中的蛋白质检出率
(横坐标为1-5400号蛋白质,纵坐标为超出检出限的样本比例)
以SPINT3蛋白为例,它是一种具有组织特异性与生理特异性的蛋白质,主要由男性生殖组织产生,为典型的“条件性观测蛋白”。在6,800份血浆样本中,其54.7%的检出率精准匹配了研究群体的性别比例,充分验证了Olink Explore平台检测的生物学合理性。样本类型与蛋白“可见性”的关系
组织与血浆的惊人差异
一个更有趣的发现是,蛋白质的表达分布具有高度的组织特异性和功能依赖性。同一蛋白在不同样本类型中的"可见度"可能截然不同。这或许解释了为何许多组织中的明星标志物,到了血液中却难以检测。我们对同一组人群的部分细胞和组织样本进行了对比分析,并观察到了几组鲜明的案例。
血液中“常见”,组织中“罕见”
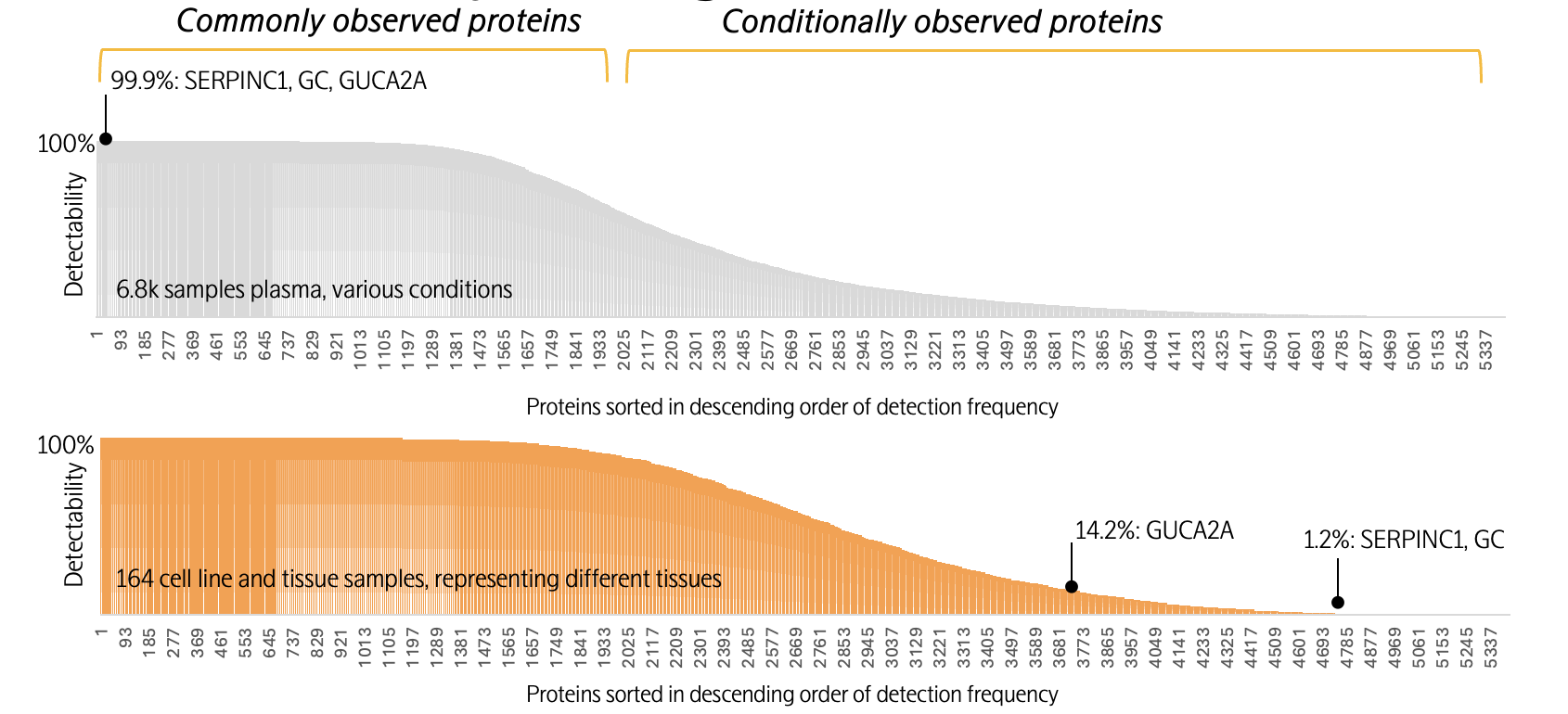
某些蛋白质在血液中为常见性观测蛋白,但在细胞和组织中则为条件性观测蛋白。例如,SERPINC1(凝血调节蛋白,由肝脏分泌)、GC(维生素D运输蛋白,由肝脏分泌)以及GUCA2A(食欲调节蛋白,由结肠与回肠分泌)在血浆样本中普遍可被检测(检出率99.9%),反映出其在循环系统中的稳定存在。然而,由于这些蛋白的组织来源具有特异性,SERPINC1 和 GC 仅由肝脏表达,而 GUCA2A 仅由结肠和回肠表达。当对164份不同细胞和组织的裂解液样本进行检测,这些蛋白质仅在其来源组织中被检测到(数据见下图)。这也表明了,采用Olink Explore平台所获得的检测结果符合样本的生物学特性。

5,400种蛋白质在血液和细胞组织裂解液中的检出范围
(SERPINC1, GC和CUCA2A;请注意,下图与上图的横坐标蛋白编号并非一一对应)
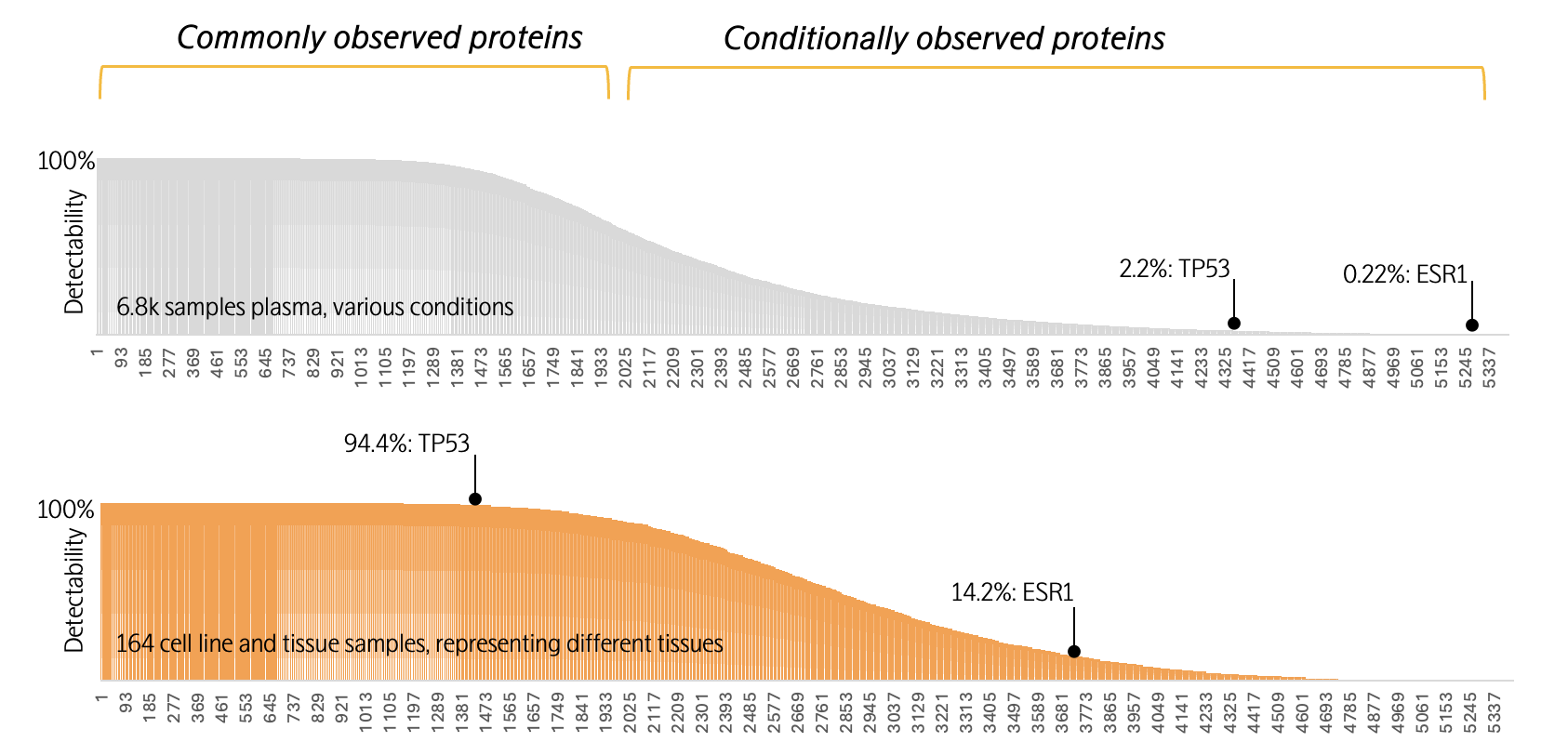
组织中“常见”,血液中“罕见”与分泌至血液中广泛分布的蛋白质相反,另一类蛋白因其细胞内定位特性,在血液中难以检测,却在特定组织或细胞中高表达。例如,转录因子TP53主要定位于细胞核内,而雌激素受体ESR1作为膜结合蛋白,特异性表达于子宫内膜、乳腺等激素应答组织。这两类蛋白在血液中的检出率极低,但在相应的组织或细胞裂解物中可被稳定检测。这一分布差异不仅反映了蛋白质功能与其亚细胞定位、组织表达模式之间的紧密关联,也为生物标志物研究提供了重要启示:在试验设计时,应依据目标蛋白的生物学特性,合理选择不同类型的样本,以提高标志物检出的有效性和准确性。

5,400种蛋白质在血液和细胞组织裂解液中的检出范围
(TP53和ESR1;请注意,下图与上图的横坐标蛋白编号并非一一对应)
“稀缺”的价值条件性观测蛋白的临床潜力
在蛋白质组学研究中,低检出率蛋白可能被视为“无关信号”而忽略。然而,基于Olink技术的一系列研究表明,这类条件性观测蛋白恰恰具备重要的生物标志物潜力。符合“稀缺价值”理论:若某一蛋白在健康人群中难以捕捉,却在特定疾病队列中高频出现,则其很可能标志着关键病理过程,具备显著的标志物价值。
癌症早诊有效“工具”
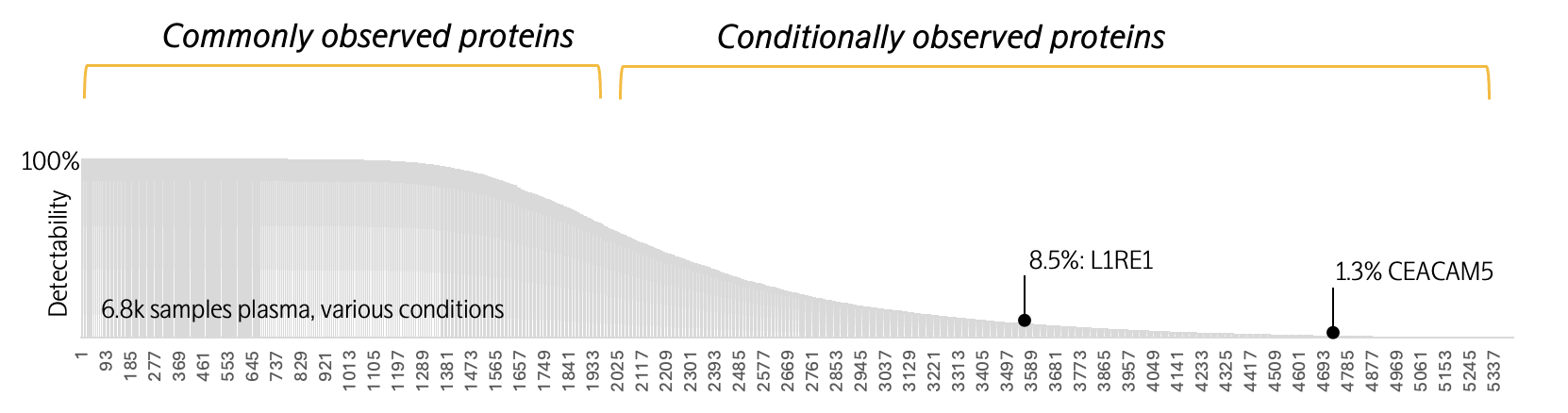
CEACAM5(癌胚抗原相关细胞粘附分子5)在6,800份泛人群血浆样本中检出率仅为1.3%,但在特定的结直肠癌研究队列中,检出率显著提升至78.4%。这一跨越不同人群的显著差异,不仅印证了CEACAM5在区分结直肠癌患者与健康个体方面的鉴别能力,也凸显了其作为潜在诊断标志物的早期应用价值。

L1RE1(LINE-1反转录转座子元件ORF1蛋白)在广泛人群血浆样本中的检出率仅为8.5%,但在III-IV期恶性卵巢癌患者中的检出率为77.7%(在良性肿瘤队列中为9.6%)。瑞典乌普萨拉大学免疫学、遗传学和病理学系Ulf Gyllensten教授团队利用Olink Explore HT技术,在未经治疗的卵巢癌队列中验证了L1RE1等蛋白在区分良恶性卵巢癌方面的能力。该研究首次提出L1RE1可作为鉴别晚期卵巢癌与良性肿瘤的潜在生物标志物,此前L1RE1尚未被报道与癌症相关。

Olink Explore平台检测结果的可靠性及其所带来的深刻生物学洞察,已获得全球学术界与大型队列研究的广泛验证,包括截止到2025年10月份已发表的3,200余篇同行评议论文,以及UK Biobank制药蛋白组学(UKB-PPP)和再生元遗传学中心等多项权威项目的认可。
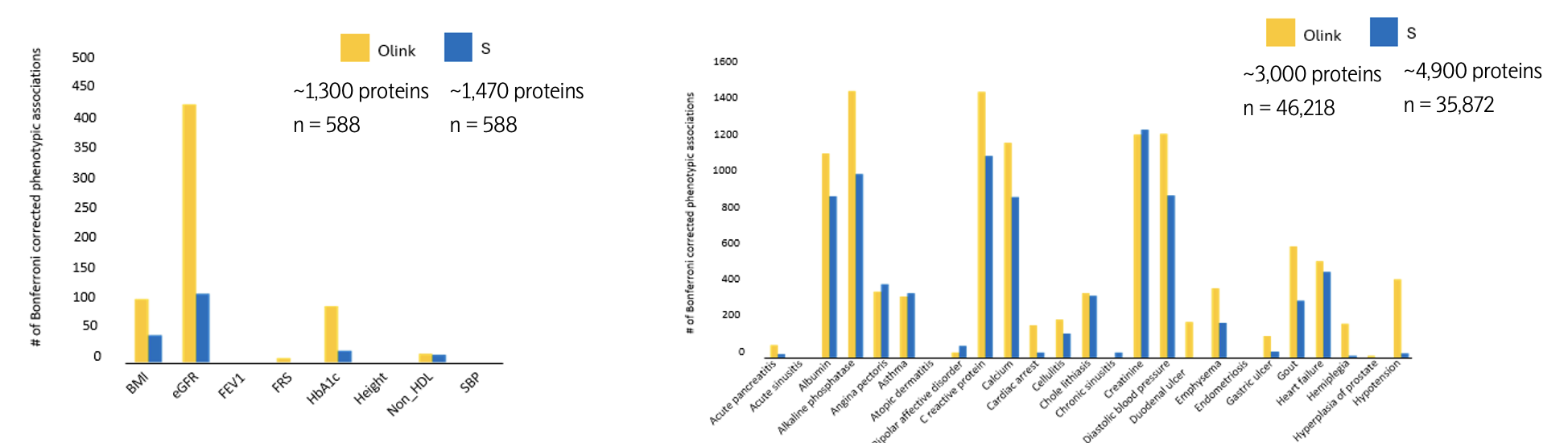
此外,发表于《Science Advances》与《Nature》等顶刊的重要研究均已表明,尽管Olink在蛋白检测数量上并非最高,其数据却能揭示更多具有生物学意义的表型关联。这源于Olink研发端对于蛋白标志物库的“精挑细选”与“严格验证”:通过精准聚焦与系统验证,确保所选蛋白覆盖关键生物学通路,同时具备高度的准确性与临床应用潜力。

横坐标代表不同的疾病表型,纵坐标代表与表型关联的蛋白比例
左图数据来源:Katz et al., Sci. dv.8,eabm5164(2022);
右图数据来源:Eldjarn et al., Nature 622, 348–358 (2023)
展望未来Olink希望通过Explore平台,不仅提供一种前沿的高通量蛋白组学技术,更推动一种研究范式的转变。我们理解到,蛋白质组学的价值边界不在于检测蛋白的数量,而在于能否从海量数据中识别真正驱动生物学过程的关键信号。
正如KTH皇家理工学院转化蛋白质组学教授、HUPO(人类血浆蛋白质组项目)主席Jochen Schwenk教授所言:

Jochen Schwenk 教授
“我并不期望所有2万个基因编码的蛋白质都出现在每个人的循环系统中。特定的蛋白质子集可能只在某个特定时间点存在于血液循环中,以标记潜在的生物学过程。”
建立起更可靠的基础参考范围;
优先关注到在特定疾病队列中显著高发的“条件性蛋白质”;
构建更具特异性和临床相关性的生物标志物模型。
最终将目光聚焦于关键的生物学事件,减少数据噪音的干扰,加速从蛋白质组学数据到可临床应用的标志物转化,为精准医疗开辟更为清晰、可靠的研究路径。
参考文献:
1. John E Blume, Michael Wilhelmsen, Ryan W Benz, et.al, Discovery and Validation of Plasma-Protein Biomarker Panels for the Detection of Colorectal Cancer and Advanced Adenoma in a Danish Collection of Samples from Patients Referred for Diagnostic Colonoscopy, The Journal of Applied Laboratory Medicine, Volume 1, Issue 2, 1 September 2016, Pages 181–193, https://doi.org/10.1373/jalm.2016.020271
2. Moskov, M., Hedlund Lindberg, J., Lycke, M. et al. Deep plasma proteomics identifies and validates an eight-protein biomarker panel that separate benign from malignant tumors in ovarian cancer. Commun Med 5, 230 (2025). https://doi.org/10.1038/s43856-025-00945-0
3. Katz DH, Robbins JM, Deng S, et al. Proteomic profiling platforms head to head: Leveraging genetics and clinical traits to compare aptamer- and antibody-based methods. Sci Adv. 2022 Aug 19;8(33):eabm5164. doi: 10.1126/sciadv.abm5164. Epub 2022 Aug 19. PMID: 35984888; PMCID: PMC9390994.
4. Eldjarn, G.H., Ferkingstad, E., Lund, S.H. et al. Large-scale plasma proteomics comparisons through genetics and disease associations. Nature 622, 348–358 (2023). https://doi.org/10.1038/s41586-023-06563-x
Olink Proteomics
Part of Thermo Fisher Scientific
Olink Proteomics创立于瑞典乌普萨拉,致力于突破蛋白检测在“多重能力/特异性”、“灵敏度”和“检测通量”等方面的综合瓶颈,进而实现超灵敏多重蛋白标志物检测、无偏靶向蛋白质组学和精准蛋白组学,以帮助蛋白标志物的发现、药物研发、转化医学、以及让“多组学整合”真正切实可行。具体来说,我们基于专利PEA技术,秉承严谨和透明的科学精神,开发并充分验证了一系列开创性的Olink Panel。
这些Panel可赋能科学家,通过在1-6µl体液中精确检测5-5400+种生物标志物,更加充分地理解实时生物学。从而,借助多组学发现pQTL等创新药物靶点;筛选更好的疾病预测和预后标志物;理解药物作用的MoA, Safety, PK, PD, Dose;拓展已上市药物的适应症;开发伴随诊断;加速药物研发进程,降低药物研发成本;同时促进从临床科研到临床应用的转化;提高肿瘤等疾病早筛方法的灵敏度和特异性,并最终达致精准医学。
Olink现已覆盖100%主要信号通路,实现生物学意义上的超灵敏无偏靶向蛋白组学(兼容各种样本类型,对传统方法无法胜任的血浆血清等体液样本尤其适用)。
官网:https://www.olink.com
电话:+86 21 5077 8771
邮箱:China@olink.com
地址:上海市浦东新区沪南路2157弄2号1011
 腾讯登录
腾讯登录







还没有人评论,赶快抢个沙发